| Issue |
Med Sci (Paris)
Volume 25, Number 4, Avril 2009
|
|
|---|---|---|
| Page(s) | 325 - 327 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2009254325 | |
| Published online | 15 April 2009 | |
« Mort sur ordonnance » ou comment l’anticorps anti-CD3 utilise l’apoptose pour induire la tolérance
CD3-specific antibody-induced T cell apoptosis and apoptotic cell uptake lead to CD3-specific antibody-induced tolerance
Inserm UMR645, Établissement Français du Sang Bourgogne Franche-Comté, Université de Franche-Comté, 1, boulevard Alexander Fleming, BP 1937, 25020 Besançon, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Anticorps thérapeutiques dans la prévention du rejet de greffe
La prévention du rejet de l’organe greffé après une transplantation repose sur deux stratégies successives : un premier traitement dit d’induction utilise les immunoglobulines anti-lymphocytaires polyclonales et permet une élimination transitoire des lymphocytes. Cette première étape est suivie d’un traitement d’entretien - qui sera pris durant toute la vie - basé sur l’utilisation d’immunosuppresseurs chimiques. Cette immunosuppression généralisée expose le receveur à de nombreuses complications, notamment infectieuses. Il est donc intéressant de développer des stratégies visant à établir un état de tolérance spécifique aux antigènes exprimés par l’organe greffé tout en conservant la possibilité de répondre aux autres antigènes auxquels nous expose notre environnement (notamment les pathogènes). Les anticorps anti-CD3 ont été utilisés initialement en transplantation comme traitement d’induction, puis abandonnés en raison de leurs effets secondaires liés en partie à leur origine animale. Des progrès technologiques ont permis ensuite l’obtention d’anticorps chimériques ou humanisés offrant une meilleure efficacité thérapeutique et une moindre toxicité et permettant d’envisager à nouveau l’utilisation d’anticorps monoclonaux en transplantation. Ainsi, les anticorps anti-CD25 chimériques1 (Basiliximab) ou humanisés (Daclizumab) sont proposés aujourd’hui dans le traitement d’induction après greffe de rein à la place des globulines anti-lymphocytaires polyclonales. Ces évolutions technologiques ont relancé la recherche préclinique et le développement d’essais cliniques utilisant les anticorps anti-CD3 notamment dans le diabète auto-immun [1].
Efficacite de l’anticorps anti-CD3 dans la prévention du diabète chez la souris
Lucienne Chatenoud et son équipe ont montré que l’administration d’anticorps anti-CD3 à des souris génétiquement programmées pour devenir diabétiques, si elle est faite dans les 10 premiers jours suivant l’apparition des symptômes, permet de prévenir la maladie [1]. Les facteurs impliqués dans cette prévention du diabète à long terme (malgré un traitement de courte durée) sont le TGF-β (transforming growth factor β) et les lymphocytes T régulateurs [2]. Notre étude publiée dans Nature Medicine au mois de mai 2008 [3] fait le lien entre ces éléments en identifiant les mécanismes à l’origine de la tolérance à long terme obtenue après une injection d’anticorps anti-CD3. En effet, l’anticorps anti-CD3 induit l’apoptose de la plupart des lymphocytes T qui sont ensuite éliminés par les cellules phagocytaires, comme les macrophages et les cellules dendritiques immatures. En réponse, ces cellules libèrent du TGF-β qui, à son tour, permet la conversion en lymphocytes T régulateurs des lymphocytes T CD4 émergeant après la déplétion secondaire à l’anti-CD3 (Figure 1). Le rôle pivot des cellules phagocytaires dans l’induction de tolérance par des anticorps anti-CD3 a été illustré dans un modèle expérimental de maladie auto-immune, l’encéphalomyélite auto-immune expérimentale [3]. Dans ce modèle, la déplétion des cellules phagocytaires par l’injection de liposomes toxiques pour ces cellules, prévient l’effet bénéfique de l’anticorps anti-CD3 [3]. Ces travaux amènent à reconsidérer la relation entre la mort apoptotique et la réponse immunitaire ; l’apoptose qui résulte de l’action de l’anticorps anti-CD3 serait le point clef dans l’induction de tolérance.
 |
Figure 1. Mécanisme d’induction de tolérance par l’anticorps anti-CD3 L’induction de tolérance après traitement par l’anticorps anti-CD3 se décompose en 3 phases : (1) apoptose des lymphocytes T induite par l’anticorps anti-CD3 (immunosuppression transitoire) ; (2) élimination des lymphocytes apoptotiques par les cellules phagocytaires (macrophages et cellules dendritiques immatures) qui vont libérer du TGF-β ; (3) conversion ou expansion de lymphocytes T CD4 régulateurs sous l’effet du TGF-β produit par les cellules phagocytaires (d’après [3]). |
La mort apoptotique, une mort sous silence
L’apoptose est le mécanisme physiologique de mort cellulaire le plus fréquemment rencontré dans l’organisme. Par exemple, 100 billions de polynucléaires neutrophiles meurent chaque jour par apoptose sans pour autant activer le système immunitaire. Le processus rapide d’élimination des cellules apoptotiques participe à l’inhibition de la réponse immunitaire contre ces cellules mourantes [11]. Un défaut de ce processus d’élimination rapide serait à l’origine de certaines maladies auto-immunes [4]. L’élimination des cellules apoptotiques est assurée par des cellules adjacentes ou les cellules phagocytaires professionnelles. Elle s’accompagne de la libération de cytokines immunosuppressives comme le TGF-β [5, 6]. Cela conduit à la création d’un environnement immunosuppresseur transitoire (Figure 2). Un autre mécanisme impliquant les lymphocytes T CD4 régulateurs peut aussi participer au contrôle des réponses auto-immunes. Les lymphocytes T régulateurs dépendent du TGF-β pour leur développement, leur survie et leur fonction [7, 8]. Le TGF-β libéré durant l’apoptose favorise la génération de lymphocytes T régulateurs, mais le signal délivré par cette cytokine n’est cependant pas suffisant. Un engagement simultané du récepteur à l’antigène, ou TCR (T cell receptor) est aussi nécessaire [3, 7] (Figure 2). Les deux conditions n’étant pas toujours réunies, cela expliquerait que des lymphocytes T régulateurs ne soient pas systématiquement associés à l’adminstration d’anticorps induisant l’apoptose.
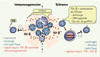 |
Figure 2. Mécanismes à l’origine des propriétés immunomodulatrices des cellules apoptotiques. Les cellules apoptotiques peuvent être à l’origine d’une immunosuppression et/ou d’une tolérance. L’immunosuppression est transitoire (le temps que les cellules apoptotiques soient éliminées), localisée (sur le site de l’élimination des cellules apoptotiques) et non spécifique (toutes les cellules immunitaires présentes à l’endroit où meurent les cellules peuvent être concernées). La tolérance est caractérisée par l’augmentation de lymphocytes T régulateurs. Elle est prolongée dans le temps (selon la durée de vie des lymphocytes T régulateurs générés), étendue à plusieurs sites (selon les capacités migratoires de ces lymphocytes) et spécifique. Selon le signal déclenchant l’activation du TCR, les lymphocytes T régulateurs générés auront une spécificité étendue (anticorps anti-CD3) ou restreinte contre les antigènes du soi (pathologie auto-immune) ou du greffon (transplantation). La balance entre tolérance et immunosuppression est donc déterminée par la stimulation du TCR. |
D’autres approches cliniques « exploitent » l’apoptose
Les données de la littérature suggèrent que les propriétés immunomodulatrices des cellules apoptotiques (Figure 2) interviennent dans d’autres approches thérapeutiques, comme la photothérapie extracorporelle ou la transfusion sanguine [9]. Dans ces deux cas, les produits administrés contiennent un nombre conséquent de leucocytes apoptotiques qui seraient à l’origine de l’effet immunomodulateur. Dans la photochimiothérapie extracorporelle, les propres globules blancs du patient, collectés par leucopherèse dans un circuit extracorporel, sont sensibilisés par un dérivé du psoralène, traités par radiations ultraviolettes, puis ces leucocytes apoptotiques sont réinjectés au patient. D’autre part, dans les produits sanguins labiles, les cellules apoptotiques correspondraient aux cellules sanguines contaminantes non désirées (leucocytes dans les concentrés de globules rouges). La transfusion au receveur de produits sanguins labiles du donneur a été utilisée en transplantation rénale pour tenter de réduire le rejet avant l’avènement des immunosuppresseurs chimiques. La déleucocytation pratiquée aujourd’hui pour prévenir les risques de contamination virale a diminué significativement le nombre de leucocytes apoptotiques présents dans les produits sanguins labiles, mais aussi l’efficacité immunomodulatrice de ces produits. Ces approches cliniques et les données expérimentales [1, 3, 9] renforcent l’idée d’une exploitation à des fins cliniques des propriétés immunomodulatrices de l’administration intraveineuse de cellules apoptotiques. Comment cette stratégie pourrait-elle trouver sa place dans l’arsenal thérapeutique ? Une étude clinique publiée récemment dans The Lancet rapporte les résultats de l’administration intramusculaire de cellules sanguines apoptotiques autologues chez plus de mille patients présentant des troubles cardiaques [10]. Malgré un bénéfice limité et un procédé d’induction d’apoptose discutable, cette étude confirme l’innocuité de l’administration de cellules apoptotiques qui pourrait rapidement trouver sa place comme produit de thérapie cellulaire.
Ce titre fait référence au film de Jacques Rouffio « Sept morts sur ordonnance » (1975) avec Michel Piccoli, Gérard Depardieu, Jane Birkin, Marina Vlady, Charles Vanel…
Basiliximab (Simulect, Novartis Pharmaceuticals) : anticorps chimérique dirigé contre contre la chaîne α du récepteur à l’IL-2 (CD25) obtenu par chimérisation d’un anticorps murin anti-CD25 avec les régions constantes de la chaîne lourde et la chaîne légère κ d’une IgG1 humaine. Daclizumab (Zenapax, Roche Pharmaceuticals) : anticorps monoclonal murin humanisé, comprenant les régions constantes des IgG1 humaines et la région complémentaire d’un anticorps monoclonal murin dirigé contre la chaîne α du récepteur à l’IL-2 (CD25).
Remerciements
Les auteurs remercient Wanjun Chen (Mucosal Immunity Unit, NIDCR, NIH, USA) pour son investissement dans ce travail et Béatrice Gaugler (Inserm UMR645) pour sa relecture.
Références
- Chatenoud L. Les anticorps monoclonaux anti-CD3. Une première étape vers un traitement du diabète insulino-dépendant d’origine auto-immune. Med Sci (Paris) 2006; 22 : 5–6. [Google Scholar]
- Chatenoud L. Une étape vers la restauration de la tolérance immunitaire au soi dans les maladies auto-immunes humaines. Med Sci (Paris) 2007; 23 : 167–71. [Google Scholar]
- Perruche S, Zhang P, Liu Y, et al. CD3-specific antibody-induced immune tolerance involves transforming growth factor-beta from phagocytes digesting apoptotic T cells. Nat Med 2008; 14 : 528–35. [Google Scholar]
- Munoz LE, van Bavel C, Franz S, et al. Apoptosis in the pathogenesis of systemic lupus erythematosus. Lupus 2008; 17 : 371–5. [Google Scholar]
- Chen W, Frank ME, Jin W, Wahl SM. TGF-beta released by apoptotic T cells contributes to an immunosuppressive milieu. Immunity 2001; 14 : 715–25. [Google Scholar]
- Fadok VA, Bratton DL, Konowal A, et al. Macrophages that have ingested apoptotic cells in vitro inhibit proinflammatory cytokine production through autocrine/paracrine mechanisms involving TGF-beta, PGE2, and PAF. J Clin Invest 1998; 101 : 890–8. [Google Scholar]
- Chen W, Jin W, Hardegen N, et al. Conversion of peripheral CD4+CD25- naive T cells to CD4+CD25+ regulatory T cells by TGF-beta induction of transcription factor Foxp3. J Exp Med 2003; 198 : 1875–86. [Google Scholar]
- Liu Y, Zhang P, Li J, et al. A critical function for TGF-beta signaling in the development of natural CD4+CD25+Foxp3+ regulatory T cells. Nat Immunol 2008; 9 : 632–40. [Google Scholar]
- Saas P, Bonnefoy F, Kleinclauss F, et al. Vers l’utilisation thérapeutique de l’administration intraveineuse de leucocytes apoptotiques du donneur en thérapie cellulaire ? Transfus Clin Biol 2008; 15 : 98–108. [Google Scholar]
- Torre-Amione G, Anker SD, Bourge RC, et al. Results of a non-specific immunomodulation therapy in chronic heart failure (ACCLAIM trial) : a placebo-controlled randomised trial. Lancet 2008; 371 : 228–36. [Google Scholar]
- Chimini G. Le récepteur des phosphatidylsérines, une arlésienne qui nous surprend toujours Med Sci (Paris) 2004; 20 : 501–2. [Google Scholar]
© 2009 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Mécanisme d’induction de tolérance par l’anticorps anti-CD3 L’induction de tolérance après traitement par l’anticorps anti-CD3 se décompose en 3 phases : (1) apoptose des lymphocytes T induite par l’anticorps anti-CD3 (immunosuppression transitoire) ; (2) élimination des lymphocytes apoptotiques par les cellules phagocytaires (macrophages et cellules dendritiques immatures) qui vont libérer du TGF-β ; (3) conversion ou expansion de lymphocytes T CD4 régulateurs sous l’effet du TGF-β produit par les cellules phagocytaires (d’après [3]). |
| Dans le texte | |
 |
Figure 2. Mécanismes à l’origine des propriétés immunomodulatrices des cellules apoptotiques. Les cellules apoptotiques peuvent être à l’origine d’une immunosuppression et/ou d’une tolérance. L’immunosuppression est transitoire (le temps que les cellules apoptotiques soient éliminées), localisée (sur le site de l’élimination des cellules apoptotiques) et non spécifique (toutes les cellules immunitaires présentes à l’endroit où meurent les cellules peuvent être concernées). La tolérance est caractérisée par l’augmentation de lymphocytes T régulateurs. Elle est prolongée dans le temps (selon la durée de vie des lymphocytes T régulateurs générés), étendue à plusieurs sites (selon les capacités migratoires de ces lymphocytes) et spécifique. Selon le signal déclenchant l’activation du TCR, les lymphocytes T régulateurs générés auront une spécificité étendue (anticorps anti-CD3) ou restreinte contre les antigènes du soi (pathologie auto-immune) ou du greffon (transplantation). La balance entre tolérance et immunosuppression est donc déterminée par la stimulation du TCR. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




