| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
|
|
|---|---|---|
| Page(s) | 258 - 262 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2026033 | |
| Published online | 20 mars 2026 | |
Quand la position des organites favorise la progression du cancer
When organelle positioning drives tumor progression
1
Tumor Biomechanics Lab, Inserm UMRS1109, Strasbourg, France
2
Université de Strasbourg, Strasbourg, France
3
Fédération de médecine translationnelle de Strasbourg (FMTS), Strasbourg, France
4
Équipe labellisée Ligue contre le cancer
5
CNRS, SNC5055, Strasbourg, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
**
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
***
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Le développement d’une tumeur s’accompagne de changements dans le positionnement des organites intracellulaires. Parmi ceux-ci, les lysosomes, longtemps considérés comme des compartiments uniquement dégradatifs, sont désormais reconnus comme des régulateurs clés du métabolisme, de la signalisation et de l’invasion tumorale. Nous discutons ici de la manière dont leur localisation intracellulaire influence leur fonction, leur signalisation et leur sécrétion. Dans le mélanome, leur distribution périphérique favorise l’agressivité des cellules tumorales et les métastases. L’existence de changements similaires dans d’autres cancers souligne le rôle du trafic lysosomal en tant que facteur de malignité et en tant que biomarqueur prometteur pour le diagnostic et le traitement.
Abstract
Long considered mere degradative compartments, lysosomes are now recognized as key regulators of metabolism, signaling, and tumor invasion. Here, we discuss how their intracellular localization controls their function, signaling, and secretion. In melanoma, the peripheral distribution of lysosomes promotes aggressiveness and metastasis. Similar changes exist in other types of cancer, highlighting the role of lysosomal trafficking as a factor in malignancy and as a promising biomarker for diagnosis and treatment.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Vignette (© Katerina Jerabkova-Roda).
Dans les tissus sains, les cellules se multiplient pour remplacer celles qui sont endommagées, mais ce processus doit être strictement contrôlé. Une division cellulaire incontrôlée peut entraîner le développement d’un cancer, par la formation d’une tumeur d’abord localisée, qui peut ensuite se disséminer dans d’autres régions du corps par le sang ou la lymphe, donnant naissance à des métastases. Les facteurs intrinsèques, liés à la division des cellules souches, ne représentent que 10 à 30 % du risque de développer un cancer au cours de la vie [1]. Les risques de cancer sont donc principalement liés à des facteurs extrinsèques [2]. Par exemple, la pollution de l’air et le tabac sont associés au cancer du poumon ; l’alcool peut déclencher des cancers du foie, tandis que l’exposition aux rayonnements UV provoque l’apparition de mélanomes, un cancer de la peau agressif qui prend naissance dans des cellules appelées mélanocytes [3].
Apparition et progression du mélanome
L’émergence et la progression du mélanome résultent d’une succession d’événements biologiques complexes, et son dépistage précoce constitue un facteur essentiel pour le pronostic et la survie des patients. Tout d’abord, les mélanocytes se transforment et se développent dans l’épiderme pendant la phase de croissance radiale (RGP, radial growth phase), formant une lésion à faible potentiel métastatique. Les modifications de leur programme de transcription conduisent à l’expression d’enzymes capables de dégrader la matrice extracellulaire et à une invasion du derme pendant la phase de croissance verticale (VGP, vertical growth phase), suivie d’une dissémination du cancer par les voies vasculaires et lymphatiques, évoluant vers des stades métastatiques [4]. Cela suggère que la formation de métastases issues d’un mélanome nécessite des programmes d’invasion spécifiques permettant une sécrétion efficace et ciblée des enzymes dégradant la matrice extracellulaire (MEC). Ces programmes transcriptionnels pourraient impliquer les facteurs de la famille MITF/TFE (microphthalmiaassociated transcription factor/transcription factor E), fréquemment surexprimés dans le mélanome [5], et impliqués dans la régulation de diverses fonctions cataboliques des lysosomes, notamment leur exocytose [6, 7].
Le mélanome pose un problème majeur de santé publique, car il évolue rapidement vers la formation de métastases : traité précocement, le taux de survie à cinq ans dépasse 95 %, mais, s’il se propage, ce taux chute à moins de 25 %. Le dépistage précoce est donc essentiel [8, 9]. Cependant, à ce jour, il n’existe pas de biomarqueur moléculaire spécifique ; le diagnostic repose essentiellement sur la forme et la couleur des lésions, mais il est désormais facilité par des méthodes ayant recours à l’intelligence artificielle [10].
Les organites intracellulaires dans la progression tumorale : l’importance grandissante des lysosomes
Les cellules eucaryotes, que l’on retrouve chez les végétaux, les animaux ainsi que chez l’être humain, contiennent des organites qui assurent une compartimentation fonctionnelle de leurs activités physiologiques. Ces organites constituent des microenvironnements biochimiques distincts, dédiés à des fonctions spécifiques telles que le stockage du matériel génétique au sein du noyau, la production et la mise en réserve d’énergie dans les mitochondries, la synthèse des protéines au niveau du réticulum endoplasmique, leur modification post-traductionnelle dans l’appareil de Golgi, ainsi que leur dégradation en éléments nutritifs dans les lysosomes et les autophagosomes. La forme et la position des organites sont minutieusement contrôlées dans la cellule, ce qui est crucial pour son équilibre et son bon fonctionnement (Figure 1A). Au cours du développement tumoral, certains organites changent de forme et de localisation intracellulaire. Ainsi, dans de nombreux cancers, les mitochondries, deviennent petites et fragmentées, ce qui favorise la croissance et la dissémination tumorale [11]; ainsi, leur morphologie peut ainsi être utilisée pour distinguer les tissus sains des tissus cancéreux [12]. Les lysosomes, autrefois considérés uniquement comme des compartiments dédiés au recyclage intracellulaire, sont désormais reconnus comme des centres métaboliques majeurs, impliqués dans la régulation du trafic membranaire et l’intégration des signaux provenant de l’environnement cellulaire [13, 14]. Plusieurs études récentes indiquent que les lysosomes jouent un nouveau rôle en tant que régulateurs de l’invasion cellulaire, en permettant aux cellules de détecter leur microenvironnement et d’activer des réponses adaptées, notamment par exocytose de leur contenu [7, 15]. Par exemple, la sécrétion de la cathepsine B, une enzyme lysosomale, favorise l’invasion et la formation de métastases par des cellules cancéreuses [16]. En outre, la sécrétion lysosomale contribue à la réparation des dommages causés à la membrane plasmique lors de la migration cellulaire et améliore la survie des cellules soumises à un stress mécanique [17].
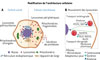 |
Figure 1 Modifications de l’architecture intracellulaires, et ses organites, liées au cancer. A. architecture d’une cellule saine (ou cancéreuse). B. Mécanisme de déplacement des lysosomes le long des microtubules. Les microtubules sont représentés en vert, les lysosomes en rouge et le noyau en violet. |
Comment se déplacent les lysosomes et pourquoi est-ce important ?
Les lysosomes se déplacent au sein de la cellule le long de rails microscopiques qui constituent le cytosquelette de la cellule, en particulier les microtubules, grâce à des protéines motrices spécialisées : la dynéine, qui assure le transport dirigé vers la région périnucléaire, et la kinésine, responsable du déplacement vers la périphérie cellulaire, à proximité de la membrane plasmique (Figure 1B). Des protéines comme Rab7 (Ras gene from rat brain) et Arl8b (ARF-like GTPase 8B) participent au guidage et à la régulation de ces mouvements en recrutant des effecteurs additionnels - FYCO1 (FYVE and coiled-coil [CC] domain containing 1), SKIP (sphingosine kinase interacting protein), RILP (Rab interacting lysosomal protein), RUFY3 (RUN and FYVE domain–containing 3), et BicD2 (Bicaudal D homolog 2) - qui interagissent avec des moteurs moléculaires (la kinésine et la dynéine) pour assurer le transport des lysosomes [18–22]. Ces complexes garantissent un positionnement dynamique des lysosomes en réponse aux signaux et aux conditions environnementales, tels que la quantité de nutriments disponibles. Il est important de noter que l’activité des lysosomes est régulée par leur localisation intracellulaire [23, 24]. Les lysosomes situés en périphérie cellulaire présentent une propension accrue à l’exocytose, processus par lequel leur membrane fusionne avec la membrane plasmique pour libérer leur contenu dans le milieu extracellulaire. Ils participent ainsi notamment, à la régulation de la signalisation par des facteurs de croissance [25]. À l’inverse, les lysosomes périnucléaires se caractérisent par une acidité plus élevée et une activité dégradative plus importante [24].
Rôle des lysosomes dans le métabolisme et le cancer
Les lysosomes modulent le métabolisme cellulaire et jouent un rôle déterminant dans la régulation du destin cellulaire en orientant celleci vers la croissance ou vers le recyclage de ses constituants selon la disponibilité en nutriments. Lorsque les lysosomes sont transportés vers la membrane plasmique, ils participent activement, entre autres, à l’activation de mTORC1 (mammalian target of rapamycin complex 1), une protéine clé impliquée dans la croissance cellulaire. En situation de pénurie de nutriments, ils se rapprochent du noyau, ce qui entraîne l’inactivation de mTORC1 et favorisent un mécanisme de recyclage appelé autophagie [26]. L’établissement de contacts entre les lysosomes et d’autres organites intracellulaires, tels que les mitochondries et le réticulum endoplasmique, permet des échanges métaboliques essentiels, notamment d’acides aminés, de lipides, d’ions inorganiques, d’acides gras et de nucléotides, contribuant ainsi au maintien de l’homéostasie cellulaire [14].
Repositionnement des lysosomes dans le cancer
Dans le mélanome, la localisation périphérique des lysosomes est caractéristique des tumeurs agressives. Elle corrèle significativement avec la progression de la tumeur. En effet, l’analyse de lignées cellulaires dérivées de patients ainsi que celle de biopsies tumorales a montré une corrélation entre la progression du cancer et la localisation périphérique des lysosomes, celle-ci augmentant avec le stade du cancer, depuis la phase de croissance radiale jusqu’au mélanome métastatique (Figure 2) [7]. Ainsi, les cellules cancéreuses les plus métastatiques présentent les lysosomes les plus périphériques. Cette disposition spatiale est associée à des programmes génétiques qui favorisent la progression du cancer et la migration des cellules. Par ailleurs, les moteurs de kinésine KIF1B et KIF5B (kinesin family members 1B et 5B) sont surexprimés dans les cellules cancéreuses, ce qui favorise le mouvement des lysosomes vers la membrane plasmique [7]. Ces données confortent de précédentes observations montrant une localisation préférentiellement périphérique des lysosomes dans d’autres types de cancer tels que le cancer du sein [27] et le cancer de la vessie [28].
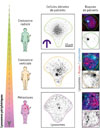 |
Figure 2 Distribution intracellulaire des lysosomes dans des cellules dérivées de patients cultivées in vitro, ou des cellules de biopsies. Les cellules de mélanome agressif présentent des lysosomes dispersés dans la cellule et périphériques, alors que les cellules de naevus bénins présentent des lysosomes regroupés à proximité du noyau. Échantillons provenant de biopsies de tumeurs de patients. Les lignes pointillées représentent le contour d’une cellule dans laquelle les lysosomes sont visibles comme des points noirs ou colorés. |
Les lysosomes dans l’essaimage du mélanome
Nos études démontrent qu’un positionnement plus périphérique des lysosomes leur permet de fusionner avec la membrane plasmique et de libérer des protéases, notamment des cathepsines et des métalloprotéases, qui modifient le microenvironnement cellulaire [7]. Ces enzymes dégradent et remodèlent la matrice extracellulaire, facilitant ainsi la migration des cellules cancéreuses et l’invasion de nouveaux tissus [7, 27]. Pour démontrer l’importance du positionnement des lysosomes dans les propriétés invasives des cellules tumorales, nous avons généré un outil génétique fondé sur l’hétérodimérisation rapide et forte des domaines FKBP (FK506-binding protein) et FRB (FKBP12-rapamycin binding domain) par le composé rapalog1 (inactivation du complexe mTOR) [29], permettant de regrouper tous les lysosomes au centre de la cellule. Nous avons fait exprimer, de manière stable, par des cellules, le domaine FKBP fusionné à LAMP1 (lysosomal-associated membrane protein 1) et le domaine FRB fusionné à l’adaptateur de dynéine BicD2. Le traitement des cellules par le rapalog induit la liaison de FKBP à FRB, ce qui entraîne le recrutement de la dynéine au niveau des compartiments marqués par LAMP1. Ce processus induit le déplacement des lysosomes vers l’extrémité – ancrée au MTOC (microtubule organization center) – des microtubules, conduisant ainsi à un regroupement périnucléaire des organites contenant LAMP1 autour du centre d’organisation des microtubules, le centrosome [7]. À l’aide de cet outil, nous avons observé que lorsque l’on force les lysosomes à rester au centre de la cellule, la dégradation de la matrice extracellulaire autour des cellules et leur capacité de dissémination sont réduites. En effet, des expériences in vivo, utilisant des modèles de souris et de poisson zèbre ont montré que forcer la localisation périnucléaire des lysosomes réduit la dissémination des tumeurs et l’invasion cellulaire [7]. Les cellules dont les lysosomes sont regroupés près du noyau présentent un potentiel métastatique limité, ce qui suggère que le contrôle spatial des lysosomes constitue un commutateur fonctionnel dans la progression du mélanome.
Potentiel diagnostique et pronostique
L’analyse de prélèvements de patients a montré que la localisation des lysosomes dans les biopsies tumorales est directement corrélée au stade du mélanome [7]. Cette caractéristique pourrait servir de biomarqueur pour distinguer les tumeurs bénignes des formes avancées et ainsi guider une intervention précoce, contribuant à la mise en place de stratégies de traitement optimisées, pour permettre, in fine, d’améliorer le suivi et la prise en charge des patients. L’intelligence artificielle offre aujourd’hui de nouveaux outils pour analyser la répartition et la morphologie des organites, facilitant le diagnostic des cancers. Une étude récente a, par exemple, développé un algorithme permettant de différencier les cellules saines des cellules tumorales en se fondant sur la distribution spatiale de leurs organites [12]. Cette première étape pourrait permettre la future classification phénotypique d’échantillons de tissus fondée sur l’architecture subcellulaire, ce qui conduirait, à terme, à améliorer le diagnostic du cancer.
Conclusion
Les organites sont des structures dynamiques dont la position s’adapte en fonction des besoins et des signaux reçus par la cellule. La position intracellulaire des lysosomes peut déterminer non seulement l’agressivité et le potentiel invasif du mélanome, mais aussi la capacité de la cellule cancéreuse à croître et à se disséminer. Une meilleure compréhension de la régulation de la position intracellulaire des lysosomes, ainsi que d’autres organites, pourrait ouvrir la voie à de nouveaux outils diagnostiques et traitements du mélanome métastatique.
Remerciements
Nous remercions l’ensemble des membres du laboratoire, ainsi que nos collaborateurs, en particulier K. Schauer, P. Rondé, C. Carapito, D. Lipsker. Nous remercions également l’ensemble du consortium Nanotumor qui a contribué aux travaux décrits dans cette revue. Nous sommes très reconnaissants à nos nombreux financeurs de nous avoir permis d’entreprendre ces travaux.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
Références
- Wu S, Powers S, Zhu W, et al. Substantial contribution of extrinsic risk factors to cancer development. Nature 2016 ; 529 : 43–7. [Google Scholar]
- Wu S, Zhu W, Thompson P, et al. Evaluating intrinsic and non-intrinsic cancer risk factors. Nat Commun 2018 ; 9 : 3490. [Google Scholar]
- Saqib U, Ricks KE, Obukhov AG, et al. Exposomes and genes: The duo influencing cancer initiation and progression. Oncotarget 2025 ; 16 : 133–5. [Google Scholar]
- Braeuer RR, Zigler M, Villares GJ, et al. Transcriptional control of melanoma metastasis: the importance of the tumor microenvironment. Semin Cancer Biol 2011 ; 21 : 83–8. [Google Scholar]
- Zoncu R, Perera RM. Emerging roles of the MiT/TFE factors in cancer. Trends Cancer 2023 ; 9 : 817–27. [Google Scholar]
- Medina DL, Fraldi A, Bouche V, et al. Transcriptional activation of lysosomal exocytosis promotes cellular clearance. Dev Cell 2011 ; 21 : 421–30. [CrossRef] [PubMed] [Google Scholar]
- Jerabkova-Roda K, Peralta M, Huang KJ, et al. Peripheral positioning of lysosomes supports melanoma aggressiveness. Nat Commun 2025 ; 16 : 3375. [Google Scholar]
- Miller AJ, Mihm MC. Melanoma. New Engl J Med 2006 ; 355 : 51–65. [Google Scholar]
- Enninga EAL, Moser JC, Weaver AL, et al. Survival of cutaneous melanoma based on sex, age, and stage in the United States, 1992–2011. Cancer Med 2017 ; 6 : 2203–12. [Google Scholar]
- Moura N, Veras R, Aires K, et al. ABCD rule and pre-trained CNNs for melanoma diagnosis. Multimed Tools Appl 2019 ; 78 : 6869–88. [Google Scholar]
- Boulton DP, Caino MC. Mitochondrial fission and fusion in tumor progression to metastasis. Front Cell Dev Biol 2022 ; 10 : 849962. [Google Scholar]
- Wang L, Goldwag J, Bouyea M, et al. Spatial topology of organelle is a new breast cancer cell classifier. iScience 2023 ; 26 : 107229. [Google Scholar]
- Ballabio A, Bonifacino JS. Lysosomes as dynamic regulators of cell and organismal homeostasis. Nat Rev Mol Cell Biol 2020 ; 21 : 101–18. [CrossRef] [PubMed] [Google Scholar]
- Jerabkova-Roda K, Marwaha R, Das T, et al. Organelle morphology and positioning orchestrate physiological and disease-associated processes. Curr Opin Cell Biol 2024 ; 86 : 102293. [Google Scholar]
- Ballabio A, Bonifacino JS. Lysosomes as dynamic regulators of cell and organismal homeostasis. Nat Rev Mol Cell Biol 2020 ; 21 : 101–18. [CrossRef] [PubMed] [Google Scholar]
- Bian B, Mongrain S, Cagnol S, et al. Cathepsin B promotes colorectal tumorigenesis, cell invasion, and metastasis. Mol Carcinog 2016 ; 55 : 671–87. [Google Scholar]
- Corrotte M, Castro-Gomes T. Chapter One - Lysosomes and plasma membrane repair. Curr Top Membr 2019 ; 84 : 1–16. [Google Scholar]
- Khatter D, Sindhwani A, Sharma M. Arf-like GTPase Arl8: Moving from the periphery to the center of lysosomal biology. Cell Logist 2015 ; 5 : e1086501. [Google Scholar]
- Rosa-Ferreira C, Munro S. Arl8 and SKIP Act together to link lysosomes to kinesin-1. Dev Cell 2011 ; 21 : 1171–8. [Google Scholar]
- Kumar G, Chawla P, Dhiman N, et al. RUFY3 links Arl8b and JIP4-Dynein complex to regulate lysosome size and positioning. Nat Commun 2022 ; 13 : 1540. [Google Scholar]
- Qi C, Zou L, Wang S, et al. Vps34 Inhibits hepatocellular carcinoma invasion by regulating endosome-lysosome trafficking via Rab7-RILP and Rab11. Cancer Res Treat 2022 ; 54 : 182–98. [Google Scholar]
- Pu J, Guardia CM, Keren-Kaplan T, et al. Mechanisms and functions of lysosome positioning. J Cell Sci 2016 ; 129 : 4329–39. [Google Scholar]
- Korolchuk VI, Saiki S, Lichtenberg M, et al. Lysosomal positioning coordinates cellular nutrient responses. Nat Cell Biol 2011 ; 13 : 453–60. [Google Scholar]
- Johnson DE, Ostrowski P, Jaumouillé V, et al. The position of lysosomes within the cell determines their luminal pH. J Cell Biol 2016 ; 212 : 677–92. [CrossRef] [PubMed] [Google Scholar]
- Jia R, Bonifacino JS. Lysosome positioning influences mTORC2 and AKT signaling. Molecular Cell 2019 ; 75 : 26–38.e3. [Google Scholar]
- Poüs C, Codogno P. Lysosome positioning coordinates mTORC1 activity and autophagy. Nat Cell Biol 2011 ; 13 : 342–4. [Google Scholar]
- Wu P-H, Onodera Y, Giaccia AJ, et al. Lysosomal trafficking mediated by Arl8b and BORC promotes invasion of cancer cells that survive radiation. Commun Biol 2020 ; 3 : 620. [Google Scholar]
- Mathur P, De Barros Santos C, Lachuer H, et al. Transcription factor EB regulates phosphatidylinositol-3-phosphate levels that control lysosome positioning in the bladder cancer model. Commun Biol 2023 ; 6 : 1–14. [CrossRef] [PubMed] [Google Scholar]
- Kapitein LC, Schlager MA, Zwan WA van der, et al. Probing intracellular motor protein activity using an inducible cargo trafficking assay. Biophys J 2010 ; 99 : 2143–52. [Google Scholar]
Les rapalogues sont des analogues synthétiques de la rapamycine, également connue sous le nom de sirolimus.
Liste des figures
 |
Figure 1 Modifications de l’architecture intracellulaires, et ses organites, liées au cancer. A. architecture d’une cellule saine (ou cancéreuse). B. Mécanisme de déplacement des lysosomes le long des microtubules. Les microtubules sont représentés en vert, les lysosomes en rouge et le noyau en violet. |
| Dans le texte | |
 |
Figure 2 Distribution intracellulaire des lysosomes dans des cellules dérivées de patients cultivées in vitro, ou des cellules de biopsies. Les cellules de mélanome agressif présentent des lysosomes dispersés dans la cellule et périphériques, alors que les cellules de naevus bénins présentent des lysosomes regroupés à proximité du noyau. Échantillons provenant de biopsies de tumeurs de patients. Les lignes pointillées représentent le contour d’une cellule dans laquelle les lysosomes sont visibles comme des points noirs ou colorés. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




