| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
Nos jeunes pousses ont du talent !
|
|
|---|---|---|
| Page(s) | 949 - 951 | |
| Section | Partenariat médecine/sciences - Écoles doctorales - Masters | |
| DOI | https://doi.org/10.1051/medsci/2025219 | |
| Published online | 12 December 2025 | |
Dérivé de phage couplé à un éditeur de base : un outil de modification génétique du microbiote
Chimeric phage associated with a base editor: a tool for microbiota genetic modification
1
Master 2 d’Infectiologie, Immunologie, Vaccinologie et Biomédicaments, Université de Tours, France
2
Équipe « Bactéries et risques materno-foetal », UMR ISP 1282, Université de Tours, INRAE, Faculté de Médecine, Tours, France
a
This email address is being protected from spambots. You need JavaScript enabled to view it.
b
This email address is being protected from spambots. You need JavaScript enabled to view it.
c
This email address is being protected from spambots. You need JavaScript enabled to view it.
d
This email address is being protected from spambots. You need JavaScript enabled to view it.
Le microbiote intestinal : impact sur la santé humaine
L’ensemble des microorganismes du tube digestif, appelé microbiote intestinal, joue un rôle essentiel dans de nombreuses fonctions telles que la digestion des aliments [1] ou la maturation du système immunitaire [2]. Depuis quelques années, le rôle de la dysbiose (altération du microbiote) dans des pathologies variées, telles que les maladies inflammatoires chroniques ou le cancer, est reconnu [3]. Il apparaît alors crucial de disposer d’outils de manipulation du microbiote afin de dégager de nouveaux axes thérapeutiques.
Les techniques actuelles de modification du microbiote in vivo reposent sur trois approches principales. La première est l’utilisation des prébiotiques, des substrats non digestibles (comme les fibres), qui favorisent le développement des bactéries bénéfiques de la flore intestinale. La deuxième consiste à administrer des probiotiques, qui sont des microorganismes vivants, capables de moduler le microbiote de manière bénéfique pour l’hôte. Enfin, il est également possible de modifier le microbiote de façon plus globale en changeant de régime alimentaire ou en transplantant du microbiote fécal. Cependant, pour que le microbiote nouvellement implanté perdure, il faut maintenir de façon durable un régime alimentaire riche en substrats. Ainsi, nous manquons d’outils pour manipuler le microbiote de façon ciblée et durable dans un environnement complexe comme le tube digestif.
L’article « In situ targeted base editing of bacteria in the mouse gut » publiée par Brödel et al. en 2024 dans Nature avait pour objectif de développer une stratégie permettant de modifier génétiquement, de façon stable et durable, une population bactérienne du microbiote intestinal [4]. Pour cela, les chercheurs ont choisi de délivrer un éditeur de base, soit une machinerie d’édition génique, via un vecteur : le génome d’un phage, un virus capable d’infecter une bactérie.
Qu’est-ce qu’un éditeur de base ?
L’édition de base (base editing) est une technique qui permet d’introduire des mutations ponctuelles dans l’ADN ou l’ARN cellulaire sans créer de cassures de l’ADN double brin [5]. Ce système est dérivé du système d’édition du génome le plus connu : le complexe CRISPR/Cas (clustered regularly interspaced short palindromic repeats/CRISPR-associated proteins). L’éditeur de base utilisé ici est composé d’un ARN guide permettant de diriger la Cas9 vers une séquence d’intérêt. La Cas 9, couplé à une désaminase, va alors se fixer à la séquence et ouvrir une boucle d’ADN simple brin permettant à la désaminase de remplacer un nucléotide par un autre. Deux types de désaminases ont été utilisés par les auteurs : une cytosine base editor (CBE) qui remplace une paire de guanine-cytosine par une paire thymine-adénine et une adénosine base editor (ABE) faisant l’inverse [4].
Développement d’un système de ciblage spécifique de bactéries du microbiote intestinal
Les auteurs ont d’abord dû élaborer un système permettant de délivrer l’ADN codant l’éditeur de base dans des espèces bactériennes spécifiques faisant partie du microbiote intestinal humain, ici Escherichia coli. Ils ont donc utilisé un bactériophage génétiquement modifié, en raison de leur propriété naturelle à injecter leur génome dans une bactérie et à en détourner la machinerie cellulaire [6].
Leur choix s’est porté sur le phage λ, qui utilise principalement la porine LamB comme récepteur pour se lier et injecter son ADN dans les bactéries. Contrairement à d’autres phages, comme M13 qui utilise le pilus F comme récepteur, et dont l’expression est absente chez certaines bactéries Gram-négatives de l’intestin [7], le phage λ peut cibler une plus large population bactérienne.
De plus, il est capable d’entrer en lysogénie, phase durant laquelle le virus intègre son ADN dans le génome de la bactérie hôte sans la détruire [8]. Cela permet non seulement le maintien stable du transgène dans le génome bactérien, mais aussi la survie de la bactérie, condition indispensable pour garantir une modification durable de la population du microbiote. Lors de cette phase, le virus reste inactif (sous la forme de prophage), ne produisant alors pas de nouveaux virions jusqu’à une activation ultérieure.
Limitation des risques de propagation génétique : création d’un vecteur d’ADN non réplicatif
Afin d’éviter la transmission incontrôlée de l’ADN introduit, les auteurs ont conçu un vecteur réplicatif inductible, le payload. Ce vecteur contient un gène, par défaut inactif, codant une primase nécessaire à sa réplication. L’activation de la primase peut être induite, par exemple par ajout de DAPG (2,4-diacétylphloroglucinol, molécule inductrice utilisée pour induire l’expression du gène), déclenchant ainsi la réplication du vecteur uniquement lorsque cela est souhaité. Cela signifie que, même si l’ADN est introduit avec succès dans une cellule bactérienne, il ne pourra pas se transmettre à d’autres bactéries de façon incontrôlée.
Optimisation du phage pour une efficacité maximale de l’injection d’ADN
Le défi majeur était de modifier l’ensemble d’une population bactérienne du microbiote. Initialement, le phage λ a été choisi pour sa capacité naturelle à infecter un spectre relativement large de souches bactériennes via le récepteur LamB. Cependant, certaines souches d’E. coli n’expriment pas ce dernier. Pour élargir le spectre d’action du phage, les auteurs ont modifié ses protéines d’attachement, gpJ et STF (side tail fibers), afin qu’elles se lient à OmpC, une porine davantage exprimée.
Afin d’éviter une compétition de liaison entre GPJ et STF pour ce même récepteur, les STF ont été fusionnées avec des segments protéiques dérivés du phage P2. Cette chimère permet aux STF de reconnaître le LPS bactérien (lipopolysaccharide, composant de la membrane externe des bactéries Gram-négatives) plutôt que OmpC, évitant ainsi toute compétition avec gpJ et améliorant l’efficacité de la reconnaissance des récepteurs bactériens (Figure 1). Cette chimère a en outre permis d’augmenter l’efficacité de l’injection d’ADN dans les bactéries cibles, atteignant jusqu’à 90 %.
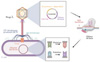 |
Figure 1 Ingénierie d’un phage λ modifié combiné avec un cosmide non réplicatif codant pour un éditeur de base et une origine de réplication dépendante de la primase, empêchant ainsi sa dissémination. L’éditeur de base (ici ABE) intégré permet des conversions nucléotidiques précises (T→C, A→G), permettant des modifications ciblées du génome bactérien. Le phage λ est modifié avec des chimères STF-P2 reconnaissant le lipopolysaccharide (LPS) et des chimères gpJ ciblant spécifiquement la protéine OmpC de la membrane bactérienne. |
Cette approche montre que même si le choix du phage λ était motivé par son spectre naturellement large, l’ingénierie des protéines d’attachement et le développement de telles chimères restent nécessaires pour augmenter l’efficacité des outils de modification génétique dans des environnements complexes comme l’intestin. Bien que d’autres phages auraient pu être modifiés de manière similaire, λ offre l’avantage supplémentaire de pouvoir entrer en lysogénie, permettant un maintien stable du transgène dans le génome bactérien.
Optimisation des cosmides pour l’édition génique in vivo
Les auteurs ont ensuite combiné la chimère obtenue avec un plasmide, appelé cosmide, contenant des séquences λ du phage (cos) nécessaire à l’empaquetage de l’ADN du phage dans le virion [9], l’éditeur de base, l’origine de réplication primase-dépendante, ainsi qu’une molécule fluorescente, la sfGFP. Le cosmide a été intégré dans une souche E. coli MG1655 porteuse d’un plasmide contenant une primase inductible. L’ajout de DAPG induit l’expression de la primase permettant la réplication du cosmide.
La stabilité du cosmide a ensuite été évaluée par cytométrie en flux en suivant le signal sfGFP. Au cours des premières heures et en l’absence de DAPG, une forte fluorescence est détectée, témoignant d’une efficacité de la délivrance du cosmide. Cependant, le signal diminue progressivement, indiquant que sans réplication, le cosmide est progressivement perdu par les bactéries, mettant en évidence son instabilité en l’absence de primase.
Le cosmide généré a été utilisé pour effectuer des modifications précises d’une souche E. coli, non pathogène et présente dans l’intestin murin, afin d’évaluer l’efficacité de l’édition génique in vivo. L’édition portait sur le gène de la β-lactamase (bla), impliqué dans la résistance aux antibiotiques. L’ingestion d’une dose de particules phagiques (4 × 1010 particules) a permis d’obtenir un taux d’édition de 93 % des bactéries cibles, maintenu pendant 6 jours, sans altérer leur croissance ni leur capacité de survie (fitness). Ils ont ensuite administré à d’autres souris BALB/C une dose intermédiaire (1 × 1010 particules) pendant trois jours consécutifs, afin d’étudier l’impact sur l’abondance relative de la population modifiée. Au bout de 42 jours, cette population modifiée était toujours présente au niveau de l’intestin, traduisant la stabilité des modifications géniques.
Par la suite, les auteurs ont essayé d’appliquer l’édition génique à des souches pathogènes E. coli et K. pneumoniae in vitro, en ciblant des gènes de la virulence ou de la résistance aux antibiotiques. Ils ont ainsi pu obtenir des modifications génétiques permettant l’inactivation de gènes de résistance et de virulence sans augmenter le taux de mutation global.
Après les succès obtenus lors des essais in vitro, des tests in vivo ont été menés afin d’évaluer l’édition de base d’une souche pathogène dans l’intestin de souris. Pour cela, des souris BALB/c traitées à la streptomycine ont été colonisées avec une souche E. coli TN03, associée à des infections extra-intestinales résistantes à la streptomycine. Les souris ont été gavées 5 jours après la colonisation, avec trois doses différentes de cosmides. Ces derniers codent pour un ABE ciblant le gène csgA, sous-unité majeure de la protéine Curli. Ce facteur d’adhésion des entérobactéries, associé à de nombreuses maladies humaines telles que la maladie d’Alzheimer [10], est une cible de choix car il est non essentiel à la croissance bactérienne et son inactivation conduit à un phénotype facilement détectable. Le traitement a induit une édition efficace du gène csgA, atteignant une médiane de 71 % des cellules cibles éditées 24 heures après l’administration de la dose la plus élevée (1 × 1011 particules). En analysant l’impact du traitement sur la composition globale du microbiote intestinal, les auteurs ont constaté des variations du microbiome interindividuelles et temporelles après l’administration de streptomycine, témoignant à la fois de la diversité naturelle de leur microbiote et de la variabilité individuelle de la réponse au traitement. En outre, les fluctuations du microbiome total observées après l’administration de l’éditeur de base ne dépassent pas celles induites par la streptomycine, suggérant que ce dernier n’a pas d’impact majeur sur la composition du microbiome.
Brödel et al. ont ainsi développé une technique novatrice pour manipuler le microbiote intestinal via des vecteurs bactériophages modifiés délivrant des éditeurs de base [4]. Les chercheurs ont démontré la possibilité de modifier durablement et précisément le génome de bactéries du microbiote intestinal, in vitro et in vivo, via un modèle murin. Les résultats montrent, dans l’intestin de souris, un taux d’édition élevé de bactéries commensales ou pathogènes. Ces modifications étaient stables dans le temps et sans impact sur la composition globale du microbiote. Cette méthode offre des perspectives thérapeutiques pour lutter contre les maladies liées aux dysbioses ou aux bactéries multi-résistantes. Toutefois, des analyses complémentaires sont à effectuer afin d’évaluer l’impact écologique et la sécurité de cet outil pour prévenir tout risque de transfert de mutations génétiques de façon non contrôlée.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Gomaa EZ. Human gut microbiota/microbiome in health and diseases: a review. Antonie van Leeuwenhoek 2020 ; 113 : 2019–2040. [Google Scholar]
- Donald K, Finlay BB. Early-life interactions between the microbiota and immune system: impact on immune system development and atopic disease. Nat Rev Immunol 2023 ; 23 : 735–748. [Google Scholar]
- Gebrayel P, Nicco C, Al Khodor S, et al. Microbiota medicine: towards clinical revolution. J Transl Med 2022 ; 20 : 111. [CrossRef] [PubMed] [Google Scholar]
- Brödel AK, Charpenay LH, Galtier M, et al. In situ targeted base editing of bacteria in the mouse gut. Nature 2024 ; 632 : 877–884. [Google Scholar]
- Rees HA, Liu DR. Base editing: precision chemistry on the genome and transcriptome of living cells. Nat Rev Genet 2018 ; 19 : 770–788. [CrossRef] [PubMed] [Google Scholar]
- Hatfull GF, Hendrix RW. Bacteriophages and their genomes. Current Opinion in Virology 2011 ; 1 : 298–303. [Google Scholar]
- Goldlust K, Ducret A, Halte M, et al. The F pilus serves as a conduit for the DNA during conjugation between physically distant bacteria. Proc. Natl. Acad. Sci. U.S.A. 2023 ; 120 : e2310842120. [Google Scholar]
- Geng Y, Nguyen TVP, Homaee E, et al. Using bacterial population dynamics to count phages and their lysogens. Nat Commun 2024 ; 15 : 7814. [Google Scholar]
- Cronan JE. Cosmid-Based System for Transient Expression and Absolute Off-to-On Transcriptional Control of Escherichia coli Genes. J Bacteriol 2003 ; 185 : 6522–6529. [Google Scholar]
- Barnhart MM, Chapman MR. Curli Biogenesis and Function. Annu. Rev. Microbiol. 2006 ; 60 : 131–147. [Google Scholar]
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Ingénierie d’un phage λ modifié combiné avec un cosmide non réplicatif codant pour un éditeur de base et une origine de réplication dépendante de la primase, empêchant ainsi sa dissémination. L’éditeur de base (ici ABE) intégré permet des conversions nucléotidiques précises (T→C, A→G), permettant des modifications ciblées du génome bactérien. Le phage λ est modifié avec des chimères STF-P2 reconnaissant le lipopolysaccharide (LPS) et des chimères gpJ ciblant spécifiquement la protéine OmpC de la membrane bactérienne. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




