| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
|
|
|---|---|---|
| Page(s) | 837 - 839 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2025210 | |
| Published online | 12 décembre 2025 | |
Exposition aux PFAS pendant la grossesse
Conséquences sur la santé et le fonctionnement du placenta
PFAS exposure during pregnancy: implications for placental health and functioning
1
Université Grenoble Alpes, Inserm U1209, CNRS UMR5309, Épidémiologie environnementale appliquée à la reproduction et la santé respiratoire, Institut pour l’avancée des biosciences, Grenoble, France
2
Commissariat à l’énergie atomique et aux énergies alternatives, CNRS, Inserm U1292, Université Grenoble Alpes, Grenoble, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Contributions équivalentes
Le placenta assure les échanges de nutriments et de gaz entre la mère et le fœtus, ainsi que les fonctions endocriniennes et métaboliques nécessaires au bon déroulement de la grossesse. Le poids du placenta ainsi que le rapport entre celui-ci et le poids fœtal sont couramment utilisés comme indicateurs de la santé et de l’efficacité du placenta. Bien que moins fréquemment exploitée dans les études épidémiologiques en raison de contraintes techniques, sa structure microscopique constitue également un indicateur essentiel : l’analyse histologique du placenta fournit en effet des informations précieuses sur la perfusion vasculaire, les échanges avec le fœtus, ainsi que sur son degré de « vieillissement ». Une altération du poids du placenta ou de ses caractéristiques histologiques est associée à des complications majeures de la grossesse, telles que la prééclampsie1, le retard de croissance intra-utérin ou la naissance prématurée. Ces éléments justifient l’intérêt porté à ces marqueurs dans l’étude de l’impact des contaminants environnementaux sur l’issue de la grossesse et la santé périnatale.
Parmi les facteurs environnementaux susceptibles d’affecter le placenta figurent les substances perfluoroalkylées et polyfluoroalkylées (PFAS), aussi connues sous le nom de « polluants éternels ». Ces composés synthétiques sont largement utilisés dans de nombreux secteurs industriels, et sont présents dans une grande variété de produits de consommation en raison de leurs propriétés chimiques particulières. On les retrouve notamment dans certains textiles, dans les emballages ou ustensiles en contact avec les aliments (comme agents antitaches), ainsi que dans les peintures, colles, mousses anti-incendie, certains cosmétiques et produits d’hygiène. En raison de leur stabilité chimique, les PFAS s’accumulent dans les tissus biologiques et dans l’environnement.
Les résultats d’études effectuées chez les rongeurs ont montré que l’exposition au perfluorooctanesulfonate (PFOS) ou au perfluorohexanesulfonate (PFHxS) entraînait une réduction du poids du placenta [1, 2]. En revanche, les effets du perfluorooctanoate (PFOA) sur ce paramètre variaient selon la dose : certaines études rapportaient une diminution, et d’autres une augmentation du poids placentaire [3, 4]. Une diminution du rapport entre le poids fœtal et le poids placentaire a également été rapportée après exposition au PFOA et au PFOS chez la souris, ainsi qu’au perfluorobutanesulfonate (PFBS) chez le lapin [3-5]. Sur le plan histopathologique, l’exposition au PFOA a été associée à la formation de caillots de fibrine [4], à l’apparition de zones de nécrose [3], ainsi qu’à une réduction de la surface du labyrinthe placentaire, principal site des échanges fœtomaternels chez la souris [4]. Des altérations similaires ont été constatées après exposition aux PFOS et au PFHxS, avec une réduction de la surface du labyrinthe et du nombre de vaisseaux sanguins [1].
Malgré un nombre croissant de données toxicologiques, suggérant des effets délétères des PFAS sur le placenta, les études épidémiologiques, et en particulier celles intégrant l’impact des PFAS sur la structure placentaire, sont encore peu nombreuses [6-8]. Dans une étude récente, 26 PFAS ont été dosés dans le sérum maternel prélevé à 19 semaines de gestation chez 367 femmes enceintes recrutées dans la cohorte française SEPAGES [9]. Parmi les 26 PFAS, 13 ont été quantifiés dans un nombre suffisant d’échantillons et inclus dans cette analyse. Le placenta a été pesé à l’accouchement. L’examen histologique des tissus placentaires a permis d’évaluer la perfusion vasculaire (proportion de villosités présentant des nodules syncytiaux, densité capillaire, espace intervilleux) ainsi que le « vieillissement » placentaire (dépôts de fibrine et présence de calcifications).
Les associations entre les PFAS et chacun de ces paramètres ont été étudiées à l’aide de régressions linéaires et logistiques ajustées (analyse « unipolluant »). Dans le but d’étudier l’effet combiné de ces PFAS, des analyses de type « multi-polluants » (analyse de clusters et modèle BKMR2) ont aussi été réalisées. Afin de limiter le risque de biais de confusion résiduel, ces modèles ont été ajustés pour les variables suivantes : la parité (nombre de grossesses antérieures), l’âge maternel à la conception, le niveau d’éducation maternel, le tabagisme actif et passif au cours de la grossesse, l’indice de masse corporelle pré-gestationnel, l’âge gestationnel à la naissance, le sexe de l’enfant, et la maternité où a lieu l’accouchement. Certains facteurs alimentaires ont aussi été pris en compte car ils ont été associés aux concentrations sanguines de PFAS dans la cohorte SEPAGES [10]. Les principaux résultats suggèrent des associations entre certains PFAS, pris individuellement, et plusieurs marqueurs histologiques placentaires, en particulier ceux liés aux échanges fœto-maternels. Trois PFAS, PFHxPA, PFHpA et PFTrDA, étaient associés à des altérations de la perfusion placentaire, faisant craindre une perturbation des échanges fœto-maternels.
Chez les femmes pour lesquelles le PFHxPA était quantifié, comparées à celles chez qui ce composé n’était pas quantifiable, nous avons constaté, en moyenne et après ajustement pour les facteurs de confusion potentiels, une augmentation de la proportion de villosités présentant des nodules syncytiaux, ainsi qu’une réduction de l’espace intervilleux. Des constats similaires ont été faits pour le PFHpA. Des associations isolées entre le PFTrDA et une augmentation de la proportion de villosités comportant des nodules syncytiaux ont également été faites, suggérant une altération des fonctions placentaires. Pour étudier l’effet conjoint des PFAS, une analyse de regroupement (clustering) permettant de classer les femmes en fonction de leurs concentrations sanguines en PFAS a été réalisée, ce qui a permis d’identifier trois groupes selon les niveaux d’exposition : faible, modéré, et fort. Seuls sept PFAS, détectés dans plus de 75 % des échantillons, ont pu être inclus dans cette analyse (PFOA, PFNA, PFOS, PFUnDA, PFDA, PFHpS et PFHxS). En raison de la taille réduite de l’échantillon dans le groupe ayant les concentrations sanguines les plus élevées, les femmes appartenant à ce groupe ont été regroupées avec celles ayant des concentrations modérées. En moyenne, et après ajustement pour les facteurs de confusion, les femmes appartenant à ce groupe « combiné » présentaient un poids placentaire plus faible comparativement à celles du groupe le moins exposé.
Les résultats de cette étude indiquent que les PFAS peuvent perturber le développement du placenta. Les associations constatées concernaient trois PFAS (PFTrDA, PFHxPA et PFHpA) et des marqueurs histologiques (augmentation de la proportion de villosités placentaires présentant des nœuds syncytiaux et réduction de l’espace intervilleux), suggérant un défaut de perfusion placentaire pouvant entraîner une hypoxie et contribuer à une insuffisance placentaire. De telles altérations de la structure histologique du placenta ont précédemment été décrites en cas d’hypertension artérielle, de prééclampsie, ou d’anémie maternelles, ainsi qu’en présence d’un risque accru de retard de croissance intra-utérin [11]. Les mécanismes biologiques qui pourraient expliquer un effet des PFAS sur le placenta incluent des interférences avec le métabolisme des lipides impliquant les récepteurs PPAR (récepteurs activés par les proliférateurs de peroxysomes), la perturbation du développement du cytotrophoblaste et l’altération des processus angiogéniques.
Cette étude est la première à examiner les effets de l’exposition aux PFAS sur l’histologie placentaire dans l’espèce humaine (Figure 1). L’inclusion des marqueurs histologiques des échanges fœto-maternels et du vieillissement placentaire en plus des indicateurs traditionnellement utilisés, tels que le poids du placenta, a permis d’approfondir la description de ces effets sur la santé placentaire. Le fait que la plupart des associations ont été trouvées avec les paramètres histologiques suggère que ceux-ci pourraient être plus sensibles à l’expositions environnementale aux PFAS que le poids du placenta. Néanmoins, ces associations n’ont été constatées qu’avec les variables d’exposition catégorielles, ce qui appelle une interprétation prudente des résultats. La taille modeste de la population limitait la puissance statistique et pourrait expliquer le petit nombre d’associations significatives avec le poids du placenta notamment.
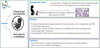 |
Figure 1 Exposition aux PFAS pendant la grossesse : conséquences sur la santé materno-fœtale et le fonctionnement du placenta. |
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Lee CK, Kang SG, Lee JT, et al. Effects of perfluorooctane sulfuric acid on placental PRL-family hormone production and fetal growth retardation in mice. Mol Cell Endocrinol 2015 ; 401 : 165–72. [Google Scholar]
- Li X, Ye L, Ge Y, et al. In utero perfluorooctane sulfonate exposure causes low body weights of fetal rats: A mechanism study. Placenta 2016 ; 39 : 125–33. [Google Scholar]
- Suh CH, Cho NK, Lee CK, et al. Perfluorooctanoic acid-induced inhibition of placental prolactin-family hormone and fetal growth retardation in mice. Mol Cell Endocrinol 2011 ; 337 : 7–15. [Google Scholar]
- Blake BE, Cope HA, Hall SM, et al. Evaluation of maternal, embryo, and placental effects in CD-1 mice following gestational exposure to perfluorooctanoic acid (PFOA) or hexafluoropropylene oxide dimer acid (HFPO-DA or GenX). Environ Health Perspect 2020 ; 128 : 027006. [Google Scholar]
- Crute CE, Landon CD, Garner A, et al. Maternal exposure to perfluorobutane sulfonate (PFBS) during pregnancy: evidence of adverse maternal and fetoplacental effects in New Zealand White (NZW) rabbits. Toxicol Sci 2023 ; 191 : 239–52. [Google Scholar]
- Fei C, McLaughlin JK, Tarone RE, et al. Fetal growth indicators and perfluorinated chemicals: A study in the Danish national birth cohort. Am J Epidemiol 2008 ; 168 : 66–72. [Google Scholar]
- Gan H, Xing Y, Tong J, et al. Impact of gestational exposure to individual and combined per- and polyfluoroalkyl substances on a placental structure and efficiency: Findings from the Ma’anshan birth cohort. Environ Sci Technol 2024 ; 58 : 6117–27. [Google Scholar]
- Chowdhury SF, Prout N, Rivera-Núñez Z, et al. PFAS alters placental arterial vasculature in term human placentae: A prospective pregnancy cohort study. Placenta 2024 ; 149 : 54–63. [Google Scholar]
- Khan S, Ouidir M, Lemaitre N, et al. PFAS exposure during pregnancy: Implications for placental health and functioning. Environ Int 2025 ; 197 : 109308. [Google Scholar]
- Jovanovic N, Brantsæter AL, Lyon-Caen S, et al. Levels and determinants of exposure to perfluoroalkyl substances in French pregnant women from the SEPAGES cohort. Environ Int 2025 ; 201 : 109559. [Google Scholar]
- Granger JP, Alexander BT, Llinas MT, et al. Pathophysiology of preeclampsia: linking placental ischemia/hypoxia with microvascular dysfunction. Microcirculation 2002 ; 9 : 147–60. [Google Scholar]
Dysfonctionnement placentaire responsable d’une hypertension artérielle et d’une protéinurie chez la femme enceinte.
La méthode BKMR (Bayesian kernel machine regression) est utilisée pour analyser les effets de mélanges de polluants sur la santé.
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Exposition aux PFAS pendant la grossesse : conséquences sur la santé materno-fœtale et le fonctionnement du placenta. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




