| Issue |
Med Sci (Paris)
Volume 32, Number 8-9, Août–Septembre 2016
Nos jeunes pousses ont du talent !
|
|
|---|---|---|
| Page(s) | 708 - 710 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/20163208015 | |
| Published online | 12 septembre 2016 | |
Perforine, granzyme et granulysine : un trio de choc inducteur de la microptose parasitaire
Perforin, granzyme and granulysin association to kill intracellular parasites
1
M1 Biologie Santé, Université Paris-Saclay, 91405 Orsay, France
2
École normale supérieure de Cachan
3
Inserm UMR 1186, immunologie intégrative des tumeurs, Institut Gustave Roussy, 114, rue Edouard Vaillant, 94800 Villejuif, France
a
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
b
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
c
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
c
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Cette Nouvelle fait partie d’une série de 15 Nouvelles rédigées par les étudiants du Master « Biologie Santé » de l’université Paris-Saclay qui paraîtront dans les numéros 6-7, 8-9 et 10 (2016) de médecine/sciences.
Ces trois auteurs ont participé également à la rédaction de cette Nouvelle.
La réponse immunitaire antiparasitaire et l’émergence du rôle de la granulysine
Les infections parasitaires représentent un défi majeur non seulement sur le plan de la prise en charge thérapeutique, mais aussi pour la compréhension des mécanismes immunitaires mis en jeu pour lutter contre ces infections. L’élimination des parasites par le système immunitaire fait intervenir différentes composantes. En particulier, les hydrolases lysosomales et les espèces oxygénées réactives (ROS) des macrophages jouent un rôle clé dans l’immunité antiparasitaire. De plus, les lymphocytes T cytotoxiques CD8+ (ou CTL) participent activement à l’élimination de ces pathogènes, notamment par la sécrétion d’interféron-γ (IFN-γ) et/ou par la destruction de la cellule hôte par apoptose [1].
L’élimination d’une cellule cible par les CTL est essentiellement induite par la libération, au niveau de la zone de contact entre la cellule effectrice et la cellule cible (ou synapse immunologique), du contenu de lysosomes sécrétoires spécialisés (appelés granules cytotoxiques) présents dans le cytoplasme de ces cellules tueuses. Ces granules cytotoxiques contiennent la protéine formant des pores perforine (PFN) et une famille de sérine protéases, les granzymes (Gzm), qui activent diverses voies de signalisation aboutissant à l’apoptose de la cellule cible. Parmi ces Gzm, le granzyme B (GzmB) est l’un des principaux inducteurs de l’apoptose ; il est exclusivement délivré dans le cytoplasme des cellules cibles par la perforine [2].
Chez l’homme, mais pas chez le rongeur, les granules cytotoxiques contiennent également une protéine aux propriétés antimicrobiennes appelée granulysine (GNLY) [3], qui altère préférentiellement la perméabilité des membranes pauvres en cholestérol comme celles des bactéries, champignons ou parasites. Différentes études ont ainsi montré qu’à forte concentration, la granulysine est cytotoxique contre différentes bactéries, mais elles suggèrent que la granulysine pourrait agir de concert avec d’autres molécules. De plus, étant donné que les patients souffrant de déficits immunitaires lymphocytaires T présentent une susceptibilité accrue aux infections bactériennes, fongiques et parasitaires, des travaux ont été réalisés pour déterminer le rôle et le mécanisme d’action de la granulysine dans l’immunité antimicrobienne induite par les CTL. Une étude récente a ainsi mis en évidence le rôle coopératif de la granulysine, du granzyme B et de la perforine dans l’élimination des bactéries intracellulaires induite par les CTL [4]. Néanmoins, le rôle éventuel et le mécanisme d’action de la granulysine dans l’immunité antiparasitaire restaient à déterminer.
Dans une étude publiée récemment dans Nature Medicine [5], Dotiwala et al. ont mis en évidence que la granulysine est également impliquée dans la réponse immunitaire induite contre les parasites intracellulaires Trypanosoma cruzi (responsable de la maladie de Chagas), Toxoplasma gondii (responsable de la toxoplasmose), et Leishmania major (responsable de la leishmaniose).
Perforine et granulysine permettent au granzyme B d’accéder aux parasites intracellulaires
En utilisant de la granulysine recombinante, les auteurs ont mis en évidence que cette protéine permet l’internalisation du granzyme B dans des parasites isolés ou présents dans le cytoplasme de cellules épithéliales humaines infectées. De plus, il apparaît que la perforine n’est pas impliquée dans la perméabilisation de la membrane parasitaire, mais est essentielle pour l’internalisation de la granulysine et du granzyme B dans le cytoplasme des cellules infectées. Ce mécanisme d’internalisation en deux étapes du granzyme B dans les parasites semble être concordant avec celui démontré précédemment pour l’élimination des bactéries intracellulaires [4]. De plus, les travaux réalisés montrent que cette internalisation du granzyme B induit la mort des parasites intracellulaires après 15 à 30 min de traitement des cellules infectées par perforine/granzyme B/granulysine, suivie 45 à 60 min plus tard de la mort de la cellule hôte. Cette différence de cinétique pourrait être cruciale pour limiter la propagation du pathogène en empêchant sa libération dans le milieu extracellulaire lors de la destruction d’une cellule hôte par les CTL.
Perforine, granulysine et granzyme B induisent la « microptose » parasitaire
Sur la base de ces observations, Dotiwala et al. ont exploré les mécanismes cellulaires et moléculaires conduisant à la mort des parasites en réponse à l’internalisation du granzyme B. Les parasites subissent une série d’événements rappelant l’apoptose des organismes pluricellulaires : gonflement des mitochondries, condensation de la chromatine, fragmentation nucléaire et bourgeonnement membranaire. De plus, la mort du parasite s’accompagne d’une forte production de ROS, d’une oxydation de l’ADN, d’une dissipation du potentiel transmembranaire mitochondrial et d’une externalisation de la phosphatidylsérine. Étonnamment, une activité caspase-like a été détectée lors de la mort du parasite, alors que la présence de protéines similaires aux caspases n’a jamais été identifiée chez les parasites. Néanmoins, cette activité caspase-like ne semble pas essentielle au déroulement du processus de mort. En effet, l’induction de ROS par le granzyme B dans le parasite est l’événement crucial pour sa destruction. Cette production de ROS est le résultat du clivage par le granzyme B de différentes protéines du parasite impliquées dans l’oxydoréduction et dans sa défense contre le stress oxydatif. Le granzyme B semble donc induire la génération de nombreux anions superoxydes tout en bloquant les mécanismes permettant de les éliminer. L’ensemble de ces éléments ont amené les auteurs de ces travaux à proposer le terme de « microptose » pour décrire la mort parasitaire induite par le trio perforine/granzyme B/granulysine (Figure 1).
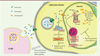 |
Figure 1. Les lymphocytes T cytotoxiques induisent la « microptose » parasitaire par la voie perforine, granulysine et granzyme B. Après reconnaissance par le LT CD8+ cytotoxique de la cellule cible infectée, l’exocytose du contenu des granules cytotoxiques conduit à la libération du trio perforine, granzyme, granulysine au niveau de la synapse immunologique. La perforine permet l’internalisation de la granulysine et du granzyme B au niveau du cytoplasme de la cellule cible (directement ou après endocytose). En interagissant avec la membrane parasitaire, la granulysine permet l’entrée du granzyme B dans le parasite. Le granzyme B va alors induire rapidement (5 à 10 min) la génération d’espèces réactives de l’oxygène (ROS) et un stress oxydatif au niveau de l’ADN du parasite par le clivage de différentes enzymes impliquées dans les réactions d’oxydoréduction et dans la protection contre le stress oxydatif (SOD A et B, APX, MPX, CPX TryX, etc.) menant à la mort du parasite (1) après environ 30 min. Le granzyme B va également induire une dissipation du potentiel membranaire mitochondrial (∆Ψm), une fragmentation nucléaire, ou encore l’externalisation des phosphatidylsérines (PS) au niveau de la membrane du parasite. En parallèle, le granzyme B va induire la destruction de la cellule hôte (2) par activation de la voie mitochondriale (clivage de BID [BH3 interacting-domain agonist], libération de cytochrome c, activation de la caspase 3) et génération de ROS. Cette apoptose de la cellule hôte se déroule avec une cinétique plus longue (45 à 60 min) que celle de la « microptose » parasitaire, permettant une élimination du parasite avant la destruction de la cellule infectée. |
L’expression de la granulysine améliore la réponse antiparasitaire des lymphocytes T chez les souris
Afin de confirmer le rôle in vivo de la granulysine, les auteurs ont analysé son impact chez les souris atteintes de différentes parasitoses. Les rongeurs n’exprimant pas la granulysine, des animaux transgéniques ont été obtenus par insertion dans leur génome du gène humain et de ses séquences régulatrices, limitant ainsi son expression aux CTL et aux cellules NK (natural killer). Les souris GNLY+/- survivent plus longtemps que les souris sauvages à une infection parasitaire par Trypanosoma cruzi, et la parasitémie est diminuée. Ces résultats confirment les résultats obtenus in vitro et démontrent que la granulysine est impliquée dans la réponse immunitaire antiparasitaire in vivo. De plus, les résultats obtenus dans ce modèle montrent que les lymphocytes T CD8+ contribuent majoritairement à cette protection.
Perspectives
Dans ce travail, Dotiwala et al. ont mis en évidence le rôle coopératif du trio perforine/granzyme B/granulysine dans la lutte contre les parasites intracellulaires exercée par les CTL et identifié un nouveau type de mort cellulaire, baptisé microptose, induit par l’action du granzyme B et largement dépendant des ROS. Cette étonnante observation d’un type de mort cellulaire qui pourrait s’apparenter à une mort cellulaire programmée chez un parasite ouvre la voie à de nouvelles perspectives de recherches fondamentale et thérapeutique. En effet, la description précise des cascades moléculaires impliquées dans l’induction de la microptose pourrait conduire à l’identification de nouvelles cibles thérapeutiques exploitables pour la lutte antiparasitaire. De plus, les résultats montrent que des souris exprimant la granulysine survivent mieux aux infections parasitaires : cette observation est en contradiction avec des résultats antérieurs suggérant que la sécrétion d’IFN-γ plutôt que l’effet cytotoxique des cellules T CD8+, permet de contrôler les infections par T. cruzi, et remet en cause la pertinence de ces résultats chez l’homme. De plus, étant donné l’activité de la granulysine sur les membranes pauvres en cholestérol, cette réponse immune dépendante de l’induction de microptose pourrait également s’appliquer à d’autres protozoaires et à d’autres parasites multicellulaires. Dans tous les cas, de futures études seront clairement nécessaires afin d’élucider ces différents points.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- De Alencar BC, Persechini PM, Haolla FA, et al. Perforin and gamma interferon expression are required for CD4+ and CD8+ T-cell-dependent protective immunity against a human parasite, Trypanosoma cruzi, elicited by heterologous plasmid DNA prime-recombinant adenovirus 5 boost vaccination. Infect Immun 2009 ; 77 : 4383–4395. [CrossRef] [PubMed] [Google Scholar]
- Chowdhury D, Lieberman J. Death by a thousand cuts: granzyme pathways of programmed cell death. Annu Rev Immunol 2008 ; 26 : 389–420. [CrossRef] [PubMed] [Google Scholar]
- Pena SV, Hanson DA, Carr BA, et al. Processing, subcellular localization, and function of 519 (granulysin), a human late T cell activation molecule with homology to small, lytic, granule proteins. J Immunol 1997 ; 158 : 2680–2688. [PubMed] [Google Scholar]
- Walch M, Dotiwala F, Mulik S, et al. Cytotoxic cells kill intracellular bacteria through granulysin-mediated delivery of granzymes. Cell 2014 ; 157 : 1309–1323. [CrossRef] [PubMed] [Google Scholar]
- Dotiwala F, Mulik S, Polidoro RB, et al. Killer lymphocytes use granulysin, perforin and granzymes to kill intracellular parasites. Nat Med 2016 ; 22 : 210–216. [Google Scholar]
© 2016 médecine/sciences – Inserm
Liste des figures
 |
Figure 1. Les lymphocytes T cytotoxiques induisent la « microptose » parasitaire par la voie perforine, granulysine et granzyme B. Après reconnaissance par le LT CD8+ cytotoxique de la cellule cible infectée, l’exocytose du contenu des granules cytotoxiques conduit à la libération du trio perforine, granzyme, granulysine au niveau de la synapse immunologique. La perforine permet l’internalisation de la granulysine et du granzyme B au niveau du cytoplasme de la cellule cible (directement ou après endocytose). En interagissant avec la membrane parasitaire, la granulysine permet l’entrée du granzyme B dans le parasite. Le granzyme B va alors induire rapidement (5 à 10 min) la génération d’espèces réactives de l’oxygène (ROS) et un stress oxydatif au niveau de l’ADN du parasite par le clivage de différentes enzymes impliquées dans les réactions d’oxydoréduction et dans la protection contre le stress oxydatif (SOD A et B, APX, MPX, CPX TryX, etc.) menant à la mort du parasite (1) après environ 30 min. Le granzyme B va également induire une dissipation du potentiel membranaire mitochondrial (∆Ψm), une fragmentation nucléaire, ou encore l’externalisation des phosphatidylsérines (PS) au niveau de la membrane du parasite. En parallèle, le granzyme B va induire la destruction de la cellule hôte (2) par activation de la voie mitochondriale (clivage de BID [BH3 interacting-domain agonist], libération de cytochrome c, activation de la caspase 3) et génération de ROS. Cette apoptose de la cellule hôte se déroule avec une cinétique plus longue (45 à 60 min) que celle de la « microptose » parasitaire, permettant une élimination du parasite avant la destruction de la cellule infectée. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




