Figure 2.
Télécharger l'image originale
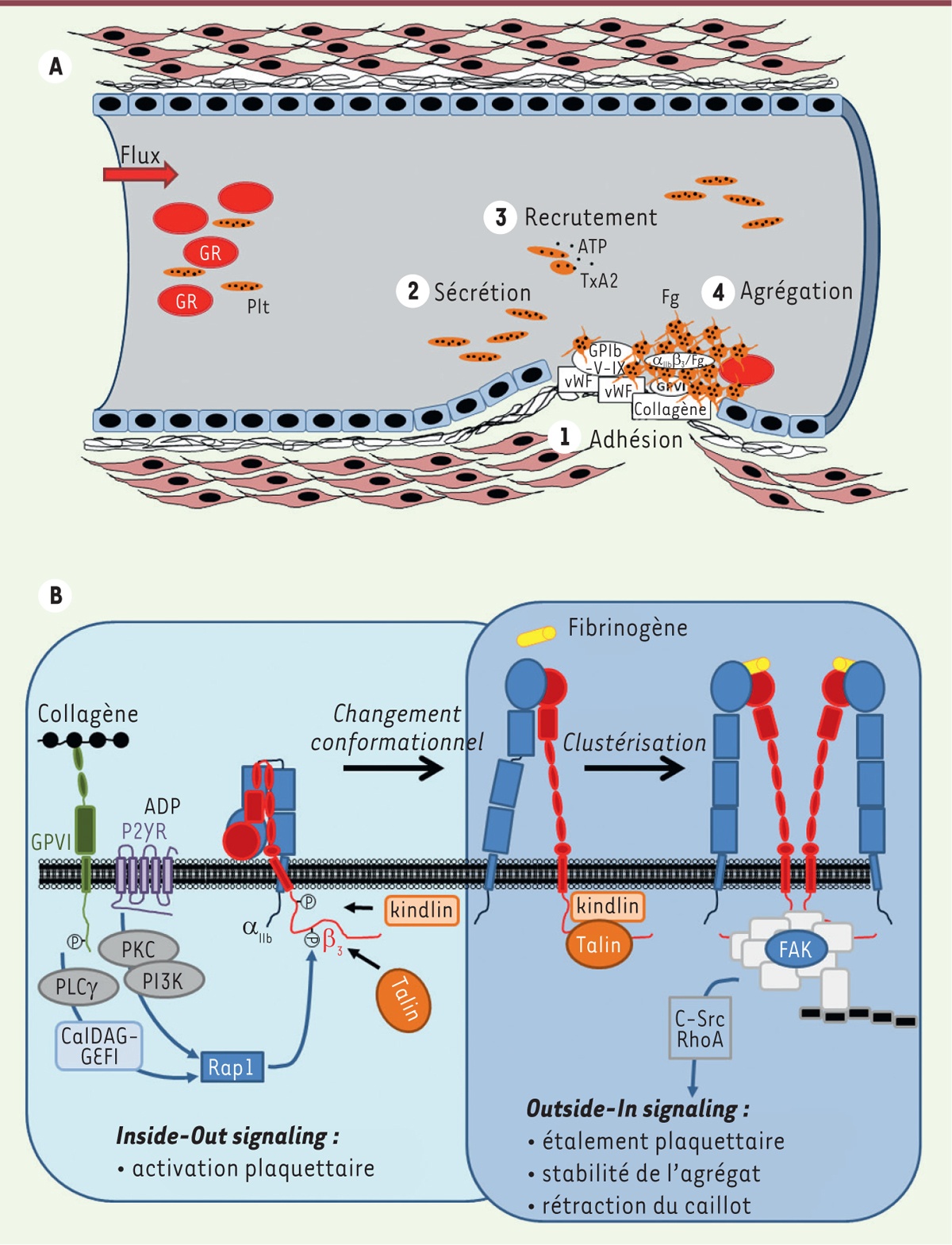
A. Rôle des principaux acteurs (plaquettes, protéines du sous-endothélium) dans la formation du thrombus blanc lors de l’hémostase primaire. Lors de la formation d’une brèche vasculaire, les plaquettes vont adhérer (1) au collagène et au facteur von Willebrand du sous-endothélium grâce à des récepteurs spécifiques (GP[glycoprotéine]VI et GPIb-IX-V). Les plaquettes vont alors s’activer, changer de forme, sécréter leur contenu en granules (2) et recruter d’autres plaquettes circulantes (3). L’ensemble de ces événements conduit à l’activation de l’intégrine αIIbβ3 nécessaire à l’agrégation des plaquettes via la fixation du fibrinogène (4). B. Représentation schématique du processus d’activation de l’intégrine αIIbβ3 plaquettaire.Inside-out signaling : de nombreux agonistes plaquettaires tels que l’adénosine diphosphate (ADP) ou le collagène sont capables d’induire un changement conformationnel d’αIIbβ3, indispensable à l’augmentation d’affinité de celle-ci pour son ligand, grâce à une signalisation complexe. Via leurs récepteurs respectifs, l’ADP et le collagène stimulent une phospholipase C (PLCγ) et une protéine kinase C (PKC) mettant en jeu la PI3-kinase (PI3K). Ces événements déclenchent l’activation de la protéine CalDAG-GEFI, une protéine d’échange de nucléotide guanylique activant elle-même la protéine Rap1, ce qui permet la phosphorylation sur des résidus sérine et thréonine de la partie cytoplasmique de la chaîne β3 de l’intégrine. Cela entraîne la réorganisation de l’interaction d’αIIb avec β3 par l’intermédiaire de protéines intracellulaires, parmi lesquelles la taline et les protéines de type Kindlin, qui sont capables d’interagir directement avec la partie cytoplasmique de l’intégrine, conduisant au changement conformationnel d’αIIbβ3. Outside-in signaling : la fixation du fibrinogène provoque une diffusion latérale de l’intégrine dans la membrane, ce qui contribue à son regroupement (clustérisation). Des signaux intracellulaires spécifiques sont alors émis permettant la formation d’un complexe d’adhérence focale, impliquant notamment la protéine FAK (focal adhesion kinase). Ces événements induisent la phosphorylation de la protéine kinase c-Src qui modifie l’état d’activation de la GTPase RhoA. GR : globules rouges ; Plt : plaquettes ; vWF : facteur von Willebrand ; TxA2 : thromboxane A2 ; Fg : fibrinogène ; CalDAG-GEFI : calcium- and diacylglycerol-regulated guanine exchange factor-1 ; Rap1 : Ras-proximate-1.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




