| Issue |
Med Sci (Paris)
Volume 31, Number 4, Avril 2015
|
|
|---|---|---|
| Page(s) | 367 - 369 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/20153104007 | |
| Published online | 8 mai 2015 | |
Une horloge circannuelle sonne le réveil des hibernants
A circannual clock wakes up hibernating mammals
Institut des neurosciences cellulaires et intégratives, UPR CNRS 3212, 5, rue Blaise Pascal, 67084 Strasbourg, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Quand les vertébrés primitifs ont envahi les milieux terrestres, ils y ont trouvé une production végétale abondante qui a permis l’explosion des espèces. Mais ils se sont également heurtés à d’importantes fluctuations saisonnières de cette production en fonction des variations de la durée du jour (photopériode), de la température et de l’humidité. Il leur a donc fallu développer des stratégies adaptatives pour survivre aux périodes de disette, et pour concentrer les coûts de la reproduction sur les périodes de production primaire maximale (Figure 1).
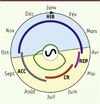 |
Figure 1. Schéma général de la distribution des processus physiologiques au cours des saisons chez les mammifères hibernants. Les fluctuations saisonnières de la disponibilité des ressources dans l’environnement (trait vert) et la durée journalière de la lumière (photopériode courte : bleu ; ou longue : jaune) sont les principaux facteurs externes qui synchronisent l’activité de l’horloge circannuelle (au centre) avec les saisons. Ceci permet d’optimiser le début et la fin de l’hibernation (HIB), de l’activité reproductive (REP), de la croissance des petits (CR) et de l’accumulation de réserves (ACC) nécessaires à la phase d’hibernation suivante. Ce cycle se répète tout au long de la vie d’un individu, et ses caractéristiques dépendent de l’espèce. |
L’hibernation est l’une des stratégies utilisées pour survivre à des conditions environnementales difficiles. Elle s’est développée à partir de mécanismes ancestraux d’inhibition métabolique communs à tous les êtres vivants (dormance, cryptobiose, etc.). Les mammifères hibernants y ont ajouté la réduction de la température corporelle (torpeur), qui ralentit les réactions métaboliques et diminue les besoins [1]. Ils peuvent ainsi survivre jusqu’à 8 mois sur 12 sans apport alimentaire, en utilisant les réserves accumulées l’été précédent sous forme, soit de graines, soit le plus souvent de réserves intracorporelles (lipides). Au cours de l’hivernage, les phases de torpeur sont interrompues par de brefs réveils, dont le dernier, l’émergence, marque le début de la reproduction printanière.
La brièveté de la saison estivale laisse peu de temps pour la rencontre des sexes, l’allaitement, la croissance des jeunes et l’accumulation des réserves indispensables à la survie au cours de l’hiver suivant (Figure 1). Au Canada, des spermophiles1 émergent un mois avant la fonte des neiges et se livrent à jeun aux activités de reproduction. Chez l’ours, la durée de la gestation oblige la femelle à mettre bas et à allaiter en pleine hibernation sur ses réserves. Pour tous, le succès reproducteur dépend de la qualité de la synchronisation entre l’émergence et l’activation printanière de la reproduction. Pour émerger de leur terrier au jour dit, en l’absence de toute information extérieure, les animaux doivent disposer d’un système endogène de mesure du temps qui sonne le signal du réveil interne. Ce système fait intervenir une horloge circannuelle (circa : environ ; annus : an) endogène qui contrôle la synthèse de protéines hépatiques impliquées dans le réveil métabolique [2], et des mécanismes neuroendocriniens qui activent la reproduction [3].
L’horloge circannuelle, un calendrier interne
Des transitions rythmiques endogènes entre les physiologies d’été et d’hiver, en l’absence de signaux externes, s’observent chez de nombreuses espèces, des invertébrés aux mammifères. Cela suggère que le système endogène à l’origine de l’horloge circannuelle est issu de mécanismes ancestraux communs [4, 5]. Nous avons ainsi montré que le hamster d’Europe (Cricetus cricetus), maintenu en conditions constantes de photopériode et de température, présente un rythme circannuel de reproduction et de masse corporelle [3, 6].
À ce jour, la localisation et les mécanismes moléculaires de l’horloge circannuelle sont toujours inconnus. Néanmoins, des données expérimentales impliquent la pars tuberalis, une région de l’hypophyse très riche en récepteurs de la mélatonine, une hormone de la glande pinéale essentielle pour la synchronisation des fonctions saisonnières [7].
Les animaux dans leur terrier ne perçoivent pas les changements climatiques, ils doivent donc anticiper les variations saisonnières de l’environnement afin que leur système reproducteur soit prêt dès l’émergence. L’horloge circannuelle endogène est donc indispensable, mais il faut également qu’elle soit synchronisée, c’est-à-dire que sa période endogène d’environ 10 mois doit être modifiée pour coïncider avec celle de l’alternance des saisons, qui est de 12 mois. La production saisonnière de mélatonine et les variations annuelles de la photopériode apparaissent comme les deux principaux facteurs capables de synchroniser l’activité de l’horloge circannuelle [8].
Mécanismes centraux de l’horloge circannuelle
Nous avons beaucoup progressé récemment dans la connaissance des mécanismes d’action de la mélatonine pour le contrôle saisonnier de la reproduction [9]. La synthèse de mélatonine par la glande pinéale est exclusivement nocturne, et sa durée est proportionnelle à celle de la nuit. La mélatonine agit sur ses récepteurs localisés dans la pars tuberalis pour contrôler la production de l’hormone thyréostimuline (TSH). En hiver, la sécrétion prolongée de mélatonine inhibe la synthèse de TSH dans la pars tuberalis, tandis que son raccourcissement printanier permet au contraire la synthèse de TSH et sa libération dans la partie basale de l’hypothalamus. La TSH active l’expression de l’enzyme déiodinase 2 (Dio2) dans les tanycytes, cellules spécialisées situées au contact du troisième ventricule. La Dio2 stimule la synthèse locale d’hormone thyroïdienne T3, qui joue un rôle fondamental dans la régulation de la physiologie saisonnière, en particulier la reproduction. En effet, la T3 stimule la production neuronale des neuropeptides kisspeptine et RFRP3 (RFamide-related peptide 3), régulateurs centraux de l’axe gonadotrope.
Nous avons utilisé ces nouveaux acquis pour étudier les mécanismes de l’horloge circannuelle chez le hamster d’Europe [3]. Des hamsters mâles ont été privés de repères saisonniers en les exposant à une photopériode fixe et en supprimant la synthèse de mélatonine par pinéalectomie. Ces animaux ont conservé des rythmes circannuels de température interne, de masse corporelle et d’activité testiculaire (Figure 2A). De façon remarquable, même en l’absence du signal mélatoninergique, l’expression des gènes TSH dans la pars tuberalis, et Dio2 dans les tanycytes, présentait des rythmes circannuels en cohérence avec ceux des variables physiologiques (Figure 2B). Ainsi, l’expression de ces gènes était réprimée chez les animaux en hiver subjectif (caractérisé par des épisodes de torpeur fréquents, un amaigrissement et une inhibition de la reproduction), tandis qu’elle était maximale chez les animaux en été subjectif (sexuellement actifs et avec une masse corporelle accrue). L’expression du gène RFRP était également augmentée en été subjectif, démontrant que l’information circannuelle est intégrée dans le système neuroendocrine contrôlant l’activité de reproduction.
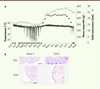 |
Figure 2. Rythmes circannuels chez l’hamster d’Europe. A. Rythmes circannuels de température (°C), masse corporelle (g) et taille testiculaire (mm) chez un hamster mâle privé de repères saisonniers. B. L’expression des gènes codant la TSH dans la pars tuberalis et Dio2 dans les tanycytes est inhibée quand les animaux se trouvent en phase d’hiver subjectif (hiver S) : phases de torpeur, diminution de la masse corporelle et régression testiculaire, tandis qu’elle augmente dans la phase d’été subjectif (été S) : augmentation de la température, de la masse corporelle et de la taille testiculaire. Barres d’échelle : TSH : 100 µm ; Dio2 : 50 µm. |
Ces résultats suggèrent que l’horloge circannuelle est localisée dans la pars tuberalis et utilise les mêmes voies de sortie neuroendocrines que celles qui assurent le contrôle saisonnier de la reproduction par la mélatonine. L’horloge circannuelle régule notamment l’expression de la TSH qui, via l’hormone T3 hypothalamique, transmet l’information circannuelle vers des structures centrales contrôlant de grandes fonctions biologiques, incluant probablement l’hibernation. L’horloge de la pars tuberalis a également été impliquée dans le contrôle circannuel de la sécrétion de prolactine par l’adénohypophyse, mais via des mécanismes indépendant de la TSH [7]. Dorénavant, les études sur le déterminisme des rythmes circannuels de l’hibernation et de la reproduction permettront de comprendre comment l’horloge circannuelle régule le début et l’émergence de l’hibernation et les coordonne aux autres fonctions saisonnières, notamment la reproduction.
Perspectives
Ces nouvelles connaissances ouvrent elles des perspectives d’application à l’homme ? Le caractère ancestral de l’hibernation permet de penser que l’homme a pu garder certains des mécanismes génomiques et neuroendocriniens mis en jeu dans l’hibernation. Il en est ainsi de l’inhibition métabolique qui peut seule expliquer les cas de survie à des arrêts cardiaques prolongés. La dépression saisonnière chez l’homme (seasonal affective disorder, SAD) s’apparente à l’hibernation par de multiples aspects [10]. Or, le suivi sur plusieurs années d’un patient atteint de SAD a mis en évidence un décours temporel évoquant une horloge circannuelle fonctionnant en libre cours [11]. En nous offrant une fenêtre sur les mécanismes neuroendocriniens de l’horloge circannuelle, les mammifères hibernants ouvrent des perspectives qui devraient tôt ou tard être applicables à l’homme.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Ce sont des rongeurs de la famille des écureuils (susliks ou écureuils terrestres).
Références
- Malan A. The evolution of mammalian hibernation: Lessons from comparative acid-base physiology. Integr Comp Biol 2014 ; 54 : 484–496. [CrossRef] [PubMed] [Google Scholar]
- Kondo N, Sekijima T, Kondo J. et al. Circannual control of hibernation by HP complex in the brain. Cell 2006 ; 125 : 161–172. [CrossRef] [PubMed] [Google Scholar]
- Sáenz de Miera C, Monecke S, Bartzen-Sprauer J. et al. A circannual clock drives expression of genes central for seasonal reproduction. Curr Biol 2014 ; 24 : 1500–1506. [CrossRef] [PubMed] [Google Scholar]
- Anderson DM, Keafer BA An endogenous annual clock in the toxic dinoflagellate Gonyaulax tamarensis. Nature 1987 ; 325 : 616–617. [CrossRef] [PubMed] [Google Scholar]
- Pengelley ET, Asmundson SJ. Circannual rhythmicity in hibernating mammals. In: Pengelley ET, (ed.) Circannual clocks: annual biological rhythms. London : Academic Press, INC, 1974 : 95–160. [CrossRef] [Google Scholar]
- Masson-Pévet M, Naimi F, Canguilhem B. et al. Are the annual reproductive and body-weight rhythms in the male European hamster (Cricetus cricetus) dependent upon a photoperiodically entrained circannual clock? J Pineal Res 1994 ; 17 : 151–163. [CrossRef] [PubMed] [Google Scholar]
- Lincoln GA, Clarke IJ, Hut RA. et al. Characterizing a mammalian circannual pacemaker. Science 2006 ; 314 : 1941–1944. [CrossRef] [PubMed] [Google Scholar]
- Woodfill CJ, Robinson JE, Malpaux B. et al. Synchronization of the circannual reproductive rhythm of the ewe by discrete photoperiodic signals. Biol Reprod 1991 ; 45 : 110–121. [CrossRef] [PubMed] [Google Scholar]
- Hazlerigg D, Simonneaux V. Seasonal regulation of reproduction in mammals. In: Plant T, Zeleznik A, eds. Knobil and Neill’s physiology of reproduction. Boston : Elsevier, 2015: In press. [Google Scholar]
- Gagné AM, Bouchard G, Tremblay P. et al. Quand la saison devient synonyme de dépression. Med Sci (Paris) 2010 ; 26 : 79–82. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Wirz-Justice A, Kräuchi K, Graw P An underlying circannual rhythm in seasonal affective disorder? Chronobiol Int 2001 ; 18 : 309–313. [CrossRef] [PubMed] [Google Scholar]
© 2015 médecine/sciences – Inserm
Liste des figures
 |
Figure 1. Schéma général de la distribution des processus physiologiques au cours des saisons chez les mammifères hibernants. Les fluctuations saisonnières de la disponibilité des ressources dans l’environnement (trait vert) et la durée journalière de la lumière (photopériode courte : bleu ; ou longue : jaune) sont les principaux facteurs externes qui synchronisent l’activité de l’horloge circannuelle (au centre) avec les saisons. Ceci permet d’optimiser le début et la fin de l’hibernation (HIB), de l’activité reproductive (REP), de la croissance des petits (CR) et de l’accumulation de réserves (ACC) nécessaires à la phase d’hibernation suivante. Ce cycle se répète tout au long de la vie d’un individu, et ses caractéristiques dépendent de l’espèce. |
| Dans le texte | |
 |
Figure 2. Rythmes circannuels chez l’hamster d’Europe. A. Rythmes circannuels de température (°C), masse corporelle (g) et taille testiculaire (mm) chez un hamster mâle privé de repères saisonniers. B. L’expression des gènes codant la TSH dans la pars tuberalis et Dio2 dans les tanycytes est inhibée quand les animaux se trouvent en phase d’hiver subjectif (hiver S) : phases de torpeur, diminution de la masse corporelle et régression testiculaire, tandis qu’elle augmente dans la phase d’été subjectif (été S) : augmentation de la température, de la masse corporelle et de la taille testiculaire. Barres d’échelle : TSH : 100 µm ; Dio2 : 50 µm. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




