| Issue |
Med Sci (Paris)
Volume 30, Number 11, Novembre 2014
Cils primaires et ciliopathies
|
|
|---|---|---|
| Page(s) | 1040 - 1046 | |
| Section | Cils primaires et ciliopathies | |
| DOI | https://doi.org/10.1051/medsci/20143011019 | |
| Published online | 10 novembre 2014 | |
De nouvelles fonctions extraciliaires pour les protéines ciliaires
Quelles conséquences sur l’apparition de ciliopathies ?
Non-ciliary functions of cilia proteins
CNRS-CRBM (centre de recherche en biochimie macromoléculaire), équipe centrosome, cil et pathologies, université de Montpellier, 1919, route de Mende, 34293
Montpellier, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Les protéines ciliaires ont initialement été caractérisées comme essentielles au bon fonctionnement des cils et sont impliquées dans les ciliopathies. Cependant, certains défauts cellulaires associés à leur dérégulation laissent entrevoir la possibilité de rôles extraciliaires pour ces protéines. En effet, de telles fonctions ont récemment été décrites pour ces protéines, notamment dans le transport vésiculaire, l’orientation du fuseau mitotique et le maintien de la stabilité chromosomique. Ces résultats soulèvent une importante question quant à la contribution de ces fonctions extraciliaires à l’apparition des manifestations cliniques associées aux ciliopathies, comme par exemple la polykystose rénale.
Abstract
Cilia proteins have long been characterized for their role in cilia formation and function, and their implications in ciliopathies. However, several cellular defects induced by cilia proteins deregulation suggest that they could have non-ciliary roles. Indeed, several non-ciliary functions have been recently characterized for cilia proteins including roles in intra-cellular and in vesicular transport, in spindle orientation or in the maintenance of genomic stability. These observations thus raise the crucial question of the contribution of non-ciliary functions of cilia proteins to the pathological manifestations associated with ciliopathies such as polycystic kidney disease.
Cet article fait partie du numéro thématique de médecine/sciences intitulé « Cils primaires et ciliopathies » (m/s n° 11, vol. 30, novembre 2014).
© 2014 médecine/sciences – Inserm
Les ciliopathies correspondent à un groupe hétérogène de maladies génétiques touchant aussi bien le rein (polykystose rénale) que l’œil, le cerveau, le foie et le cœur, ou pouvant provoquer une obésité et un diabète [1, 42–44] (→).
(→) Voir les Synthèses de R. Bachmann-Gagescu ; de K. Chennen et al. ; et de C. Laclef, pages 1011, 1034 et 980 de ce numéro
La présence systématique d’anomalies ciliaires structurales ou fonctionnelles dans ces pathologies a permis, malgré la grande diversité des manifestations cliniques qui leur sont associées, de les regrouper sous le terme de ciliopathies [1]. Les gènes mutés dans ces pathologies codent pour des protéines se localisant toutes au niveau du cil et/ou du corps basal (centrosome). Ces protéines sont donc essentielles à la formation ou au bon fonctionnement des cils [1]. Les cils sont des structures motiles ou sensorielles présentes à la surface d’une grande majorité de cellules de l’organisme, à l’exception principalement des lymphocytes T et des cellules en division. Ils sont essentiels au maintien de l’homéostasie tissulaire et jouent par conséquent un rôle majeur au cours du développement.
De nombreuses protéines peuvent être considérées comme « ciliaires » de par leur localisation au niveau du cil et/ou du corps basal, mais également de par leur rôle central dans la formation et la fonction des cils ou leur implication dans les ciliopathies. À ce jour, la liste de ces protéines dites « ciliaires » ne cesse de croître grâce à la caractérisation du protéome du cil et aux approches de séquençage à haut débit qui permettent d’identifier les mutations dans des gènes impliqués dans les ciliopathies [2, 3]. Parmi les protéines ciliaires les plus étudiées impliquées dans des pathologies ciliaires humaines [1], on peut citer celles qui interviennent dans les dyskinésies ciliaires, dans la polykystose rénale (PKD1 [polycystic kidney disease 1], PKD2, PKHD1 [polycystic kidney and hepatic disease 1]) ou dans la néphronophtise (NPHP [nephrocystin protein]), celles impliquées dans les syndromes de Meckel (MKS), de Joubert (RPGRIP1L), et de Bardet Biedl (BBS), la protéine OFD1 (oral-facial-digital syndrome 1), ou encore certaines protéines du transport intraflagellaire (IFT, intraflagellar transport) [42, 48] (→).
(→) Voir la Synthèse de C. Fort et P. Bastin, page 955 de ce numéro
Ces dernières ont initialement été décrites pour leur rôle de transport au niveau du flagelle de Chlamydomonas en association avec des moteurs de type kinésine (KIF3A [kinesin family member 3A]) ou dynéine, et sont impliquées dans des syndromes humains de ciliopathies tels que le syndrome de Jeune [4]. Toutes ces protéines sont donc bien caractérisées comme essentielles au bon fonctionnement ciliaire, et leur dérégulation contribue à l’apparition de ciliopathies. Mais ces protéines dites « ciliaires » ne pourraient-elles pas avoir également des fonctions extraciliaires ?
L’objectif de cette revue est d’identifier les dysfonctionnements cellulaires associés à des dérégulations de protéines ciliaires, de faire le point sur les fonctions extraciliaires qui ont récemment émergé pour des protéines considérées jusqu’alors comme protéines exclusivement ciliaires et, par conséquent, de poser la question de la contribution des fonctions extraciliaires de ces protéines dans les manifestations cliniques associées aux ciliopathies.
Défauts cellulaires associés aux protéines ciliaires : quelle place pour les fonctions extraciliaires ?
La dérégulation des protéines ciliaires a depuis longtemps été intimement liée à des défauts de ciliogenèse ou à des anomalies de la fonction ciliaire (Figure1A) [1]. Certaines protéines sont en effet importantes pour la formation ou la motilité des cils, d’autres sont nécessaires à la régulation de la signalisation cellulaire au niveau du cil, notamment pour le contrôle de la voie Sonic Hedgehog (Shh) [5, 45] (→).
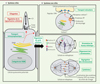 |
Figure 1. Fonctions des protéines ciliaires. Schéma récapitulatif des fonctions ciliaires (rouge) et extraciliaires (vert) des protéines du cil dans des systèmes ciliés ( A ) et non ciliés ( B ). RE : réticulum endoplasmique ; CMH : complexe majeur d’histocompatibilité. |
(→) Voir la Synthèse de C. Métin, page 991 ce numéro
Cependant, plusieurs travaux utilisant des approches d’ARN interférence en culture cellulaire ou des modèles in vivo de déplétion de protéines ciliaires, soulignent la présence de défauts pouvant avoir une origine extraciliaire (Tableau I). Ces défauts, qui incluent notamment des altérations du transport vésiculaire en amont ou indépendants de la formation du cil, des dérégulations du cycle cellulaire, des anomalies d’orientation de la division cellulaire, des problèmes d’alignement et de ségrégation des chromosomes, des défauts du nombre de centrosomes, des problèmes de cytokinèse ou des problèmes au niveau de l’intégrité de l’ADN, laissent entrevoir la possibilité de fonctions extraciliaires pour des protéines décrites jusqu’alors uniquement pour leur rôle ciliaire (Tableau I).
Fonctions extraciliaires associées aux protéines du cil. CEP164 : centrosomal protein of 164-kDa ; SDCCAG8 : serologically defined colon cancer antigen 8 ; OFD1 : oral-facial-digital syndrome 1 ; IFT : intraflagellar transport.
Transport intracytoplasmique et transport vésiculaire indépendants du cil
Parmi les fonctions extraciliaires, on peut citer le transport de certaines protéines ciliaires dans des compartiments cellulaires autres que le cil, et notamment au niveau du cytoplasme (Figure 1A). En effet, la déplétion de certaines protéines du transport intraflagellaire, initialement décrites pour leur rôle de cargo au niveau des cils et des flagelles, induit des défauts de transport vésiculaire intracytoplasmique. Ainsi, IFT20 joue un rôle important dans la localisation des protéines centrosomales au niveau du corps basal [6]. De plus, en accord avec un rôle cytoplasmique de la machinerie de transport intraflagellaire, IFT46 est 10 à 50 fois plus abondante dans le cytoplasme que dans le cil [7]. De manière intéressante, plusieurs protéines IFT sont également associées à des vésicules dans des systèmes non ciliés, tels que les cellules non ciliées de la rétine [8], suggérant que les fonctions de transport de ces protéines pourraient ne pas se limiter aux seules cellules ciliées. Un rôle strictement extraciliaire a même été démontré pour les protéines IFT, puisqu’elles sont impliquées dans le transport vésiculaire dans les lymphocytes T, cellules non ciliées (Figure 1B). En effet, plusieurs protéines IFT sont nécessaires à la mise en place de la synapse immunologique via le contrôle du recyclage du récepteur des lymphocytes T [9, 10]. Ces travaux démontrent de manière claire un rôle indépendant du cil pour les protéines du complexe IFT, ouvrant de nouvelles perspectives quant aux fonctions de transport associées à ces protéines. D’autres protéines ciliaires jouent également un rôle au niveau cytoplasmique, en amont de la formation du cil, comme les facteurs responsables de l’assemblage des bras de dynéine [11] ou la protéine BBS4 (Bardet–Biedl syndrome 4 protein), qui est localisée au niveau des satellites où elle est essentielle à l’adressage des protéines du matériel péricentriolaire, à la stabilisation du corps basal, et donc à l’organisation des microtubules [12].
Contrôle du cycle cellulaire et prolifération
La prolifération anormale des progéniteurs granulaires au niveau du cerveau induite par la déplétion de protéines ciliaires telles que KIF3A ou IFT88, a été proposée comme résultant d’une dérégulation de la voie Shh médiée par le cil [13]. Cependant, elle pourrait avoir également comme origine des défauts de régulation du cycle cellulaire indépendants du cil. En effet, la déplétion de BBS4, IFT27 ou IFT88 entraîne un retard ou bloque la progression à différentes étapes du cycle cellulaire, suggérant un rôle des protéines ciliaires dans le contrôle du cycle cellulaire (Figure 1) [12, 14, 15]. Même si l’origine de ces défauts reste à déterminer, il a été proposé que la transition centrosome/corps basal puisse être affectée, résultant en une activation des points de contrôle du cycle cellulaire [16]. Cet arrêt de cycle pourrait être causé par un défaut de recrutement des protéines centrosomales, dont l’absence induit des défauts de structure du centrosome et un arrêt du cycle dépendant de p38/p21/p53 [17]. Confirmant un rôle pour IFT88 dans la régulation du cycle cellulaire, une étude a montré que sa surexpression bloquait la progression du cycle cellulaire en G1/S, et que sa déplétion favorisait la progression du cycle cellulaire de cellules HeLa non ciliées. IFT88 pourrait, en effet, réguler la transition G1/S en interagissant avec la protéine Che-1, un inhibiteur de Rb (retinoblastoma protein) [18]. En accord avec cette observation, il existe, chez les souris mutantes pour IFT88, une hyperprolifération cellulaire dans différents tissus, expliquant que IFT88 ait été proposée comme suppresseur de tumeur potentiel [19, 20]. De même, les protéines PKD1 et PKD2 peuvent réguler le cycle cellulaire via la protéine Id2 (inhibitor of DNA binding 2) [21]. Que ces protéines agissent de façon strictement indépendante du cil dans le contrôle du cycle cellulaire reste cependant difficile à prouver puisque ciliogenèse, résorption ciliaire et cycle cellulaire sont intimement liés et peuvent s’influencer réciproquement [48] (→).
(→) Voir la Synthèse de N. Delgehyr et N. Spassky, page 976 de ce numéro
Orientation du fuseau mitotique
Des défauts d’orientation de la division cellulaire ont été observés chez différents mutants ciliaires, dont KIF3A, IFT88, IFT20, PKD1 ou encore PKHD1/fibrocystine, et ils sont principalement associés à une atteinte rénale polykystique [14, 22–25]. Ces défauts d’orientation ont initialement été décrits comme ayant une origine ciliaire via la dérégulation de la voie de polarité planaire qui oriente vectoriellement la cellule dans le plan de l’épithélium [22–25]. Cependant, des résultats récents suggèrent qu’ils pourraient avoir une origine différente en fonction des tissus étudiés ou des modèles utilisés [14, 26]. En accord avec un rôle des protéines ciliaires dans les cellules en mitose, l’expression de certaines IFT chez Chlamydomonas est augmentée dans les phases S-M [27]. De plus, nos travaux ont montré que, dans le cas de la déplétion d’IFT88, les défauts d’orientation de la division cellulaire peuvent être causés par un défaut structural du fuseau mitotique en métaphase, et seraient donc indépendants du cil [14]. Plus précisément, dans des cellules mitotiques non ciliées, IFT88 est essentielle au transport des microtubules périphériques vers les pôles du fuseau (Figure 1B). Ce mécanisme est dépendant de la dynéine et permet la formation rapide et robuste du réseau de microtubules astraux qui, via leur interaction avec le cortex cellulaire, permettent la bonne orientation du fuseau mitotique (Figure 1B). IFT88 est donc essentielle à la bonne orientation du fuseau mitotique via un mécanisme indépendant du cil. De plus, des études récentes faites au cours du développement chez le poisson suggèrent que IFT88 pourrait contrôler l’orientation de la division de manière indépendante du cil et de la polarité planaire [26]. Cependant, des anomalies des microtubules n’ont pas pu être mises en évidence dans ce modèle, soulevant la question de l’origine de cette mauvaise orientation. En raison de l’importance de l’orientation du fuseau mitotique dans le contrôle de la division asymétrique des cellules souches, et de la présence de défauts de prolifération des progéniteurs de cellules neuronales en absence d’IFT88, il est envisageable que, outre les défauts de la voie Shh décrits précédemment, le renouvellement anormal des cellules souches puisse être causé par une division asymétrique aberrante induite par un défaut d’orientation du fuseau mitotique, dont la cause serait indépendante du cil. En effet, une mauvaise orientation du fuseau mitotique pourrait aboutir à une division asymétrique anormale et, par conséquent, à un renouvellement incontrôlé des cellules souches [46].
Maintien de la stabilité génétique, cytokinèse
Des cellules issues de patients ou de modèles animaux présentant une polykystose rénale se caractérisent par la présence d’aneuploïdie [28, 29]. Les défauts de stabilité chromosomique pouvant générer de l’aneuploïdie sont engendrés au cours de la mitose. Cela suggère une origine potentiellement non ciliaire de ces défauts. En accord avec cette hypothèse, plusieurs groupes ont montré que des protéines ciliaires, et notamment PKD1, PKD2, PKHD1/fibro-cystine, KIF3A ou IFT88, pourraient avoir des fonctions mitotiques [14, 28–33]. PKHD1/fibrocystine est localisée au niveau du fuseau mitotique, et sa déplétion induit des fuseaux multipolaires et un mauvais alignement des chromosomes [30]. Des défauts similaires ont également été observés dans des cellules déplétées en IFT88, PKD1 ou PKD2 via la dérégulation de la protéine survivine [28, 29], suggérant un rôle de ces protéines dans l’organisation du fuseau mitotique et la ségrégation des chromosomes (Figure 1B). Ces défauts mitotiques sont décrits comme générant une instabilité chromosomique et peuvent aboutir à une aneuploïdie des cellules, voire à une polyploïdie en cas de problèmes de cytokinèse. Un rôle dans la cytokinèse a d’ailleurs été suggéré pour la protéine BBS6 [34], ainsi que pour plusieurs protéines de la machinerie de transport intraflagellaire [15, 27] ; IFT27, IFT46, IFT72 et IFT139 se localisent au niveau du sillon de clivage pendant la cytokinèse (Figure 1B) [27].
Enfin, il est intéressant de noter que les dommages à l’ADN observés lors de la déplétion de protéines ciliaires [35, 36], pourraient résulter des défauts de division décrits ci-dessus. L’origine ciliaire ou non de ces défauts reste cependant à identifier, mais pourrait révéler de nouvelles fonctions mitotiques ou nucléaires pour les protéines ciliaires, notamment dans le maintien de l’intégrité de l’ADN. Dans la logique d’une fonction nucléaire, OFD1 (oral-facial-digital syndrome 1) a été décrite comme interagissant avec des complexes de remodelage de la chromatine [37].
Les fonctions extraciliaires peuvent-elles contribuer aux manifestations pathologiques associées aux ciliopathies ?
Les anomalies ciliaires ont longtemps été acceptées comme étant la cause majeure et unique des ciliopathies. En effet, des défauts ciliaires sont observés dans les ciliopathies humaines ou dans des modèles animaux de ciliopathies. Cependant, les fonctions extraciliaires qui émergent pour des protéines jusqu’alors décrites uniquement pour leur rôle ciliaire, soulèvent la question de l’implication de ces fonctions dans l’apparition des différentes manifestations cliniques associées aux ciliopathies et, notamment, dans la polykystose rénale (Figure 2). En effet, la formation de kystes au niveau des reins pourrait être due, au moins partiellement, à des défauts cellulaires indépendants du cil [47] (→).
(→) Voir la Synthèse de M. Pacès-Fessy, page 1024 de ce numéro
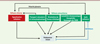 |
Figure 2. Fonctions extraciliaires et polykystose rénale. Schéma récapitulatif des fonctions ciliaires (rouge) et extraciliaires (vert) corrélées à l’apparition des polykystoses rénales. L’efficacité des inhibiteurs (bleu), connus pour bloquer la prolifération cellulaire, suggère un rôle des fonctions extraciliaires dans la polykystose rénale. |
Les défauts de transports intracytoplasmique et vésiculaire pourraient générer des problèmes de polarité cellulaire en amont de la formation du cil, ou directement réguler la mise en place de la polarité cellulaire via la modulation du cytosquelette d’actine [38]. D’autre part, les anomalies de division cellulaire, dont les défauts d’orientation du fuseau mitotique, ont été corrélées à l’apparition de polykystose rénale [14, 22–25], même si leur contribution directe à la pathologie reste discutée. De même, des défauts de prolifération, de stabilité chromosomique ou d’aneuploïdie ont été associés aux atteintes rénales caractéristiques des ciliopathies [28]. Enfin, même si la cause n’est pas connue, un travail récent a identifié des dommages à l’ADN dans des ciliopathies avec atteinte rénale [36]. En accord avec un rôle de la prolifération cellulaire dans les polykystoses rénales, une prolifération induite à la suite d’une blessure favorise l’apparition de kystes [22]. De plus, plusieurs inhibiteurs connus pour bloquer la prolifération cellulaire et la progression du cycle, tels que les inhibiteurs de la voie mTOR (mammalian target of rapamycin) ou des CDK (cyclin-dependent kinase), ont été utilisés avec succès dans des modèles animaux de polykystose rénale [39]. Cependant, dans ces modèles de polykystose rénale, l’origine exclusivement ciliaire ou non ciliaire des défauts reste à prouver.
Même si les défauts cellulaires indépendants du cil n’ont, pour l’instant, été corrélés qu’à l’apparition d’une polykystose rénale, une contribution multiple de ces fonctions à l’apparition des différentes manifestations cliniques caractéristiques des ciliopathies doit être envisagée, comme par exemple dans le cas des atteintes vasculaires associées aux ciliopathies [28]. Cette contribution pourrait permettre d’expliquer la diversité des manifestations pathologiques associées aux ciliopathies, ainsi que leur différence de gravité. De plus, la caractérisation précise des fonctions non ciliaires des protéines associées aux ciliopathies pourrait permettre d’identifier des sous-catégories « exclusivement ciliaires », par rapport à d’autres impliquant à la fois les fonctions ciliaires et extraciliaires des protéines en cause.
Conclusion
La multiplicité des fonctions extraciliaires récemment identifiées pour des protéines dont seules les fonctions ciliaires avaient été reconnues révèle les liens complexes existant entre l’état cilié et non cilié des cellules, et ouvre un vaste champ d’investigation. Cependant, la plupart des fonctions extraciliaires des protéines du cil restent encore mal caractérisées. Même si la fonction ciliaire reste une fonction centrale pour ces protéines, des fonctions alternatives ont été conservées ou acquises au cours de l’évolution, car elles sont essentielles à des processus cellulaires indépendants du cil. La complexité de l’étude de ces fonctions multiples est renforcée par le fait que des protéines initialement décrites pour leurs fonctions non ciliaires, mitotiques par exemple, peuvent également influencer la ciliogenèse. C’est le cas de la kinase Aurora A, initialement décrite pour son rôle mitotique, qui est également essentielle à la résorption du cil lors de l’entrée en cycle [16, 49]. De même, une comparaison des protéomes du cil et des protéines impliquées dans la cytokinèse montre que plusieurs protéines importantes pour la cytokinèse, PRC1 (protein regulator of cytokinesis 1) ou MKLP1 (mitotic kinesin-like protein 1), sont localisées au niveau du cil et régulent la structure et la fonction ciliaires [40]. Enfin, la protéine BubR1, connue pour son rôle dans la régulation du point de contrôle de l’assemblage du fuseau mitotique, influence la ciliogenèse [41]. Étant donné le nombre croissant de fonctions à la fois ciliaires et non ciliaires impliquant les protéines du cil et leur interdépendance, il est à l’heure actuelle difficile de dire lequel de ces processus est véritablement en amont de l’apparition des ciliopathies. La variabilité des phénotypes observés dans les ciliopathies impliquant différentes protéines ciliaires pourrait cependant être due à la diversité de fonctions impliquant ces protéines dans différents tissus. De futurs travaux permettront de mieux caractériser les fonctions extraciliaires des protéines ciliaires et de séparer les rôles ciliaires et non ciliaires des protéines impliquées dans les ciliopathies humaines. Ceci sera essentiel pour mieux comprendre la contribution des fonctions extraciliaires à l’apparition des manifestations cliniques associées aux ciliopathies et, par conséquent, pour mieux appréhender ces pathologies complexes.
Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Merci à Christelle Anguille pour sa lecture attentive de ce manuscrit. Notre équipe est actuellement financée par le CNRS, l’Agence nationale pour la recherche (ANR), la Fondation pour la recherche médicale en partenariat avec la Fondation Schlumberger pour l’éducation et la recherche (FRM-FSER), et le programme Marie Curie Career integration grant (Marie Curie CIG).
Références
- Hildebrandt F, Benzing T, Katsanis N. Ciliopathies. N Engl J Med 2011 ; 364 : 1533–1543. [CrossRef] [PubMed] [Google Scholar]
- Zaghloul NA, Katsanis N. Functional modules, mutational load and human genetic disease. Trends Genet 2010 ; 26 : 168–176. [CrossRef] [PubMed] [Google Scholar]
- Ishikawa H, Thompson J, Yates JR, et al. Proteomic analysis of mammalian primary cilia. Curr Biol 2012 ; 22 : 414–419. [CrossRef] [PubMed] [Google Scholar]
- Rosenbaum JL, Witman GB. Intraflagellar transport. Nat Rev Mol Cell Biol 2002 ; 3 : 813–825. [CrossRef] [PubMed] [Google Scholar]
- Huangfu D, Liu A, Rakeman AS, et al. Hedgehog signalling in the mouse requires intraflagellar transport proteins. Nature 2003 ; 426 : 83–87. [CrossRef] [PubMed] [Google Scholar]
- Jurczyk A, Gromley A, Redick S, et al. Pericentrin forms a complex with intraflagellar transport proteins and polycystin-2 and is required for primary cilia assembly. J Cell Biol 2004 ; 166 : 637–643. [CrossRef] [PubMed] [Google Scholar]
- Ahmed NT, Gao C, Lucker BF, et al. ODA16 aids axonemal outer row dynein assembly through an interaction with the intraflagellar transport machinery. J Cell Biol 2008 ; 183 : 313–322. [CrossRef] [PubMed] [Google Scholar]
- Sedmak T, Wolfrum U. Intraflagellar transport molecules in ciliary and nonciliary cells of the retina. J Cell Biol 2010 ; 189 : 171–186. [CrossRef] [PubMed] [Google Scholar]
- Finetti F, Patrussi L, Masi G, et al. Specific recycling receptors are targeted to the immune synapse by the intraflagellar transport system. J Cell Sci 2014 ; 127 : 1924–1937. [CrossRef] [PubMed] [Google Scholar]
- Finetti F, Paccani SR, Riparbelli MG, et al. Intraflagellar transport is required for polarized recycling of the TCR/CD3 complex to the immune synapse. Nat Cell Biol 2009 ; 11 : 1332–1339. [CrossRef] [PubMed] [Google Scholar]
- Omran H, Kobayashi D, Olbrich H, et al. Ktu/PF13 is required for cytoplasmic pre-assembly of axonemal dyneins. Nature 2008 ; 456 : 611–616. [CrossRef] [PubMed] [Google Scholar]
- Kim JC, Badano JL, Sibold S, et al. The Bardet-Biedl protein BBS4 targets cargo to the pericentriolar region and is required for microtubule anchoring and cell cycle progression. Nat Genet 2004 ; 36 : 462–470. [CrossRef] [PubMed] [Google Scholar]
- Spassky N, Han YG, Aguilar A, et al. Primary cilia are required for cerebellar development and Shh-dependent expansion of progenitor pool. Dev Biol 2008 ; 317 : 246–259. [CrossRef] [PubMed] [Google Scholar]
- Delaval B, Bright A, Lawson ND, et al. The cilia protein IFT88 is required for spindle orientation in mitosis. Nat Cell Biol 2011 ; 13 : 461–468. [CrossRef] [PubMed] [Google Scholar]
- Qin H, Wang Z, Diener D, et al. Intraflagellar transport protein 27 is a small G protein involved in cell-cycle control. Curr Biol 2007 ; 17 : 193–202. [CrossRef] [PubMed] [Google Scholar]
- Plotnikova OV, Golemis EA, Pugacheva EN. Cell cycle-dependent ciliogenesis and cancer. Cancer Res 2008 ; 68 : 2058–2061. [CrossRef] [PubMed] [Google Scholar]
- Mikule K, Delaval B, Kaldis P, et al. Loss of centrosome integrity induces p38–p53-p21-dependent G1-S arrest. Nat Cell Biol 2007 ; 9 : 160–170. [CrossRef] [PubMed] [Google Scholar]
- Robert A, Margall-Ducos G, Guidotti JE, et al. The intraflagellar transport component IFT88/polaris is a centrosomal protein regulating G1-S transition in non-ciliated cells. J Cell Sci 2007 ; 120 : 628–637. [CrossRef] [PubMed] [Google Scholar]
- Isfort RJ, Cody DB, Doersen CJ, et al. The tetratricopeptide repeat containing Tg737 gene is a liver neoplasia tumor suppressor gene. Oncogene 1997 ; 15 : 1797–1803. [CrossRef] [PubMed] [Google Scholar]
- Richards WG, Yoder BK, Isfort RJ, et al. Oval cell proliferation associated with the murine insertional mutation TgN737Rpw. Am J Pathol 1996 ; 149 : 1919–1930. [PubMed] [Google Scholar]
- Li X, Luo Y, Starremans PG, et al. Polycystin-1 and polycystin-2 regulate the cell cycle through the helix-loop-helix inhibitor Id2. Nat Cell Biol 2005 ; 7 : 1202–1212. [CrossRef] [PubMed] [Google Scholar]
- Patel V, Li L, Cobo-Stark P, et al. Acute kidney injury and aberrant planar cell polarity induce cyst formation in mice lacking renal cilia. Hum Mol Genet 2008 ; 17 : 1578–1590. [CrossRef] [PubMed] [Google Scholar]
- Jonassen JA, San Agustin J, Follit JA, et al. Deletion of IFT20 in the mouse kidney causes misorientation of the mitotic spindle and cystic kidney disease. J Cell Biol 2008 ; 183 : 377–384. [CrossRef] [PubMed] [Google Scholar]
- Luyten A, Su X, Gondela S, et al. Aberrant regulation of planar cell polarity in polycystic kidney disease. J Am Soc Nephrol 2010 ; 21 : 1521–1532. [CrossRef] [PubMed] [Google Scholar]
- Fischer E, Legue E, Doyen A, et al. Defective planar cell polarity in polycystic kidney disease. Nat Genet 2006 ; 38 : 21–23. [CrossRef] [PubMed] [Google Scholar]
- Borovina A, Ciruna B. IFT88 plays a cilia- and PCP-independent role in controlling oriented cell divisions during vertebrate embryonic development. Cell Rep 2013 ; 5 : 37–43. [CrossRef] [PubMed] [Google Scholar]
- Wood CR, Wang Z, Diener D, et al. IFT proteins accumulate during cell division, localize to the cleavage furrow in Chlamydomonas. PloS One 2012 ; 7 : e30729. [CrossRef] [PubMed] [Google Scholar]
- Aboualaiwi WA, Muntean BS, Ratnam S, et al. Survivin-induced abnormal ploidy contributes to cystic kidney and aneurysm formation. Circulation 2014 ; 129 : 660–672. [CrossRef] [PubMed] [Google Scholar]
- AbouAlaiwi WA, Ratnam S, Booth RL, et al. Endothelial cells from humans and mice with polycystic kidney disease are characterized by polyploidy and chromosome segregation defects through survivin down-regulation. Hum Mol Genet 2011 ; 20 : 354–367. [CrossRef] [PubMed] [Google Scholar]
- Zhang J, Wu M, Wang S, et al. Polycystic kidney disease protein fibrocystin localizes to the mitotic spindle and regulates spindle bipolarity. Hum Mol Genet 2010 ; 19 : 3306–3319. [CrossRef] [PubMed] [Google Scholar]
- Haraguchi K, Hayashi T, Jimbo T, et al. Role of the kinesin-2 family protein, KIF3, during mitosis. J Biol Chem 2006 ; 281 : 4094–4099. [CrossRef] [PubMed] [Google Scholar]
- Burtey S, Riera M, Ribe E, et al. Centrosome overduplication and mitotic instability in PKD2 transgenic lines. Cell Biol Int 2008 ; 32 : 1193–1198. [CrossRef] [PubMed] [Google Scholar]
- Battini L, Macip S, Fedorova E, et al. Loss of polycystin-1 causes centrosome amplification and genomic instability. Hum Mol Genet 2008 ; 17 : 2819–2833. [CrossRef] [PubMed] [Google Scholar]
- Kim JC, Ou YY, Badano JL, et al. MKKS/BBS6, a divergent chaperonin-like protein linked to the obesity disorder Bardet-Biedl syndrome, is a novel centrosomal component required for cytokinesis. J Cell Sci 2005 ; 118 : 1007–1020. [CrossRef] [PubMed] [Google Scholar]
- Chaki M, Airik R, Ghosh AK, et al. Exome capture reveals ZNF423 and CEP164 mutations, linking renal ciliopathies to DNA damage response signaling. Cell 2012 ; 150 : 533–548. [CrossRef] [PubMed] [Google Scholar]
- Airik R, Slaats GG, Guo Z, et al. Renal-retinal ciliopathy gene Sdccag8 regulates DNA damage response signaling. J Am SocNephrol 2014 (sous presse). [Google Scholar]
- Giorgio G, Alfieri M, Prattichizzo C, et al. Functional characterization of the OFD1 protein reveals a nuclear localization and physical interaction with subunits of a chromatin remodeling complex. Mol Biol Cell 2007 ; 18 : 4397–4404. [CrossRef] [PubMed] [Google Scholar]
- Cui C, Chatterjee B, Lozito TP, et al. Wdpcp, a PCP protein required for ciliogenesis, regulates directional cell migration, cell polarity by direct modulation of the actin cytoskeleton. PLoS Biol 2013 ; 11 : e1001720. [CrossRef] [PubMed] [Google Scholar]
- Ibraghimov-Beskrovnaya O, Natoli TA. mTOR signaling in polycystic kidney disease. Trends Mol Med 2011 ; 17 : 625–633. [CrossRef] [PubMed] [Google Scholar]
- Smith KR, Kieserman EK, Wang PI, et al. A role for central spindle proteins in cilia structure and function. Cytoskelet Hoboken 2011 ; 68 : 112–124. [CrossRef] [Google Scholar]
- Miyamoto T, Porazinski S, Wang H, et al. Insufficiency of BUBR1, a mitotic spindle checkpoint regulator, causes impaired ciliogenesis in vertebrates. Hum Mol Genet 2011 ; 20 : 2058–2070. [CrossRef] [PubMed] [Google Scholar]
- Bachmann-Gagescu R. Complexité génétique des ciliopathies et identification de nouveaux gènes. Med Sci (Paris) 2014 ; 30 : 1011–1023. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Chennen K, Scerbo MJ, Dollfus H, et al. Syndrome de Bardet-Biedl : cils et obésité. De la génétique à l’approche intégrative. Med Sci (Paris) 2014 ; 30 : 1034–1039. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Laclef C. Le cil primaire, orchestrateur de la morphogenèse cérébrale. Med Sci (Paris) 2014 ; 30 : 980–990. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Métin C. Cils et migrations neuronales. Med Sci (Paris) 2014 ; 30 : 991–995. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Hollande F, Joubert D. Fuseau mitotique et division asymétrique des cellules souches. Med Sci (Paris) 2010 ; 26 : 1027–1030. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Paces-Fessy M. Cils et kystes rénaux. Med Sci (Paris) 2014 ; 30 : 1024–1033. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Fort C, Bastin P. élongation de l’axonème et dynamique du transport intraflagellaire. Med Sci (Paris) 2014 ; 30 : 955–961. [Google Scholar]
- Delgehyr N, Spassky N. Cil primaire, cycle cellulaire et prolifération. Med Sci (Paris) 2014 ; 30 : 976–979. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des tableaux
Fonctions extraciliaires associées aux protéines du cil. CEP164 : centrosomal protein of 164-kDa ; SDCCAG8 : serologically defined colon cancer antigen 8 ; OFD1 : oral-facial-digital syndrome 1 ; IFT : intraflagellar transport.
Liste des figures
 |
Figure 1. Fonctions des protéines ciliaires. Schéma récapitulatif des fonctions ciliaires (rouge) et extraciliaires (vert) des protéines du cil dans des systèmes ciliés ( A ) et non ciliés ( B ). RE : réticulum endoplasmique ; CMH : complexe majeur d’histocompatibilité. |
| Dans le texte | |
 |
Figure 2. Fonctions extraciliaires et polykystose rénale. Schéma récapitulatif des fonctions ciliaires (rouge) et extraciliaires (vert) corrélées à l’apparition des polykystoses rénales. L’efficacité des inhibiteurs (bleu), connus pour bloquer la prolifération cellulaire, suggère un rôle des fonctions extraciliaires dans la polykystose rénale. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




