| Issue |
Med Sci (Paris)
Volume 30, Number 1, Janvier 2014
|
|
|---|---|---|
| Page(s) | 33 - 35 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/20143001010 | |
| Published online | 24 janvier 2014 | |
Vers un vaccin prophylactique bivalent contre les virus des hépatites B et C ?
Towards a bivalent prophylactic vaccine against hepatitis B and C viruses?
Inserm U966, Université François Rabelais et CHRU de Tours, 10, boulevard Tonnellé 37032 Tours, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
**
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
L’hépatite C en 2013
Au cours des dernières années, des progrès majeurs ont été réalisés en termes de traitements contre le virus de l’hépatite C (VHC), avec la mise au point d’antiviraux à action directe (DAA, pour direct-acting antiviral agents), notamment des inhibiteurs de la protéase virale [1, 14] (→).
(→) Voir la Synthèse de S. Pol, m/s novembre 2013, n° 11, page 998
Cependant, ces traitements sont très coûteux, souvent associés à d’importants effets secondaires, et ne suffisent donc pas à traiter les 170 millions de personnes chroniquement infectées par le VHC dans le monde. Par ailleurs, l’organisation mondiale de la santé (OMS) estime que près de 4 millions de nouvelles infections par le VHC surviennent chaque année dans le monde. Ce problème de santé publique n’est pas confiné aux pays en développement puisqu’on estime à environ 18 000 le nombre de nouvelles infections tous les ans aux États-Unis, soit une toutes les trente minutes [2]. Comme la plupart de ces nouvelles infections sont asymptomatiques, les personnes infectées ignorent le plus souvent qu’elles deviennent porteuses chroniques du virus. Elles ne sont donc pas prises en charge médicalement et sont par ailleurs susceptibles de transmettre le virus à des sujets sains. Si l’infection par le VHC n’est pas détectée lors d’un examen de médecine préventive, la maladie ne se révèle que plusieurs années après l’infection, bien souvent sous la forme d’une hépatite chronique active ayant induit des lésions hépatiques. À ce stade, les traitements antiviraux sont toutefois beaucoup moins efficaces. Pour toutes ces raisons, la mise au point d’un vaccin prophylactique contre le VHC est un enjeu majeur. Un tel vaccin représente le meilleur espoir de pouvoir contrôler l’épidémie à l’échelle mondiale, ainsi qu’une opportunité de diminuer considérablement les dépenses de santé liées aux traitements des infections chroniques par le VHC.
Les potentiels vaccins prophylactiques contre le VHC
L’infection par le VHC peut être spontanément résolutive chez certains sujets récemment contaminés, ainsi que chez le chimpanzé, la seule espèce animale pouvant être infectée expérimentalement par ce virus. Ce phénomène fournit des arguments solides pour le développement d’un vaccin préventif contre le VHC. Dans le même temps, la complexité de la mise au point d’un tel vaccin est soulignée par la persistance fréquente du virus en raison de sa capacité à muter pour échapper à l’immunité humorale et cellulaire [3]. Dans ce contexte, deux grands types de vaccins prophylactiques ont été proposés [4] : ceux basés sur l’induction d’une réponse humorale contre les protéines d’enveloppe du virus, destinée à neutraliser ce dernier ; et ceux visant à induire une réponse cellulaire contre la protéine de capside ou les protéines non structurales du virus, qui sont très conservées au sein des différents génotypes du VHC. Les réponses immunitaires déclenchées par ces deux types de vaccin sont ainsi complémentaires et ceux-ci pourraient d’ailleurs être associés pour obtenir une protection optimale. Évalués dans un modèle chimpanzé, ces vaccins ont donné des résultats intéressants, bien que ne protégeant pas complètement de l’infection expérimentale occasionnée chez les animaux immunisés [5]. Si dans certains cas ils empêchaient l’infection, ils pouvaient au moins, dans les autres cas, diminuer de façon importante la virémie et enrayer le développement d’une infection chronique. Deux candidats vaccins ayant généré des résultats prometteurs dans un modèle chimpanzé ont fait l’objet d’essais de phase I chez l’homme. Un premier vaccin, basé sur l’usage de protéines d’enveloppes recombinantes E1 et E2 du VHC purifiées, s’est avéré capable d’induire une bonne réponse humorale chez l’homme, permettant la neutralisation de différents génotypes du VHC in vitro [6]. Le second, basé sur l’injection de vecteurs adénoviraux exprimant les protéines non structurales du VHC, était capable d’induire une bonne réponse cellulaire multi-épitopique [7]. Ce dernier est actuellement en essai de phase II aux États-Unis pour évaluer la protection induite chez des toxicomanes utilisateurs de drogues par voie intraveineuse.
Les difficultés rencontrées lors de la mise au point d’un vaccin prophylactique basé sur les protéines d’enveloppe du VHC
Le concept d’un vaccin basé sur les protéines d’enveloppe E1 et E2 du VHC semble prometteur, mais un obstacle majeur entrave la poursuite de son développement. Ces deux protéines possèdent un domaine transmembranaire (DTM) qui les retient dans les compartiments intracellulaires, rendant leur extraction et leur purification incompatibles avec un développement industriel. Ces difficultés ont conduit à l’élaboration de stratégies alternatives basées sur l’utilisation de protéines E1 et/ou E2 tronquées, pouvant être sécrétées. Toutefois, ces approches ont rencontré un succès limité, puisque la suppression de leur DTM diminue considérablement leurs propriétés antigéniques et fonctionnelles [8]. Plus récemment, des particules rétrovirales murines pseudotypées pour les protéines d’enveloppe du VHC ont été proposées comme une nouvelle plate-forme de vaccination [9]. Ces particules appelées VHCpp (pour pseudo-particules) présentent les protéines E1 et E2 dans une conformation correcte et sont couramment utilisées comme modèle d’étude de l’entrée du VHC. Cependant, leur production à grande échelle s’avère complexe, et l’utilisation de particules rétrovirales animales pour le développement d’un vaccin prophylactique en médecine humaine nécessite une validation préalable. Encore plus récemment, une souche particulière du VHC (la souche JFH-1 de génotype 2a [10]), cultivée sur la lignée d’hépatocarcinome Huh7.5 et inactivée, a été proposée comme candidat vaccin [11]. Cependant, la production à grande échelle de ce virus en culture cellulaire (VHCcc) reste complexe, et la lignée Huh7.5 n’est pas approuvée pour une production de vaccins. Il sera par ailleurs difficile d’identifier une lignée cellulaire approuvée qui puisse exprimer les facteurs nécessaires à l’entrée, la réplication et l’assemblage du virus.
Le concept innovant des particules chimères d’enveloppe du VHB et du VHC
À la différence du VHC, il existe un vaccin très efficace contre le virus de l’hépatite B (VHB), fondé sur la propriété de sa protéine majeure d’enveloppe (la protéine S, pour surface, présentant quatre DTM) à s’auto-assembler en petites particules sous-virales non infectieuses (Figure 1). Ces particules, constituées d’une centaine de copies de la protéine S, sont très immunogènes et représentent la base du vaccin contre le VHB, utilisé avec succès depuis le début des années 1980. Plusieurs approches vaccinales originales visant à incorporer des épitopes hétérologues en positions amino- ou carboxy-terminales de la protéine S du VHB ont depuis été développées [12]. Le DTM des protéines E1 et E2 du VHC étant essentiel à leur conformation et leur immunogénicité, nous avons proposé récemment une stratégie innovante en élaborant des protéines d’enveloppe chimères pour lesquelles le DTM amino-terminal de la protéine S du VHB a été substitué par le DTM des protéines E1 ou E2 du VHC [13] (Figure 1). Exprimées dans la lignée CHO (chinese hamster ovary cells, une lignée approuvée pour les biomédicaments), ces protéines d’enveloppe chimères VHB-VHC sont co-assemblées avec la protéine sauvage S en particules sous-virales, qui sont efficacement sécrétées (Figure 1). Ces particules ressemblent à celles du vaccin contre le VHB et présentent l’avantage d’arborer les protéines d’enveloppe du VHC dans leur intégralité. Elles peuvent induire dans un modèle animal la production d’anticorps qui neutralisent in vitro différents génotypes du VHC. En effet, bien que les particules utilisées lors des premiers essais d’immunisation contenaient une enveloppe de VHC de génotype 1a, tous les génotypes testés ont été neutralisés par les anticorps induits, même si cette neutralisation se faisait de manière plus efficace pour les génotypes 1a et 1b que pour les génotypes 2a et 3a, plus distants génétiquement [13]. Par ailleurs, ces particules chimères induisent une réponse équivalente à celle induite par un vaccin commercial contre le VHB, renforçant ainsi l’idée que de telles particules vaccinales puissent se substituer aux vaccins contre le VHB, avec l’avantage de pouvoir aussi protéger contre le VHC. Ces particules présentent également l’avantage de pouvoir être produites selon les procédures établies pour le vaccin contre le VHB, ce qui réduirait les délais et coûts de développement industriel. Tous ces résultats obtenus en modèle animal nécessitent d’être confirmés chez l’homme, mais indiquent néanmoins que la mise au point d’un vaccin « bivalent », qui protégerait de l’infection par ces deux agents majeurs des hépatites virales humaines, représente une éventualité crédible.
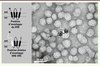 |
Figure 1. Principe des particules chimères d’enveloppe VHB-VHC. La protéine d’enveloppe S (pour surface) du virus de l’hépatite B (VHB) est une protéine qui présente quatre domaines transmembranaires (DTM). Exprimée dans une cellule eucaryote, cette protéine est capable de s’auto-assembler en particules sous-virales d’environ 25 nm de diamètre composées d’une centaine de copies de S. Les extrémités amino-terminales et carboxy-terminales de S ainsi qu’une boucle antigénique sont exposées à la surface des particules. Ces particules sous virales sont très immunogènes et constituent la base du vaccin contre le VHB. Les deux protéines d’enveloppe E1 et E2 du virus de l’hépatite C (VHC) présentent un seul DTM qui est essentiel à leur conformation et leur immunogénicité. Des protéines chimères, dans lesquelles le DTM amino-terminal de S est substitué par celui des protéines E1 ou E2, sont capables de s’auto-assembler avec la protéine sauvage S en particules chimères d’enveloppe incorporant E1 ou E2 dans leur intégralité [13]. |
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Nos travaux sur le développement d’un vaccin bivalent VHB-VHC ont été soutenus par l’Institut Mérieux, le programme FEDER (Fonds européens de développement régional) et le Cluster de recherche en infectiologie de la région centre. Ils sont soutenus actuellement par l’ANR (grant Emergence Hepatibivax) et l’ANRS.
Références
- Sarrazin C, Hézode C, Zeuzem S, Pawlotsky JM. Antiviral strategies in hepatitis C virus infection. J Hepatol 2012 ; 56 : S88–100. [CrossRef] [PubMed] [Google Scholar]
- Edlin BR. Perspective: test and treat this silent killer. Nature 2011 ; 474 : S18–S19. [CrossRef] [PubMed] [Google Scholar]
- Rehermann B. Hepatitis C virus versus innate and adaptive immune responses: a tale of coevolution and coexistence. J Clin Invest 2009 ; 119 : 1745–1754. [CrossRef] [PubMed] [Google Scholar]
- Houghton M. Prospects for prophylactic and therapeutic vaccines against the hepatitis C viruses. Immunol Rev 2011 ; 239 : 99–108. [CrossRef] [PubMed] [Google Scholar]
- Dahari H, Feinstone SM, Major ME. Meta-analysis of hepatitis C virus vaccine efficacy in chimpanzees indicates an importance for structural proteins. Gastroenterology 2010 ; 139 : 965–974. [CrossRef] [PubMed] [Google Scholar]
- Stamataki Z, Coates S, Abrignani S, Houghton M, McKeating JA. Immunization of human volunteers with hepatitis C virus envelope glycoproteins elicits antibodies that cross-neutralize heterologous virus strains. J Infect Dis 2011 ; 204 : 811–813. [CrossRef] [PubMed] [Google Scholar]
- Barnes E, Folgori A, Capone S, et al. Novel adenovirus-based vaccines induce broad and sustained T cell responses to HCV in man. Sci Transl Med 2012 ; 4 : 115ra1. [CrossRef] [PubMed] [Google Scholar]
- Sominskaya I, Alekseeva E, Skrastina D, et al. Signal sequences modulate the immunogenic performance of human hepatitis C virus E2 gene. Mol Immunol 2006 ; 43 : 1941–1952. [CrossRef] [PubMed] [Google Scholar]
- Garrone P, Fluckiger AC, Mangeot PE, et al. A prime-boost strategy using virus-like particles pseudotyped for HCV proteins triggers broadly neutralizing antibodies in macaques. Sci Transl Med 2011 ; 3 : 94ra71. [CrossRef] [PubMed] [Google Scholar]
- Legrand-Abravanel F, Izopet J. Culture du virus de l’hépatite C, enfin ! Med Sci (Paris) 2007 ; 23 : 588–589. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Akazawa D, Moriyama M, Yokokawa H, et al. Neutralizing antibodies induced by cell culture-derived hepatitis C virus protect against infection in mice. Gastroenterology 2013 ; 145 : 447–455. [CrossRef] [PubMed] [Google Scholar]
- Phogat S, Svehla K, Tang M, et al. Analysis of the human immunodeficiency virus type 1 gp41 membrane proximal external region arrayed on hepatitis B surface antigen particles. Virology 2008 ; 373 : 72–84. [CrossRef] [PubMed] [Google Scholar]
- Beaumont E, Patient R, Hourioux C, et al. Chimeric hepatitis B virus/hepatitis C virus envelope proteins elicit broadly neutralizing antibodies and constitute a potential bivalent prophylactic vaccine. Hepatology 2013 ; 57 : 1303–1313. [CrossRef] [PubMed] [Google Scholar]
- Pol S. Virus de l’hépatite C : 25 ans, la fin de l’histoire ? Med Sci (Paris) 2013 ; 29 : 998–1003. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
© 2014 médecine/sciences – Inserm
Liste des figures
 |
Figure 1. Principe des particules chimères d’enveloppe VHB-VHC. La protéine d’enveloppe S (pour surface) du virus de l’hépatite B (VHB) est une protéine qui présente quatre domaines transmembranaires (DTM). Exprimée dans une cellule eucaryote, cette protéine est capable de s’auto-assembler en particules sous-virales d’environ 25 nm de diamètre composées d’une centaine de copies de S. Les extrémités amino-terminales et carboxy-terminales de S ainsi qu’une boucle antigénique sont exposées à la surface des particules. Ces particules sous virales sont très immunogènes et constituent la base du vaccin contre le VHB. Les deux protéines d’enveloppe E1 et E2 du virus de l’hépatite C (VHC) présentent un seul DTM qui est essentiel à leur conformation et leur immunogénicité. Des protéines chimères, dans lesquelles le DTM amino-terminal de S est substitué par celui des protéines E1 ou E2, sont capables de s’auto-assembler avec la protéine sauvage S en particules chimères d’enveloppe incorporant E1 ou E2 dans leur intégralité [13]. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




