| Issue |
Med Sci (Paris)
Volume 29, Number 1, Janvier 2013
|
|
|---|---|---|
| Page(s) | 22 - 25 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2013291007 | |
| Published online | 25 janvier 2013 | |
Vers un vaccin universel contre la grippe ?
Towards a universal vaccine against flu?
Départment de biologie moléculaire, The Scripps research institute, 10550 North Torrey Pines Road, La Jolla, CA 92037, États-Unis
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Le virus de la grippe (influenza virus) est responsable d’infections du système respiratoire chez l’homme causant le décès de plus de 250 000 patients lors des épidémies saisonnières et dont le coût annuel est estimé à plusieurs milliards d’euros [1]. Tous les 10 à 50 ans, des pandémies émergent. Au cours du siècle dernier, la « grippe espagnole » (virus H1N1) de 1918 et les autres pandémies de 1957 (H2N2), 1968 (H3N2) et 2009 (H1N1) ont fait entre 50 et 100 millions de victimes dans le monde.
La diversité génétique des virus de la grippe, un frein au développement d’un vaccin universel
La grippe est causée par des virus à ARN de trois genres différents appartenant à la famille des Orthomyxoviridae, désignés par les types A, B et C. Les virus de type A sont responsables des pandémies du siècle dernier, les virus de types A et B sont impliqués dans les épidémies saisonnières. Les virus de type C ne causent, le plus souvent, qu’une infection modérée, et ne sont pas associés à des épidémies. Par conséquent, le développement de stratégies thérapeutiques pour combattre les infections par les virus influenza A et B représente un enjeu majeur.
Un des principaux freins au développement d’un vaccin universel contre la grippe est la capacité du virus à modifier son profil antigénique en mutant les gènes codant pour ses glycoprotéines de surface, cibles des anticorps, ce qui lui permet ainsi d’échapper au système immunitaire de l’hôte. Cette stratégie de diversification génétique est partagée également par d’autres types de virus, tels que le VIH (virus de l’immunodéficience humaines) et le virus de l’hépatite B [1]. Cependant, en dépit de l’hypervariabilité dans la séquence primaire de ces antigènes de surface, des contraintes fonctionnelles peuvent sévèrement restreindre la variabilité du virus au niveau de régions clefs. Ces régions, nécessaires à l’infection de la cellule hôte par le virus, représentent des cibles de reconnaissance pour les anticorps neutralisants.
Au cours de la dernière décennie, beaucoup d’efforts ont été déployés afin d’isoler et de caractériser des anticorps capables de neutraliser différents sous-types de virus influenza A (bnAb, broadly neutralizing antibodies) [2–6]. Nos travaux, publiés récemment dans Science et fruits d’une collaboration entre le Wilson laboratory du Scripps research institute, le Crucell vaccine Institute et l’université de Hong Kong [3], identifient plusieurs anticorps capables de neutraliser différents sous-types de virus de la grippe B. Parmi ceux-ci, CR9114 est capable de neutraliser les virus de la grippe A et de la grippe B. L’isolement et la caractérisation structurale de tels anticorps complexés à l’hémagglutinine, le principal antigène de surface du virus, ouvrent de nouvelles perspectives pour le développement d’un vaccin universel et de nouveaux antiviraux pour le traitement de la grippe.
L’hémagglutinine : cible des anticorps neutralisants
Les virus influenza A sont divisés en sous-types en fonction des propriétés antigéniques de leurs glycoprotéines de surface : l’hémagglutinine (HA) et la neuraminidase (d’où leur dénomination familière HxNx). Les HA sont elles-mêmes divisées en deux groupes majeurs, rassemblant au total 17 HA (Figure 1A). Les virus influenza B ne ségrègent pas en sous-types, mais leur évolution est caractérisée par la cocirculation de deux lignées possédant des caractéristiques génétiques et antigéniques différentes (Figure 1B) [7]. L’HA, une glycoprotéine antigénique présente à la surface du virus de la grippe, est nécessaire à l’attachement du virus aux acides sialiques présents à la surface de la cellule cible, ainsi qu’à la fusion de la membrane virale et de la membrane cellulaire après endocytose (Figure 2). L’HA est la cible principale des anticorps et constitue donc une composante clef pour la production d’un vaccin contre la grippe. Aujourd’hui, les vaccins saisonniers sont composés des souches dominantes des sous-types H1 et H3 du virus influenza A et de la souche dominante du virus influenza B en circulation, et permettent d’induire une réponse immunitaire efficace contre les épidémies saisonnières. Cependant, les constantes mutations - antigenic drift - des virus en circulation nécessitent le renouvellement des vaccins tous les ans. Dans le cas d’une pandémie, la production d’un vaccin prendrait plusieurs mois à partir de l’émergence du virus. De ce fait, des stratégies de prévention ou de traitement permettant de couvrir un large spectre de souches représentent un véritable enjeu.
 |
Figure 1. Variabilité génétique de l’hémagglutinine. A. Arbre phylogénétique représentant les relations entre les 17 sous-types d’HA du virus influenza A. Les sous-types encerclés sont reconnus ou neutralisés par CR9114. Les astérisques marquent les sous-types capables d’infecter les humains. n.t. : sous-types non testés. B. Dendrogramme représentant l’ensemble des séquences d’HA du virus influenza B disponibles dans la base de donnée du centre national pour l’information biotechnologique sur la grippe [14]. Les noms de l’ensemble des virus testés lors de notre étude sont indiqués (adapté de [3]). |
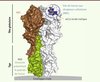 |
Figure 2. Structure tridimensionnelle de l’hémagglutinine. Structure de l’HA (pdb 3GBN), la glycoprotéine de surface majeure du virus de la grippe. L’HA est une protéine homotrimérique synthétisée sous la forme d’un précurseur HA0. Pour être fonctionnelle, l’HA est ensuite clivée par protéolyse en deux sous-unités HA1 (marron) et HA2 (vert), ce qui libère le peptide de fusion du côté de l’extrémité amino-terminale de HA2. L’HA peut être divisée en deux parties : une partie proche de la membrane (tige) et une partie distante (tête globulaire). HA1 contient le site de liaison aux récepteurs des cellules cibles (RBS) représenté en bleue. Un α2,6 acide sialique est représenté au niveau du RBS. HA2 contient le domaine nécessaire à la fusion des membranes virale et cellulaire. Sous l’effet du pH acide de l’endosome, l’HA subit un changement conformationnel important et irréversible qui est essentiel à la fusion des deux membranes. |
Anticorps neutralisant le virus grippal
Différentes équipes de recherche, dont la nôtre, ont récemment décrit des anticorps monoclonaux humains capables de neutraliser différents sous-types du groupe 1 et/ou du groupe 2 des virus influenza A (Figure 1) [2, 4–6, 8]. Jusqu’à aujourd’hui, moins d’attention avait été portée aux virus influenza B, probablement parce qu’ils n’infectent pas les oiseaux aquatiques, réservoir clé pour l’émergence des pandémies. Cependant, tous les 2 à 4 ans, les virus influenza B sont les principaux responsables d’épidémies saisonnières et causent plus de victimes que les virus H1N1 saisonniers d’influenza A [9].
Dans notre équipe, afin d’identifier des anticorps monoclonaux capables de neutraliser les virus influenza B, nous avons construit - en utilisant la technique du phage display - une banque d’anticorps provenant de lymphocytes B issus de donneurs récemment vaccinés. Les phages recombinants étaient sélectionnés sur leurs capacités de liaison à des HA provenant de virus influenza A et B, puis à des HA provenant des deux lignées de virus influenza B. Deux immunoglobulines, CR8033 and CR8071, capables de reconnaître les HA des deux lignées d’influenza B, ainsi qu’un anticorps, CR9114, capable de se lier à l’ensemble des différentes HA des virus influenza A et B testés, ont ainsi été identifiés.
CR8033 et CR8071 neutralisent les virus influenza B
Les études structurales réalisées par cristallographie aux rayons X et par microscopie électronique nous ont permis d’identifier les épitopes reconnus par CR8033 et CR8071 (Figure 3). Ces deux anticorps reconnaissent des régions hautement conservées au niveau de la tête globulaire de l’HA. CR8033 se lie au niveau du site de liaison aux récepteurs, alors que CR8071 reconnaît un épitope à la base de la tête globulaire de l’HA (Figure 3). Afin d’évaluer l’efficacité de ces anticorps, nous avons inoculé chez des souris un virus représentatif de chacune des lignées du virus influenza B à des doses normalement létales. Ces tests révèlent que ces anticorps confèrent à ces souris une protection à la fois prophylactique et thérapeutique contre les virus influenza B.
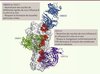 |
Figure 3. CR9114, CR8033 et CR8071 reconnaissent différentes épitopes à la surface de l’hémagglutinine. Les différents sites de vulnérabilité sont représentés en rouge. Chaque site est unique et reconnu par un anticorps différent. Les Fab (fragment antigen-binding) de CR9114, CR8071 CR8033 sont respectivement colorés en violet, vert et bleu. |
Alors que les anticorps reconnaissant la tête globulaire des virus influenza A neutralisent ces derniers en empêchant la fixation de l’HA aux acides sialiques de la cellule hôte, les deux anticorps que nous avons mis en évidence utilisent un autre mécanisme de neutralisation. En présence de CR8033 et CR8071, le virus est capable d’infecter la cellule et d’y répliquer son matériel génétique, mais sa propagation est bloquée. Nous avons donc testé la capacité de ces anticorps à bloquer la libération de nouvelles particules virales. De fait, ces anticorps empêchent la création de nouvelles particules virales lors du bourgeonnement à la surface des cellules hôtes. Ce mécanisme ressemble à celui du Zanamivir, un inhibiteur de la neuraminidase qui bloque la libération de nouvelles particules virales à la surface des cellules infectées [10].
CR9114 neutralise les virus influenza A et B
L’anticorps monoclonal CR9114 cible une région similaire à celle reconnue par les bnAb identifiés récemment (CR6261, F10 et FI6) [2, 4, 6]. Cette région hautement conservée se situe au niveau de la partie de l’HA proche de la membrane appelée stem1(Figure 3). Contrairement aux précédents anticorps, CR9114 reconnaît un épitope conservé non seulement chez tous les virus influenza A, mais aussi chez les virus influenza B. L’analyse des déterminants moléculaires de l’interaction entre CR9114 et l’HA nous a révélé comment, via son mode de liaison, CR9114 est capable de neutraliser une telle diversité de virus [3].
Les anticorps reconnaissant cette région de l’HA neutralisent le virus par un mécanisme nouveau, en bloquant le changement conformationnel de l’HA nécessaire à la fusion de la membrane virale avec celle de l’endosome durant le processus d’entrée du virus. Des tests in vitro de microneutralisation réalisés avec CR9114 sur des virus influenza A nous ont permis de confirmer ce mécanisme. En revanche, ce mécanisme n’a pas pu être détecté chez les virus influenza B. De récentes études ayant montré l’importance des fonctions effectrices des anticorps [2, 11], nous avons testé la capacité de CR9114 à protéger des souris contre des doses létales de différents virus influenza A et B. Pour toutes les souches testées, CR9114 confère aux souris une résistance vis-à-vis des virus. Ces résultats confirment l’importance des fonctions effectrices des anticorps, lesquelles avaient peut-être été jusqu’alors sous-estimées. Ils indiquent aussi que la neutralisation in vitro n’est pas prédictive de la neutralisation in vivo. Ces différences de neutralisation par CR9114 peuvent s’expliquer par la différence d’affinité de cet anticorps pour les différents HA.
Une future thérapie universelle contre la grippe ?
L’identification et la caractérisation d’anticorps monoclonaux capables de neutraliser l’ensemble des virus influenza B nous rapprochent d’une thérapie universelle contre la grippe. En particulier, un vaccin capable d’induire la production d’anticorps ciblant le même épitope que CR9114 pourrait permettre une protection à long terme contre la plupart des virus influenza A et B.
L’enjeu consiste maintenant à tirer parti de l’incroyable quantité d’informations disponibles sur les anticorps neutralisants pour développer et améliorer les thérapies vaccinales contre la grippe. À court terme, les anticorps eux-mêmes peuvent être utilisés dans une approche d’immunothérapie passive. L’étude structurale des sites de vulnérabilité du virus et des sites d’interactions antigène-anticorps fournit des informations clés pour le développement de molécules antivirales et la conception de petites molécules thérapeutiques. Par exemple, des protéines telles que HB36 et HB80 [12, 13], qui imitent les interactions de l’anticorps CR6261 avec son épitope, ont récemment été développées. Ces protéines sont capables de reconnaître différentes HA et représentent une stratégie alternative aux thérapies à base d’anticorps.
Les travaux récemment présentés par notre équipe montrent que, bien que loin d’être atteinte, la production d’un vaccin universel contre la grippe n’est peut-être plus un fantasme. L’identification et la caractérisation d’anticorps neutralisant un large spectre d’HA sont une première étape. Les difficultés consistent maintenant à développer des stratégies permettant de stimuler les cellules B produisant des anticorps similaires à CR9114 et d’orienter la neutralisation, non pas vers les régions immunodominantes de l’HA, mais vers celles hautement conservées, qui représentent le talon d’Achille dans la défense du virus.
Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Stem (en français tige) correspond à la partie basale de l’hémagglutinine proche de la membrane et située sous la tête globulaire.
Références
- Burton DR, Poignard P, Stanfield RL, Wilson IA. Broadly neutralizing antibodies present new prospects to counter highly antigenically diverse viruses. Science 2012 ; 337 : 183–186. [CrossRef] [PubMed] [Google Scholar]
- Corti D, Voss J, Gamblin ST, et al. A neutralizing antibody selected from plasma cells that binds to group 1 and group 2 influenza A hemagglutinins. Science 2011 ; 333 : 850–856. [CrossRef] [PubMed] [Google Scholar]
- Dreyfus C, Laursen NS, Kwaks T, et al. Highly conserved protective epitopes on influenza B viruses. Science 2012 ; 337 : 1343–1348. [CrossRef] [PubMed] [Google Scholar]
- Ekiert DC, Bhabha G, Elsliger MA, et al. Antibody recognition of a highly conserved influenza virus epitope. Science 2009 ; 324 : 246–251. [CrossRef] [PubMed] [Google Scholar]
- Ekiert DC, Friesen RH, Bhabha G, et al. A highly conserved neutralizing epitope on group 2 influenza A viruses. Science 2011 ; 333 : 843–850. [CrossRef] [PubMed] [Google Scholar]
- Sui J, Hwang WC, Perez S, et al. Structural and functional bases for broad-spectrum neutralization of avian and human influenza A viruses. Nat Struct Biol 2009 ; 16 : 265–273. [CrossRef] [Google Scholar]
- McCullers JA, Saito T, Iverson AR. Multiple genotypes of influenza B virus circulated between 1979 and 2003. J Virol 2004 ; 78 : 12817–12828. [CrossRef] [PubMed] [Google Scholar]
- Throsby M, van den Brink E, Jongeneelen M, et al. Heterosubtypic neutralizing monoclonal antibodies cross-protective against H5N1, H1N1 recovered from human IgM+ memory B cells. PLoS One 2008 ; 3 : e3942. [CrossRef] [PubMed] [Google Scholar]
- Thompson WW, Shay DK, Weintraub E, et al. Influenza-associated hospitalizations in the United States. JAMA 2004 ; 292 : 1333–1340. [CrossRef] [PubMed] [Google Scholar]
- Gubareva LV, Kaiser L, Hayden FG. Influenza virus neuraminidase inhibitors. Lancet 2000 ; 355 : 827–835. [CrossRef] [PubMed] [Google Scholar]
- Hessell AJ, Hangartner L, Hunter M, et al. Fc receptor but not complement binding is important in antibody protection against HIV. Nature 2007 ; 449 : 101–104. [CrossRef] [PubMed] [Google Scholar]
- Fleishman SJ, Whitehead TA, Ekiert DC, et al. Computational design of proteins targeting the conserved stem region of influenza hemagglutinin. Science 2011 ; 332 : 816–821. [CrossRef] [PubMed] [Google Scholar]
- Whitehead TA, Chevalier A, Song Y, et al. Optimization of affinity, specificity and function of designed influenza inhibitors using deep sequencing. Nat Biotechnol 2012 ; 30 : 543–548. [CrossRef] [PubMed] [Google Scholar]
- Bao Y, Bolotov P, Dernovoy D, et al. The influenza virus resource at the National Center for Biotechnology Information. J Virol 2008 ; 82 : 596–601. [CrossRef] [PubMed] [Google Scholar]
© 2013 médecine/sciences – Inserm / SRMS
Liste des figures
 |
Figure 1. Variabilité génétique de l’hémagglutinine. A. Arbre phylogénétique représentant les relations entre les 17 sous-types d’HA du virus influenza A. Les sous-types encerclés sont reconnus ou neutralisés par CR9114. Les astérisques marquent les sous-types capables d’infecter les humains. n.t. : sous-types non testés. B. Dendrogramme représentant l’ensemble des séquences d’HA du virus influenza B disponibles dans la base de donnée du centre national pour l’information biotechnologique sur la grippe [14]. Les noms de l’ensemble des virus testés lors de notre étude sont indiqués (adapté de [3]). |
| Dans le texte | |
 |
Figure 2. Structure tridimensionnelle de l’hémagglutinine. Structure de l’HA (pdb 3GBN), la glycoprotéine de surface majeure du virus de la grippe. L’HA est une protéine homotrimérique synthétisée sous la forme d’un précurseur HA0. Pour être fonctionnelle, l’HA est ensuite clivée par protéolyse en deux sous-unités HA1 (marron) et HA2 (vert), ce qui libère le peptide de fusion du côté de l’extrémité amino-terminale de HA2. L’HA peut être divisée en deux parties : une partie proche de la membrane (tige) et une partie distante (tête globulaire). HA1 contient le site de liaison aux récepteurs des cellules cibles (RBS) représenté en bleue. Un α2,6 acide sialique est représenté au niveau du RBS. HA2 contient le domaine nécessaire à la fusion des membranes virale et cellulaire. Sous l’effet du pH acide de l’endosome, l’HA subit un changement conformationnel important et irréversible qui est essentiel à la fusion des deux membranes. |
| Dans le texte | |
 |
Figure 3. CR9114, CR8033 et CR8071 reconnaissent différentes épitopes à la surface de l’hémagglutinine. Les différents sites de vulnérabilité sont représentés en rouge. Chaque site est unique et reconnu par un anticorps différent. Les Fab (fragment antigen-binding) de CR9114, CR8071 CR8033 sont respectivement colorés en violet, vert et bleu. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




