| Issue |
Med Sci (Paris)
Volume 27, Number 5, Mai 2011
|
|
|---|---|---|
| Page(s) | 458 - 460 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2011275004 | |
| Published online | 25 May 2011 | |
Myotubularine et desmine
Un complexe au service de la dynamique mitochondriale dans le muscle squelettique
The myotubularin-desmin complex regulates mitochondria dynamics
IGBMC, Inserm U964, UMR7104 CNRS, Université de Strasbourg, 1, rue Laurent Fries, 67404 Illkirch, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
**
This email address is being protected from spambots. You need JavaScript enabled to view it.
Les myopathies centronucléaires (CNM) regroupent des myopathies rares caractérisées par une faiblesse musculaire généralisée et le positionnement anormal d’organites comme les noyaux dans les muscles squelettiques [1]. La forme liée au chromosome X, aussi appelée myopathie myotubulaire (XLCNM, X-linked centronuclear myopathy), se manifeste par une hypotonie sévère à la naissance, entraînant souvent le décès du patient dans la première année. Cette forme est attribuée à des mutations du gène MTM1 codant pour la myotubularine [1]. Deux autres formes de myopathies centronucléaires autosomiques ont été décrites : l’une à transmission dominante (ADCNM) et l’autre à transmission récessive (ARCNM), attribuées à des mutations dans le gène DNM2 codant pour la GTPase dynamine 2 [2] et dans le gène BIN1 (amphiphysine 2), respectivement [1, 3, 4]. En général, le phénotype des patients atteints de la forme XLCNM est plus sévère.
La myotubularine (MTM1) partage des homologies de séquence avec la famille des protéines tyrosine phosphatases mais son activité enzymatique s’exerce sur une classe de lipides membranaires, les phosphoinositides (PI) [3]. Ces seconds messagers sont impliqués dans plusieurs processus cellulaires comme le trafic des membranes internes et le remodelage du cytosquelette d’actine [5]. La famille des myotubularines comporte 14 membres (MTM1, MTMR1-13, myotubularin-related proteins) et est subdivisée en 2 sous-groupes : les myotubularines enzymatiquement actives (MTM1, MTMR1-4, R6-8) et inactives (MTMR5, MTMR9-13) [6].
Les connaissances sur le rôle cellulaire de MTM1 se limitent à son implication dans la voie de l’endocytose où elle agit sur le métabolisme des phosphoinositides [3]. Cependant, sa fonction dans le muscle n’a pas encore été élucidée. Afin de comprendre comment l’absence de cette protéine provoque des défauts d’organisation intracellulaire spécifiquement dans le muscle squelettique, nous avons entrepris l’identification de ses partenaires.
La desmine : un nouveau partenaire musculaire de MTM1
Par une approche de double hybride dans la levure, nous avons identifié la desmine comme un ligand potentiel de MTM1 [7]. Cette protéine appartient à la famille des filaments intermédiaires. La desmine participe à la maturation de la cellule musculaire mais aussi à la préservation de l’architecture intracellulaire de la fibre adulte [8, 9]. De plus, elle est impliquée dans plusieurs types de myopathies et cardiomyopathies appelées les desminopathies, qui touchent le muscle squelettique (DRM, desmin related myopathies) et cardiaque (DRCM, desmin related cardiomyopathies) [10, 11]. Nous avons confirmé l’interaction entre MTM1 et la desmine in vitro et in vivo dans des modèles cellulaires, à partir de muscle squelettique de souris et de muscle humain. Ces expériences ont aussi permis d’identifier les acides aminés directement impliqués dans l’interaction. De plus, des mutations ponctuelles dans MTM1 (décrites chez des patients XLCNM), ou bien des mutations touchant la desmine (décrites chez des patients DRM) affectent l’interaction entre les deux protéines. Ces résultats suggèrent l’existence d’un lien moléculaire et physiopathologique entre ces deux formes de myopathies (XLCNM et DRM). En effet, nous avons observé la présence d’agrégats de filaments de desmine dans les muscles de souris dépourvues de MTM1 (souris knock out [KO] MTM1) et dans les muscles et cellules musculaires de patients XLCNM (Figure 1). Ces agrégats représentent un marqueur caractéristique du muscle des patients DRM [12]. La plupart des mutations touchant la desmine interfèrent avec la structure des filaments de desmine, ce qui se traduit par la formation d’agrégats de la protéine sous forme de dépôts granulo-filamentaires [12]. Alors que les défauts de la desmine se répercutent sur les deux types de muscle, squelettique et cardiaque, des anomalies du muscle cardiaque sont absentes chez les patients XLCNM [13]. En accord avec ces données cliniques, nous avons montré que MTM1 n’interagit pas avec la desmine dans le muscle cardiaque. De plus, des analyses biochimiques et phénotypiques ont révélé qu’il n’y a pas de signe d’atrophie cardiaque ni de marqueurs de cardiomyopathie chez la souris modèle KO MTM1 [7]. Nous avons conclu que MTM1 contrôle la formation et/ou la stabilité des filaments de desmine spécifiquement dans le muscle squelettique.
 |
Figure 1. Défaut de localisation de la desmine dans les cellules musculaires (myotubes) de patients XLCNM. Immunomarquage de la desmine : des filaments de desmine sont présents dans les cellules contrôles alors que des agrégats de desmine sont visibles dans les cellules de patients XLCNM (têtes de flèches) (mutations MTM1 F238fs et R241C). |
L’action de MTM1 sur l’assemblage des filaments de desmine est indépendante de son activité enzymatique
Les observations sur le muscle et les cellules issues de patients XLCNM nous ont conduits à analyser plus en détail l’effet de MTM1 sur les filaments de desmine. Nous avons testé in vitro l’impact de l’addition de la protéine MTM1 recombinante sur la formation des filaments de desmine et l’effet de la desmine sur l’activité phosphatase de MTM1. MTM1 affecte la formation des filaments de desmine en agissant sur leur morphologie et l’équilibre entre les formes monomérique et multimérique (forme après assemblage en filament). Ces observations sont confirmées par des analyses ex vivo sur des cellules musculaires primaires issues de la souris KO MTM1 montrant que cet équilibre y est aussi affecté, ce qui expliquerait l’apparition d’agrégats de desmine dans le muscle déficient en MTM1 [7]. Ce défaut n’est pas lié à une phosphorylation accrue de la desmine (qui pourrait provoquer une agrégation des filaments), ce qui rend improbable l’implication directe ou indirecte de MTM1 dans la phosphorylation de la desmine. De plus, l’activité phosphatase de MTM1 vis-à-vis de ses substrats lipidiques n’est pas affectée par la desmine. La régulation du cytosquelette de desmine par MTM1 est le premier exemple d’une fonction de MTM1 indépendante de son activité enzymatique.
Dynamique mitochondriale régulée par MTM1 et le complexe MTM1-desmine
Une des particularités morphologiques des desminopathies est un défaut de la fonction et de la morphologie mitochondriales [12, 14]. L’analyse histologique de biopsies de patients XLCNM a aussi révélé des défauts de l’emplacement des mitochondries et de l’activité des enzymes mitochondriales [15, 16]. Nous avons donc étudié le lien entre le complexe MTM1-desmine et la dynamique mitochondriale. Les résultats obtenus montrent que MTM1 est capable d’agir sur la distribution et la mobilité des mitochondries dans les cellules musculaires, via son lien avec la desmine. En effet, des mutations de MTM1 qui abolissent la liaison à la desmine ou/et l’absence de MTM1 induisent une agrégation des filaments de desmine ainsi qu’une accumulation anormale des mitochondries autour du noyau (Figure 2). Ces défauts se traduisent aussi par une diminution de la vitesse de déplacement des mitochondries dans la zone périnucléaire. La perte de l’interaction entre MTM1 et la desmine provoque aussi des défauts ultrastructuraux de la morphologie des mitochondries affectant la compartimentalisation de leurs structures internes (anomalies de la double membrane et des crêtes) [17]. Ces mitochondries semblent gonflées avec une accumulation de plusieurs couches de membranes. Ces dernières observations suggèrent un lien direct entre le complexe MTM1-desmine et la mitochondrie. Ceci est confirmé par un fractionnement subcellulaire à partir du muscle de souris, révélant que ce complexe est associé à la mitochondrie. De plus, la fonction mitochondriale établie à partir de l’activité cytochrome C oxydase et de la quantité d’ATP libéré est diminuée dans les cellules musculaires issues des patients XLCNM. Cependant aucun signe d’apoptose ou de prédisposition à l’apoptose n’a été retrouvé dans ces cellules [18]. En parallèle de ces analyses, nous avons montré que certaines mutations de MTM1 qui ne provoquaient pas de dissociation du complexe MTM1-desmine, affectent la dynamique des mitochondries. Ainsi MTM1 régulerait la dynamique et la fonction mitochondriales par deux voies, la première agissant via la régulation des filaments de desmine. La seconde voie semble indépendante de la desmine et son mécanisme reste encore à élucider.
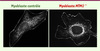 |
Figure 2. Désorganisation des mitochondries dans des cellules musculaires déficientes en MTM1. L’absence de MTM1 provoque une accumulation des mitochondries dans le compartiment périnucléaire. |
En conclusion, cette étude a identifié un partenariat inattendu entre deux protéines impliquées dans des pathologies musculaires différentes [7]. Ce lien met en évidence un mécanisme physiopathologique commun entre les myopathies centronucléaires et les desminopathies, et souligne l’importance du complexe MTM1-desmine dans la régulation de la dynamique mitochondriale dans le muscle squelettique. Ce travail ouvre aussi de nouvelles perspectives sur la compréhension de la spécificité tissulaire et la fonction des protéines se liant aux filaments intermédiaires (Figure 3).
 |
Figure 3. Implication des partenaires de la desmine dans la dynamique et la fonction mitochondriales. La myotubularine MTM1 est un partenaire nouvellement identifié de la desmine; la plectine est une protéine qui fait le lien entre les éléments du cytosquelette et est impliquée dans l’épidermolyse bulleuse associée à une dystrophie musculaire (EB-MD); et l’alphaB-crystalline une protéine du stress thermique mutée dans les desminopathies liées à l’alphaB-crystalline. Ce diagramme souligne aussi les spécificités tissulaires des interactions entre la desmine et ses partenaires. |
Conflit d’intérêts
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
Remerciements
Les auteurs tiennent à remercier Jean-Louis Mandel pour son aide tout au long de l’étude. Ces travaux ont été soutenus par le Collège de France, l’Agence nationale pour la recherche (ANR), l’Association française contre les myopathies (AFM), la Fondation pour la recherche médicale (FRM) et le programme E-rare.
Références
- Jungbluth H, Wallgren-Pettersson C, Laporte J. Centronuclear (myotubular) myopathy. Orphanet J Rare Dis 2008 ; 3 : 26. [CrossRef] [PubMed] [Google Scholar]
- Bitoun M, Romero NB, Guicheney P. Des mutations de la dynamine 2 à l’origine de la forme dominante de la myopathie centronucléraire. Med Sci (Paris) 2006 ; 22 : 101-102. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Nicot AS, Laporte J. Endosomal phosphoinositides and human diseases. Traffic 2008 ; 9 : 1240-1249. [CrossRef] [PubMed] [Google Scholar]
- Toussaint A, Nicot AS, Mandel JL, Laporte J. Mutations de l’amphiphysine 2 (BIN1) dans les myopathies centronucléaires récessives. Med Sci (Paris) 2007 ; 23 : 1080-1082. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Vicinanza M, D’Angelo G, Di Campli A, De Matteis MA. Phosphoinositides as regulators of membrane trafficking in health and disease. Cell Mol Life Sci 2008 ; 65 : 2833-2841. [CrossRef] [PubMed] [Google Scholar]
- Laporte J, Bedez F, Bolino A, Mandel JL. Myotubularins, a large disease-associated family of cooperating catalytically active and inactive phosphoinositides phosphatases. Hum Mol Genet 2003 ; 12 : 285-292. [CrossRef] [Google Scholar]
- Hnia K, Tronchere H, Tomczak KK, et al. Myotubularin controls desmin intermediate filament architecture and mitochondrial dynamics in human and mouse skeletal muscle. J Clin Invest 2011 ; 121 : 70-85. [CrossRef] [PubMed] [Google Scholar]
- Goldfarb LG, Dalakas MC. Tragedy in a heartbeat: malfunctioning desmin causes skeletal and cardiac muscle disease. J Clin Invest 2009 ; 119 : 1806-1813. [CrossRef] [PubMed] [Google Scholar]
- Herrmann H, Strelkov SV, Burkhard P, Aebi U. Intermediate filaments: primary determinants of cell architecture and plasticity. J Clin Invest 2009 ; 119 : 1772-1783. [Google Scholar]
- Omary MB. IF-pathies: a broad spectrum of intermediate filament-associated diseases. J Clin Invest 2009 ; 119 : 1756-1762. [CrossRef] [PubMed] [Google Scholar]
- Vicart P, Caron A, Guicheney P, et al. A missense mutation in the alphaB-crystallin chaperone gene causes a desmin-related myopathy. Nat Genet 1998 ; 20 : 92-95. [CrossRef] [PubMed] [Google Scholar]
- Schroder R, Goudeau B, Simon MC, et al. On noxious desmin: functional effects of a novel heterozygous desmin insertion mutation on the extrasarcomeric desmin cytoskeleton and mitochondria. Hum Mol Genet 2003 ; 12 : 657-669. [CrossRef] [PubMed] [Google Scholar]
- Herman GE, Finegold M, Zhao W, et al. Medical complications in long-term survivors with X-linked myotubular myopathy. J Pediatr 1999 ; 134 : 206-214. [CrossRef] [PubMed] [Google Scholar]
- Kostareva A, Sjoberg G, Bruton J, et al. Mice expressing L345P mutant desmin exhibit morphological and functional changes of skeletal and cardiac mitochondria. J Muscle Res Cell Motil 2008 ; 29 : 25-36. [CrossRef] [PubMed] [Google Scholar]
- Bevilacqua JA, Bitoun M, Biancalana V, et al. Necklace fibers, a new histological marker of late-onset MTM1-related centronuclear myopathy. Acta Neuropathol 2009 ; 117 : 283-291. [CrossRef] [PubMed] [Google Scholar]
- Canal N, Comi GC, Comola M, et al. Centronuclear myopathy with unusual mitochondrial abnormalities. Clin Neuropathol 1985 ; 4 : 23-27. [PubMed] [Google Scholar]
- Sauvanet C, Arnauné-Pelloquin L, David C, et al. Dynamique et morphologie mitochondriales : acteurs, mécanismes et pertinence fonctionnelle. Med Sci (Paris) 2010 ; 26 : 823-829. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Castanier C, Arnoult D. La dynamique mitochondriale au cours de l’apoptose. Med Sci (Paris) 2010 ; 26 : 830-835. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
© 2011 médecine/sciences – Inserm / SRMS
Liste des figures
 |
Figure 1. Défaut de localisation de la desmine dans les cellules musculaires (myotubes) de patients XLCNM. Immunomarquage de la desmine : des filaments de desmine sont présents dans les cellules contrôles alors que des agrégats de desmine sont visibles dans les cellules de patients XLCNM (têtes de flèches) (mutations MTM1 F238fs et R241C). |
| Dans le texte | |
 |
Figure 2. Désorganisation des mitochondries dans des cellules musculaires déficientes en MTM1. L’absence de MTM1 provoque une accumulation des mitochondries dans le compartiment périnucléaire. |
| Dans le texte | |
 |
Figure 3. Implication des partenaires de la desmine dans la dynamique et la fonction mitochondriales. La myotubularine MTM1 est un partenaire nouvellement identifié de la desmine; la plectine est une protéine qui fait le lien entre les éléments du cytosquelette et est impliquée dans l’épidermolyse bulleuse associée à une dystrophie musculaire (EB-MD); et l’alphaB-crystalline une protéine du stress thermique mutée dans les desminopathies liées à l’alphaB-crystalline. Ce diagramme souligne aussi les spécificités tissulaires des interactions entre la desmine et ses partenaires. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




