| Issue |
Med Sci (Paris)
Volume 25, Number 12, Décembre 2009
Anticorps monoclonaux en thérapeutique
|
|
|---|---|---|
| Page(s) | 1149 - 1154 | |
| Section | III - Un futur en développement | |
| DOI | https://doi.org/10.1051/medsci/200925121149 | |
| Published online | 15 décembre 2009 | |
Transgenèse animale et humanisation des anticorps
Des souris pour des hommes
Transgenesis and humanization of murine antibodies
Université de Limoges, Laboratoire d’immunologie, Faculté de médecine, F-87025 Limoges, France
CNRS, UMR6101, Limoges, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
L’une des principales limitations de l’utilisation initiale des anticorps monoclonaux d’origine murine en thérapeutique était leur immunogénicité, entraînant leur neutralisation. Depuis, de nombreuses voies de recherche ont tenté avec succès de rapprocher les immunoglobulines (Ig) murines des anticorps humains et d’en améliorer ainsi l’efficacité et la tolérance chez l’homme. Deux grandes voies méthodologiques peuvent être utilisées : la biotechnologie, modifiant in vitro la séquence d’un anticorps animal, ou l’immunisation d’animaux dont le répertoire des gènes d’immunoglobulines a été préalablement humanisé. Dans ce dernier cas (objet de cette revue), des approches diverses ont permis de créer des souris transgéniques pour un nombre plus ou moins élevé de segments V humains permettant d’obtenir un répertoire diversifié d’anticorps complètement humains. D’autres stratégies aboutissent à des Acm chimériques, le répertoire murin des segments VDJ réarrangés étant conservé et ceuxci s’associant à une région constante de chaîne lourde humaine. Les souris transgéniques humanisées constituent aujourd’hui des outils directs et séduisants, ayant permis le développement d’un nombre important d’anticorps de forte affinité et de faible immunogénicité dont certains sont en phase d’essai clinique et d’autres déjà commercialisés.
Abstract
The properties of monoclonal antibodies explain why they are such a successful class of therapeutic molecules. However, pionneered initial antibodies were of murine origin and triggered an immune response which limited the therapeutic potential of the antibody and generated deleterious effects. Consequently, tremendous efforts have been developped to engineer these murine Ig by introducing human sequences in vitro, or in vivo by humanization of murine antibodies, leading to chimeric immunoglobulins, and more recently generation of fully human antibodies in transgenic mice with a more or less diversified V repertoire. These approaches have led to the development of an increasing number of these chimeric or humanized monoclonal antibodies entering pharmaceutical pipelines.
© 2009 médecine/sciences - Inserm / SRMS
Depuis l’établissement par Köhler et Milstein des méthodes de production d’hybridomes à partir des cellules B de rongeurs immunisés (→), les anticorps monoclonaux (Acm) constituent la référence en matière d’anticorps définis et de haute spécificité [1]. Les anticorps murins restent utilisables en thérapeutique humaine pour des traitements brefs, et l’anti-CD3 (muromonab) introduit en 1986 a été largement utilisé pour le conditionnement immunosuppresseur avant greffe d’organe (→). Immunogènes chez l’homme, ces anticorps animaux peuvent être neutralisés et/ou induire des réactions allergiques. Diverses voies ont donc été développées pour rapprocher les immunoglobulines (Ig) murines des anticorps humains et en améliorer l’efficacité et la tolérance chez l’homme. Cette « humanisation » peut être réalisée en retouchant in vitro la séquence d’un anticorps animal produit par biotechnologie (→), ou bien directement via l’immunisation d’animaux dont le répertoire des gènes d’immunoglobulines a été préalablement humanisé. De nombreux anticorps issus de tels animaux sont en phase d’essai clinique ou déjà commercialisés et apparaissent comme des molécules particulièrement sûres. L’intérêt de ces animaux est lié au large répertoire d’antigènes qu’ils peuvent reconnaître, y compris quand il s’agit d’antigènes humains. S’y ajoute la possibilité de dériver ainsi tant des anticorps monoclonaux que polyclonaux (ou des associations oligoclonales). À l’inverse, le développement des méthodes de production d’anticorps humains à partir de lymphocytes humains reste limité en termes de répertoire, notamment vis-à-vis des auto-antigènes.
(→) voir J.L. Teillaud, page 1010 ; R. Abès et al., page 1011
(→) voir B. Vanhove, page 1121
(→) voir A. Beck et al., page 1024
Répertoire diversifié d’anticorps humanisés et chimériques chez la souris
Alors que la transgenèse a pu être utilisée chez de grands mammifères tels que la chèvre pour la production abondante d’un anticorps de spécificité définie, le seul animal permettant à ce jour de reconstituer un répertoire diversifié d’anticorps humanisés est la souris. La première description de souris exprimant un répertoire restreint de gènes d’Ig humains date de 1989 [2]. L’utilisation de longs transgènes humains qui incluaient les séquences codant pour deux à cinq régions variables [capables de réarrangements V(D)J] et plusieurs gènes codant pour les régions constantes (capables de subir la commutation de classe) a ensuite été combinée à l’inactivation des gènes endogènes codant les immunoglobulines de souris [3–5]. Ces modèles ont permis d’obtenir des hybridomes producteurs d’anticorps humains spécifiques malgré un répertoire V assez restreint : en effet, une part notable de la diversité des anticorps provient de la diversité jonctionnelle puis de la maturation d’affinité par hypermutation somatique, part plus importante que celle que crée la diversité combinatoire des différents segments germinaux. Un nombre restreint de segments V induit cependant des lacunes du répertoire, en particulier contre des antigènes polysaccharides connus comme ciblés par des anticorps aux séquences germinales sans besoin d’hypermutation somatique [6].
En restant dans des fonds génétiques murins déficients pour les gènes d’Ig endogènes, des lignées transgéniques disposant d’un nombre plus élevé de segments V humains ont donc été générées. Ce qui améliore l’étendue du répertoire et permet la reconstitution de compartiments lymphocytaires B de taille plus proche de la normale [7, 8]. Ces lignées ont été produites tant par transgenèse classique que par fusion de cellules souches embryonnaires (ES) avec des protoplastes pour le transfert de chromosomes de levure porteurs de larges transgènes humains, ou encore par fusion de cellules ES avec des microcellules dérivées de fibroblastes humains et apportant un minichromosome humain. Des lignées de souris portant les locus IgH et Igκ (HuMAb mouse de Medarex), ou portant en plus le locus Igλ (Xenomouse d’ABgenix) ont notamment ainsi été créées. Des anticorps de haute affinité ont été obtenus à partir de ces lignées. [9–12].
Approches chimériques
Des approches chimériques ont également été réalisées en parallèle : des lignées murines ont été établies chez lesquelles les réarrangements des segments V, D et J endogènes (murins) sont respectés, mais où les segments VDJ réarrangés peuvent s’exprimer en association à une région constante de chaîne lourde humaine (Figure 1). Ainsi, Zou et Rajewsky ont-ils remplacé les exons codant la partie sécrétée de la chaîne lourde γ1 de l’IgG1 murine par des exons γ1 humains, substituant efficacement par des IgG1 humaines chimériques les réponses humorales IgG1 de ces animaux, tout en gardant le répertoire VDJ murin [13]. Enfin, l’approche chimérique peut maintenant bénéficier de la disponibilité d’animaux qui correspondent simplement à l’insertion d’un gène codant pour la région constante humaine γ1 ou α1 en aval des clusters V, D et JH du locus IgH de la souris. Ces animaux permettent donc d’obtenir, d’emblée après fusion, des hybridomes spécifiques d’un antigène et dont l’isotype est prédéfini, soit IgG1 soit IgA1, autorisant donc dès le stade des hybridomes initiaux les tests fonctionnels propres à l’isotype souhaité in fine (brevets Michel Cogné et al., 2005 ; Michel Cogné et al., 20081) (Figure 2).
 |
Figure 1. Transgènes d’immunoglobulines humaines introduits chez la souris. Les locus des chaînes lourdes μ, δ, γ, α et légères λ, κ, etc. sont représentés en configuration germinale. Les gènes introduits par insertion aléatoire dans le génome des souris transgéniques sont schématisés en précisant le nombre de segments V et de gènes constants inclus dans les transgènes. |
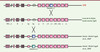 |
Figure 2. Séquences d’immunoglobulines humaines introduites dans le génome de la souris. Le locus des chaînes lourdes de la souris a été ciblé de façon à y introduire par recombinaison homologue des séquences provenant de régions constantes γ ou α des gènes d’immunoglobulines humains. |
Exemples d’anticorps thérapeutiques humanisés
Tous ces animaux mutants sont caractérisés par une maturation lymphocytaire B relativement normale en termes de taille des compartiments B, de réarrangements VDJ, de réarrangements de commutation de classe et d’hypermutation [14]. Ils ont ainsi permis de dériver un certain nombre d’anticorps de forte affinité et d’intérêt commercial important, reconnaissant aussi bien des petites molécules [15], des protéines spécifiques de pathogènes [16,17], des polysaccharides [18], des protéines humaines solubles et des cytokines comme l’interleukine-15 [19–21] ou membranaires comme l’antigène spécifique de prostate PSMA, le CD20, le CD30 ou le récepteur à l’EGF (epidermal growth factor) [22–24] et des antigènes associés à des tumeurs comme l’antigène carcinoembryonnaire [25].
Les premiers résultats à propos de tous ces Acm semblent très encourageants quant à leur faible immunogénicité chez l’homme (→). C’est le cas du panitumumab, anti-EGFR bloquant la liaison entre le ligand EGF et son récepteur (Abgenix/Amgen, Thousand Oaks, CA, USA). Les patients traités par le panitumumab ne développent pas d’anticorps polyclonaux contre l’anticorps thérapeutique [26] (→).
(→) voir P. Stas et I. Lasters, page 1070
(→) voir A. Beck et al., Tableau I, page 1026
Le denosumab est un autre anticorps apparemment très bien toléré [20] (Amgen, Thousand Oaks, CA, États-Unis). Il vise à combattre l’ostéoporose en ciblant le régulateur du remodelage osseux RANKL (receptor activator of NK-κB ligand). La faible variabilité de la pharmacocinétique entre patients semble indiquer l’absence de réponse immune contre le desomumab.
Même chez des patients porteurs de pathologies inflammatoires ou auto-immunes, la même absence de réponse immune a été observée vis-à-vis du zanolimumab [27] (Genmab, Copenhagen) qui lie le marqueur spécifique des lymphocytes T CD4 (avec un intérêt dans les lymphomes T et les pathologies auto-immunes). Même constat avec l’ipilimumab [28, 29] de Medarex (Princeton, NJ, USA) et Bristol-Myers Squibb (Wallingford, CT), qui en ciblant le récepteur inhibiteur CTLA-4 active les réponses immunes et est prescrit dans le mélanome. Globalement, les essais cliniques semblent donc indiquer une excellente tolérance de ces anticorps. Cette observation pourrait traduire une meilleure stabilité (des CDR3 et des paires H-L) des anticorps sélectionnés chez l’animal, alors corrélée à une moindre immunogénicité [30].
En revanche, d’autres Acm thérapeutiques, qu’ils soient chimériques ou humanisés par greffe des CDR (complementary determining regions), voire issus de séquences humaines via des librairies de phage display, ont pu se révéler occasionnellement immunogènes en clinique [Humira anti-TNF (tumor necrosis factor), anti-IL-12, etc.] [31]. Il convient d’ailleurs de noter que toute séquence V, même strictement humaine, peut être potentiellement immunogène chez l’homme et stimuler l’apparition d’anti-idiotypes(→).
(→) voir P. Stas et I. Lasters, page 1070
Une méthodologie d’avenir
Outre le fait qu’elle permet l’obtention d’anticorps stables et peu immunogènes, l’utilisation d’animaux transgéniques présente l’intérêt de produire des molécules qui possèdent d’emblée les fonctions effectrices souhaitées pour la molécule thérapeutique finale, et peuvent donc entrer rapidement dans des tests de screening fonctionnel. À l’inverse, les régions variables créées artificiellement ou par phage display nécessitent un processus plus long de greffe sur des régions effectrices avant de pouvoir être validées et de permettre le choix des anticorps les plus intéressants dans une application et dirigés contre une cible donnée.
L’obtention d’hybridomes peut aussi permettre - en n’utilisant qu’un seul système d’expression - d’aller de la caractérisation initiale d’un anticorps jusqu’à sa production industrielle. Cependant, même s’agissant d’hybridomes, l’étape de la production industrielle à long terme substituera souvent aux cellules d’hybridomes l’utilisation de transfectants stables via des vecteurs d’expression dans lesquels auront été clonées les séquences Ig d’intérêt (→).
(→) voir O. Cochet et M. Chartrain, page 1078 ; S. Olivier et M. Mehtali, page 1163
Pour des applications où il serait intéressant de mimer une réponse physiologique et de reconstituer l’équivalent d’un sérum polyclonal ou oligoclonal capable de neutraliser simultanément un grand nombre d’épitopes sur un antigène complexe, l’utilisation d’animaux transgéniques humanisés est également intéressante parce qu’elle permet d’obtenir rapidement une variété d’anticorps de mêmes fonctions effectrices et possédant des paratopes et des affinités variés.
Pour l’ensemble de ces raisons, dans l’arsenal des stratégies d’obtention d’anticorps d’intérêt thérapeutique, les souris transgéniques humanisées constituent aujourd’hui des outils directs et séduisants.
Conflit D’Intérêts
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
Cogné M, Sirac C, Bardel M, Decourt C, Laroche C, Brevet WO2005047333, 2005, « Mammifère non humain transgénique pour la région constante de la chaîne lourde des IgA humaines et ses applications (monoclonaux humanisés à destinée muqueuse) ».
Cogné M, Duchez S, Cogné N, Pinaud E, Brevet 08/00319, 2008, « Mammifère non humain transgénique pour la région constante de la chaîne lourde des immunoglobulines humaines de classe G et ses applications ».
Références
- Kohler G, Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity. Nature 1975; 256 : 495–7. [Google Scholar]
- Bruggemann M, Caskey HM, Teale C, et al. A repertoire of monoclonal antibodies with human heavy chains from transgenic mice. Proc Natl Acad Sci USA 1989; 86 : 6709–13. [Google Scholar]
- Lonberg N, Taylor LD, Harding FA, et al. Antigen-specific human antibodies from mice comprising four distinct genetic modifications. Nature 1994; 368 : 856–9. [Google Scholar]
- Green LL, Hardy MC, Maynard-Currie CE, et al. Antigen-specific human monoclonal antibodies from mice engineered with human Ig heavy and light chain YAC. Nat Genet 1994; 7 : 13–21. [Google Scholar]
- Taylor LD, Carmack CE, Huszar D, et al. Human immunoglobulin transgenes undergo rearrangement, somatic mutation and class switching in mice that lack endogenous IgM. Int Immunol 1994; 6 : 579–91. [Google Scholar]
- Adderson EE, Shackelford PG, Insel RA, et al. Immunoglobulin light chain variable region gene sequences for human antibodies to Haemophilus influenzae type b capsular polysaccharide are dominated by a limited number of V kappa and V lambda segments and VJ combinations. J Clin Invest 1992; 89 : 729–38. [Google Scholar]
- Mendez MJ, Green LL, Corvalan JR, et al. Functional transplant of megabase human immunoglobulin loci recapitulates human antibody response in mice. Nat Genet 1997; 15 : 146–56. [Google Scholar]
- Green LL, Jakobovits A. Regulation of B cell development by variable gene complexity in mice reconstituted with human immunoglobulin yeast artificial chromosomes. J Exp Med 1998; 188 : 483–95. [Google Scholar]
- Tomizuka K, Shinohara T, Yoshida H, et al. Double trans-chromosomic mice : maintenance of two individual human chromosome fragments containing Ig heavy and kappa loci and expression of fully human antibodies. Proc Natl Acad Sci USA 2000; 97 : 722–7. [Google Scholar]
- Kuroiwa Y, Tomizuka K, Shinohara T, et al. Manipulation of human minichromosomes to carry greater than megabase-sized chromosome inserts. Nat Biotechnol 2000; 18 : 1086–90. [Google Scholar]
- Popov AV, Zou X, Xian J, Nicholson IC, Bruggemann M. A human immunoglobulin lambda locus is similarly well expressed in mice and humans. J Exp Med 1999; 189 : 1611–20. [Google Scholar]
- Nicholson IC, Zou X, Popov AV, et al. Antibody repertoires of four- and five-feature translocus mice carrying human immunoglobulin heavy chain and kappa and lambda light chain yeast artificial chromosomes. J Immunol 1999; 163 : 6898–906. [Google Scholar]
- Zou YR, Muller W, Gu H, Rajewsky K. Cre-loxP-mediated gene replacement : a mouse strain producing humanized antibodies. Curr Biol 1994; 4 : 1099–103. [Google Scholar]
- Harding FA, Lonberg N. Class switching in human immunoglobulin transgenic mice. Ann NY Acad Sci 1995; 764 : 536–46. [Google Scholar]
- Ball WJ, Jr., Kasturi R, Dey P, et al. Isolation and characterization of human monoclonal antibodies to digoxin. J Immunol 1999; 163 : 2291–8. [Google Scholar]
- Mukherjee J, Chios K, Fishwild D, et al. Human Stx2-specific monoclonal antibodies prevent systemic complications of Escherichia coli O157 : H7 infection. Infect Immun 2002; 70 : 612–9. [Google Scholar]
- He Y, Honnen WJ, Krachmarov CP, et al. Efficient isolation of novel human monoclonal antibodies with neutralizing activity against HIV-1 from transgenic mice expressing human Ig loci. J Immunol 2002; 169 : 595–605. [Google Scholar]
- Chang Q, Zhong Z, Lees A, et al. Structure-function relationships for human antibodies to pneumococcal capsular polysaccharide from transgenic mice with human immunoglobulin Loci. Infect Immun 2002; 70 : 4977–86. [Google Scholar]
- Villadsen LS, Schuurman J, Beurskens F, et al. Resolution of psoriasis upon blockade of IL-15 biological activity in a xenograft mouse model. J Clin Invest 2003; 112 : 1571–80. [Google Scholar]
- Bekker PJ, Holloway DL, Rasmussen AS, et al. A single-dose placebo-controlled study of AMG 162, a fully human monoclonal antibody to RANKL, in postmenopausal women. J Bone Miner Res 2004; 19 : 1059–66. [Google Scholar]
- Yang XD, Corvalan JR, Wang P, et al. Fully human anti-interleukin-8 monoclonal antibodies : potential therapeutics for the treatment of inflammatory disease states. J Leukoc Biol 1999; 66 : 401–10. [Google Scholar]
- Teeling JL, French RR, Cragg MS, et al. Characterization of new human CD20 monoclonal antibodies with potent cytolytic activity against non-Hodgkin lymphomas. Blood 2004; 104 : 1793–800. [Google Scholar]
- Schuler W, Bigaud M, Brinkmann V, et al. Efficacy and safety of ABI793, a novel human anti-human CD154 monoclonal antibody, in cynomolgus monkey renal allotransplantation. Transplantation 2004; 77 : 717–26. [Google Scholar]
- Bleeker WK, Lammerts van Bueren JJ, van Ojik HH, et al. Dual mode of action of a human anti-epidermal growth factor receptor monoclonal antibody for cancer therapy. J Immunol 2004; 173 : 4699–707. [Google Scholar]
- Imakiire T, Kuroki M, Shibaguchi H, et al. Generation, immunologic characterization and antitumor effects of human monoclonal antibodies for carcinoembryonic antigen. Int J Cancer 2004; 108 : 564–70. [Google Scholar]
- Foon KA, Yang XD, Weiner LM, et al. Preclinical and clinical evaluations of ABX-EGF, a fully human anti-epidermal growth factor receptor antibody. Int J Radiat Oncol Biol Phys 2004; 58 : 984–90. [Google Scholar]
- Skov L, Kragballe K, Zachariae C, et al. HuMax-CD4 : a fully human monoclonal anti-CD4 antibody for the treatment of psoriasis vulgaris. Arch Dermatol 2003; 139 : 1433–9. [Google Scholar]
- Keler T, Halk E, Vitale L, et al. Activity and safety of CTLA-4 blockade combined with vaccines in cynomolgus macaques. J Immunol 2003; 171 : 6251–9. [Google Scholar]
- Phan GQ, Yang JC, Sherry RM, et al. Cancer regression and autoimmunity induced by cytotoxic T lymphocyte-associated antigen 4 blockade in patients with metastatic melanoma. Proc Natl Acad Sci USA 2003; 100 : 8372–7. [Google Scholar]
- Hermeling S, Crommelin DJ, Schellekens H, Jiskoot W. Structure-immunogenicity relationships of therapeutic proteins. Pharm Res 2004; 21 : 897–903. [Google Scholar]
- Mannon PJ, Fuss IJ, Mayer L, et al. Anti-interleukin-12 antibody for active Crohn’s disease. N Engl J Med 2004; 351 : 2069–79. [Google Scholar]
Liste des figures
 |
Figure 1. Transgènes d’immunoglobulines humaines introduits chez la souris. Les locus des chaînes lourdes μ, δ, γ, α et légères λ, κ, etc. sont représentés en configuration germinale. Les gènes introduits par insertion aléatoire dans le génome des souris transgéniques sont schématisés en précisant le nombre de segments V et de gènes constants inclus dans les transgènes. |
| Dans le texte | |
 |
Figure 2. Séquences d’immunoglobulines humaines introduites dans le génome de la souris. Le locus des chaînes lourdes de la souris a été ciblé de façon à y introduire par recombinaison homologue des séquences provenant de régions constantes γ ou α des gènes d’immunoglobulines humains. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




