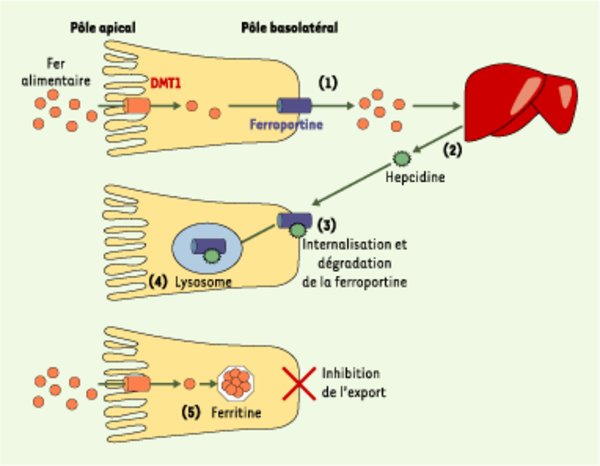
Figure 1.
Télécharger l'image originale
Modèle du mécanisme d’action de l’hepcidine. Après avoir été réduit, le fer alimentaire traverse la membrane apicale de l’entérocyte grâce au transporteur DMT1 puis transite vers la membrane basolatérale qu’il traverse en empruntant la ferroportine tout en étant réoxydé (1) (pour une revue plus détaillée des protéines impliquées, voir [1]). Le fer absorbé en excès est stocké au niveau du foie, provoquant une augmentation de la synthèse et de l’excrétion de l’hepcidine (par un mécanisme qui demeure inconnu) (2). L’hepcidine se lie alors directement sur la ferroportine (3), et induit son internalisation puis sa dégradation dans le lysosome (4). Le fer qui entre dans la cellule s’accumule alors dans la ferritine (5) et n’est plus exporté. Au final, le transport net du fer alimentaire est diminué et le pool de fer sera perdu lors de l’exfoliation de l’entérocyte au sommet de la villosité duodénale. Les réserves en fer (notamment hépatiques) sont alors utilisées pour maintenir une érythropoïèse efficace, ce qui, à terme, permet un retour à un état d’équilibre avec une diminution des réserves en fer. Lors d’une inflammation, une production excessive d’hepcidine pourrait aboutir à une dégradation trop importante de la ferroportine, engendrant une absorption insuffisante de fer. Un mécanisme similaire existerait au niveau des macrophages et des cellules du syncytiotrophoblaste, deux cibles tissulaires de l’hepcidine.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




