| Numéro |
Med Sci (Paris)
Volume 19, Numéro 2, Février 2003
|
|
|---|---|---|
| Page(s) | 135 - 137 | |
| Section | Le Magazine : Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2003192135 | |
| Publié en ligne | 15 février 2003 | |
Un rôle pour le cytosquelette dans les maladies mentales ?
A role for the cytoskeleton in mental diseases
Laboratoire du Cytosquelette, Inserm U.366, Département réponse et dynamique cellulaire, CEA-Grenoble, 17, rue des Martyrs, 38054 Grenoble, France
Les microtubules, des tubes à tout faire…
Les cellules eucaryotes contiennent un réseau d’éléments tubulaires de 25 nm de diamètre et de longueur variable, de 5 à 50 µm selon les types cellulaires. Dans les cellules de mammifères, ces microtubules sont en général polymérisés (nucléés) à partir d’un centrosome. Les réseaux microtubulaires adoptent des configurations variées correspondant à des fonctions également variées [1]. Ainsi, l’organisation de l’appareil de Golgi et des trafics intracellulaires dans les cellules interphasiques, ou la création du fuseau achromatique et la ségrégation des chromosomes durant la mitose sont des fonctions dépendantes des microtubules. Les réseaux microtubulaires sont particulièrement abondants dans les neurones. La tubuline représente à elle seule 20% des protéines neuronales. Les microtubules neuronaux sont nécessaires aux transports dendritiques et axonaux, et la perturbation de ces transports par des drogues ayant pour cible les microtubules telles que celles utilisées en oncologie induit des neuropathies. Un rôle des microtubules dans les fonctions cérébrales intégrées a été proposé, mais les connaissances dans ce domaine restent extrêmement limitées.
… avec des propriétés physico-chimiques spéciales
Les microtubules sont des polymères dynamiques. L’assemblage de la tubuline in vitro est facilement réversible, par exemple, par exposition des suspensions microtubulaires à des températures inférieures à 10 °C. Dans des solutions de tubuline complètement assemblée, les microtubules individuels présentent des fluctuations de longueur considérables, spontanées, qui témoignent de l’instabilité dynamique du système [2]. Cette instabilité microtubulaire est intimement liée à des propriétés d’auto-organisation spécifiques des microtubules [3]. En effet, in vitro, les microtubules sont capables d’auto-organisation dans le temps (oscillations cohérentes au cours desquelles l’ensemble des microtubules passe par des phases successives de désassemblage et de réassemblage) et spatiale (formation de structures ordonnées macroscopiques dites de Turing). En présence de protéines motrices, les microtubules peuvent s’organiser spontanément pour former des structures en fuseau, semblables aux assemblages mitotiques [4].
La stabilité énigmatique des microtubules neuronaux…
Bien que la dynamique microtubulaire semble intimement liée à la plupart des fonctions des microtubules cytoplasmiques, de nombreux types cellulaires contiennent des microtubules stables, insensibles à des conditions dépolymérisantes comme par exemple l’exposition au froid. Ainsi, dans les neurones, la quasitotalité des microtubules sont stables au froid [5]. L’origine et la signification fonctionnelle de cette stabilisation sont restées longtemps énigmatiques. Ces dernières années, toutefois, il est devenu évident que la stabilisation des neurotubules résulte largement de l’association de ces polymères avec des protéines contrôlées par la calmoduline, appelées protéines STOP (stable tubule only polypeptide). Dans des cellules neuronales en culture, l’inhibition de l’activité des protéines STOP abolit la stabilité au froid des microtubules et provoque une inhibition de la croissance des neurites [6].
… et les conséquences de la suppression de cette stabilité
Pour tester directement la fonction des protéines STOP, nous avons récemment développé des souris transgéniques porteuses d’un gène STOP invalidé (STOP−/−) [7]. Ces souris sont dépourvues de microtubules neuronaux stables (Figure 1). Les souris déficientes en protéines STOP ne présentent pas d’anomalies détectables de l’anatomie du cerveau et du système nerveux en général. Ces souris sont, en revanche, porteuses d’anomalies synaptiques, avec une diminution du nombre de vésicules synaptiques et l’abolition de plusieurs formes de plasticité synaptique à court et à long terme. Ces déficits synaptiques sont compatibles avec la survie des souris, mais sont associés à des troubles du comportement multiples et sévères. En particulier, les souris invalidées sont incapables de materner leur progéniture et les souriceaux nouveaunés ne survivent pas à cette déficience maternelle. Tous meurent dans les 24 à 48 heures qui suivent la naissance. Nous avons étudié les effets de divers agents psychotropes sur le comportement des mères déficientes en protéines STOP et observé un effet bénéfique des neuroleptiques. L’efficacité du traitement dépend de sa durée: administré dès la naissance des animaux déficients et durant leur développement, il induit ultérieurement une amélioration du comportement maternel, incomplète, mais cependant suffisante pour rendre possible la survie des nouveau-nés.
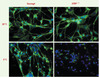 |
Figure 1. Les microtubules neuronaux des souris STOP−/− sont labiles au froid. Des neurones en culture issus de cerveaux embryonnaires (15,5 jours) d’animaux sauvages ou déficients en proteins STOP sont maintenus à température ambiante (20°C), ou exposés au froid (0°C) pendant 45 minutes. Les microtubules sont ensuite révélés avec un anticorps anti-β-tubuline (vert) et les noyaux sont marques avec une solution de Hoechst (bleu) (reproduit de [7] avec l’autorisation de l’éditeur). |
Conclusions
Les phénotypes observés chez les souris STOP−/− apportent tout d’abord la preuve que les protéines STOP sont bien les effecteurs principaux de l’étonnante stabilité des microtubules neuronaux. Ils indiquent également un rôle important de ces protéines dans la plasticité synaptique. Celleci étant dépendante d’événements morphogénétiques au niveau des boutons axonaux et des épines dendritiques, un tel rôle des microtubules et de leurs effecteurs était suspecté depuis longtemps [8]. Nos observations apportent un élément de preuve tangible à l’appui de ces hypothèses. La diminution du nombre de vésicules synaptiques que nous observons dans le compartiment pré-synaptique des souris STOP−/− est une cause plausible des troubles de certaines formes de plasticité à court terme. D’autres anomalies affectant la plasticité synaptique à long terme de ces souris suggèrent un rôle des protéines STOP dans le compartiment postsynaptique.
Les neuroleptiques sont de puissants antipsychotiques, principalement utilisés dans le traitement de la schizophrénie. L’origine de la schizophrénie reste mal connue, mais des modèles récents proposent d’en faire une « maladie de la synapse » [9]. Les souris déficientes en protéines STOP constituent un modèle de troubles multiples du comportement liés à une maladie synaptique et sensibles aux neuroleptiques. La disponibilité de telles souris ouvre de nouvelles perspectives de test de l’effet des neuroleptiques sur les fonctions synaptiques et le comportement.
Le gène STOP est-il impliqué dans des maladies humaines ? Ce gène est situé dans la région 11q14 du génome humain, région associée à des désordres schizoïdes chez l’homme [10]. Des études sont en cours pour déterminer s’il s’agit d’une coïncidence ou d’une association causale.
Références
- Bruce Alberts R, Bray D, Lewis J, et al. Molecular biology of the Cell, 3rd ed. New York: Garland publishing, 1994. [Google Scholar]
- Mitchison T, Kirschner M. Dynamic instability of microtubule growth. Nature 1984; 312: 237–42. [Google Scholar]
- Tabony J, Job D. Spatial structures in microtubular solutions requiring a sustained energy source. Nature 1990; 346: 448–51. [Google Scholar]
- Karsenti E, Vernos I. The mitotic spindle: a selfmade machine. Science 2001; 294: 543–7. [Google Scholar]
- Baas PW, Pienkowski TP, Cimbalnik KA, et al. Tau confers drug stability but not cold stability to microtubules in living cells. J Cell Sci 1994; 107: 135–43. [Google Scholar]
- Guillaud L, Bosc C, Fourest- Lieuvin A, et al. STOP proteins are responsible for the high degree of microtubule stabilization observed in neuronal cells. J Cell Biol 1998; 142: 167–79. [Google Scholar]
- Andrieux A, Salin PA, Vernet M, et al. The suppression of brain cold-stable microtubules in mice induces synaptic defects associated with neuroleptic-sensitive behavioral disorders. Genes Dev 2002; 16: 2350–64. [Google Scholar]
- Van Rossum D, Hanisch UK. Cytoskeletal dynamics in dendritic spines: direct modulation by glutamate receptors? Trends Neurosci 1999; 22: 290–5. [Google Scholar]
- Mirnics K, Middleton FA, Lewis DA, Levitt P. Analysis of complex brain disorders with gene expression microarrays: schizophrenia as a disease of the synapse. Trends Neurosci 2001; 24: 479–86. [Google Scholar]
- Brzustowicz LM, Hodgkinson KA, Chow EW, Honer WG, Bassett AS. Location of a major susceptibility locus for familial schizophrenia on chromosome 1q21-q22. Science 2000; 288: 678–82. [Google Scholar]
© 2003 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Les microtubules neuronaux des souris STOP−/− sont labiles au froid. Des neurones en culture issus de cerveaux embryonnaires (15,5 jours) d’animaux sauvages ou déficients en proteins STOP sont maintenus à température ambiante (20°C), ou exposés au froid (0°C) pendant 45 minutes. Les microtubules sont ensuite révélés avec un anticorps anti-β-tubuline (vert) et les noyaux sont marques avec une solution de Hoechst (bleu) (reproduit de [7] avec l’autorisation de l’éditeur). |
| Dans le texte | |
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.




