| Issue |
Med Sci (Paris)
Volume 19, Number 1, Janvier 2003
|
|
|---|---|---|
| Page(s) | 118 - 124 | |
| Section | Forum : Hypothéses Et Débats | |
| DOI | https://doi.org/10.1051/medsci/2003191118 | |
| Published online | 15 janvier 2003 | |
La mémoire aux prises avec les émotions et le stress : un impact nécessairement dommageable?
Memory at odds with emotion and stress: is the impact necessarily negative?
Centre de recherche de l’Hôpital Douglas, Pavillon Frank B. Common, 6875, boulevard LaSalle, Verdun, Québec, H4H 1R3, Canada
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Les émotions optimisent le rappel d’un événement traumatisant alors que le stress nuit à l’apprentissage de toute information lors d’une situation perturbatrice. Ces effets divergents des émotions et du stress sur la mémoire ont été attribués aux réactions physiologiques manifestées par l’organisme. En effet, lors de situations traumatisantes, les catécholamines et les glucocorticoïdes, en particulier, sont sécrétés. Ces hormones seraient des agents modulateurs des capacités mnésiques. Cet article décrit les effets spécifiques des émotions et du stress sur la mémoire. Les déterminants psychologiques et biologiques responsables de ces effets seront présentés, et différents points méthodologiques seront abordés dans le but de nuancer l’implication de ces déterminants quant à l’impact des émotions et du stress sur la mémoire. Mieux définir les effets des émotions et du stress sur la mémoire devrait permettre de comprendre plus spécifiquement les déficits cognitifs dont souffrent les patients qui, atteints de dépression ou d’un syndrome de stress post-traumatique, présentent des troubles émotifs.
Abstract
While intense negative events are vividly recalled, information learned during stressful situations is poorly remembered. These differential effects of emotions and stress on memory have been attributed to the physiological manifestations generated during those affective states. Intense emotional and stressful events trigger the secretion of catecholamines and of glucocorticoids, in particular. These hormones would be modulatory agents of memory functions. In the first part of this paper, we review the specific effects emotions and stress have on memory. We then summarize the psychological and biological determinants responsible for these effects. Finally, we discuss different methodological issues that could explain the discrepancy found between the impact of emotions and stress on memory. Defining more precisely the effects emotion and stress have on memory will lead to a better comprehension of the cognitive problems that characterize patients dealing with emotional turmoil, such as patients suffering from depression or post-traumatic stress disorder.
© 2003 médecine/sciences - Inserm / SRMS
Les émotions et le stress partagent de nombreuses caractéristiques [1]. En effet, un stress peut être ressenti lors d’une émotion, comme c’est le cas par exemple de la tristesse vécue lors d’un deuil, souvent accompagnée d’un état de stress. À l’inverse, lors d’une situation stressante, un individu peut ressentir différents types d’émotions, telles la peur ou la surprise. De plus, tout comme le stress, une émotion est une expérience affective intense, consciente, observable et brève, engendrée par des stimulus identifiables. Des agents de type physique (exercice physique) ou psychologique (être confronté à une situation nouvelle ou imprévisible) se sont révélés capables de susciter une émotion tout autant qu’un stress [2]. Enfin, lors d’une émotion comme lors d’un stress, l’organisme émet des réactions physiologiques. Il en résulte une mobilisation de l’énergie et des manifestations biologiques (voir ci-dessous) dont le principal effet est d’augmenter le niveau de vigilance (c’est-à-dire de stimuler la concentration) [2, 3].
Bien qu’ils partagent ces similitudes, les émotions et le stress sont en réalité deux entités distinctes [1]. Ainsi, une expérience émotive ne suscite pas toujours un stress (exemple de la tristesse vécue en regardant un film), alors qu’un stress engendre presque toujours une émotion spécifique (exemple d’un stress dû à un accident de voiture, accompagné de la peur de se blesser gravement). Aussi, les protocoles utilisés en laboratoire pour susciter une émotion ou un stress varient de façon importante. L’induction des émotions se fait passivement, l’individu étant soumis à la présentation d’images, de films ou de mots qui auront comme impact souhaité de susciter une émotion négative. Le stress, en revanche, est habituellement induit de façon active: on sollicite la participation d’un individu en le plaçant devant une situation nouvelle et imprévisible, comme celle où il se trouve obligé de prononcer un discours en public.
Fondements physiologiques des émotions et du stress
Malgré les distinctions qui opposent émotions et stress, l’organisme présente la même réactivité physiologique lorsqu’il est soumis à l’un ou à l’autre de ces deux états affectifs [3, 4]. Les manifestations se caractérisent principalement par l’augmentation du rythme cardiaque et de la tension artérielle, ainsi que par l’élévation de la sécrétion d’hormones telles que certaines catécholamines (adrénaline, noradrénaline) et les glucocorticoïdes.
Il s’agit dans un premier temps d’une mobilisation rapide du système nerveux autonome (SNA). Lorsque le cerveau perçoit et reconnaît le caractère émotif ou stressant d’un événement, il stimule immédiatement l’hypothalamus, lequel active le SNA. Celui-ci stimule alors la médullo-surrénale, laquelle sécrète davantage d’adrénaline et de noradrénaline (Figure 1) [4].
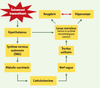 |
Figure 1. Activation du système noradrénergique. Le cerveau, après avoir interprété un événement comme étant traumatisant, stimule l’hypothalamus, qui, à son tour, mobilise le système nerveux autonome (SNA). Ce dernier active la médullo-surrénale qui déclenche alors la sécrétion des catécholamines - adrénaline et noradrénaline - responsables de l’activation du nerf vague et du tractus solitaire. Les influx nerveux en provenance du tractus solitaire stimulent le locus coeruleus, ce qui déclenche l’activation du système noradrénergique central. La noradrénaline sécrétée par le locus coeruleus rejoint les noyaux noradrénergiques centraux de l’amygdale et de l’hippocampe. Notons que l’hypothalamus peut activer lui-même les cellules du locus coeruleus, et stimuler ainsi la sécrétion de noradrénaline avant même que les catécholamines périphériques en provenance de la médullo-surrénale n’en donnent l’ordre au locus coeruleus |
Dans un second temps, l’axe hypothalamo-hypophysosurrénalien s’active (Figure 2) [4]. Le cerveau stimule alors la sécrétion de CRH (corticotropin-releasing hormone) par l’hypothalamus, qui entraîne une augmentation de la libération de l’hormone corticotrope (ACTH) par l’hypophyse. Par la suite, l’ACTH stimule la corticosurrénale, laquelle sécrète des glucocorticoïdes [4].
 |
Figure 2. Activation et rétrocontrôle de l’axe hypothalamo-hypophyso-surrénalien (HHS) lors d’un événement traumatisant. La sécrétion de CRH (corticotropinreleasing hormone) par l’hypothalamus stimule la production d’ACTH (hormone corticotrope) par l’hypophyse. La corticosurrénale détecte les concentrations sanguines d’ACTH et, en réponse à cette activation de l’hypophyse, sécrète du cortisol. Celui-ci rejoint ses récepteurs, situés en périphérie et au niveau cérébral: récepteurs des glucocorticoïdes de type II surtout dans le cortex préfrontal et récepteurs de type I et II dans l’hippocampe. Ces deux structures corticales sont responsables du contrôle négatif de l’axe HHS, par l’envoi d’un message inhibiteur à l’hypothalamus entraînant l’arrêt de la libération de CRH. Le cortisol circulant adresse également un message inhibiteur à l’hypothalamus, pour faire cesser la sécrétion de CRH, et à l’hypophyse, pour faire cesser la sécrétion d’ACTH. Enfin, l’ACTH circulant envoie un message inhibiteur à l’hypothalamus, chargé de limiter la sécrétion de CRH. Par ces boucles de rétrocontrôle négatif, l’organisme peut réduire, et ramener à une valeur basale, les concentrations sanguines de cortisol après un événement traumatisant. |
Le cortisol, principal glucocorticoïde chez l’homme, est très liposoluble, et traverse donc facilement la barrière hémato-encéphalique. Il rejoint alors les récepteurs des glucocorticoïdes présents dans différentes régions cérébrales, dont le cortex préfrontal [5] et le complexe hippocampique (hippocampe, gyrus parahippocampique et cortex enthorinal [6]). La mémoire « déclarative », c’est-à-dire la mémoire des scènes et des expériences vécues en fonction des endroits et des moments où ces événements ont eu lieu, est très sensible aux émotions et au stress, puisqu’elle dépend de ces deux régions [7]. Contrairement au cortisol, l’adrénaline et la noradrénaline sécrétées en périphérie ne rejoignent pas si facilement les structures cérébrales, car ce sont des molécules hydrosolubles qui ne traversent pas aisément la barrière hémato-encéphalique [8]. Toutefois, ces catécholamines périphériques réussissent à stimuler la sécrétion de noradrénaline au niveau du cerveau en envoyant un message le long de fibres viscérales efférentes aboutissant au cortex (Figure 1). Des études réalisées chez des rongeurs ont démontré que des fibres rénales sympathiques reliaient les reins et les glandes surrénales au bulbe rachidien inférieur [9]. Ces fibres viscérales afférentes suivent alors les projections du nerf vague et forment des synapses au niveau du noyau du tractus solitaire, à partir duquel les neurones noradrénergiques projettent des fibres efférentes vers le cortex [10].
Le système noradrénergique central n’a cependant pas besoin de ce message nerveux provenant de la périphérie pour s’activer lors d’une émotion ou d’un stress. Les cellules nerveuses du locus coeruleus, un noyau regroupant des neurones noradrénergiques dans la région médiane rostrale de la protubérance, sont directement stimulées par l’hypothalamus, avant même que les catécholamines périphériques en provenance de la médullo-surrénale ne leur en donnent l’ordre [8]. La stimulation du locus coeruleus entraîne une augmentation de la sécrétion de noradrénaline qui suivra des fibres efférentes jusqu’aux noyaux noradrénergiques du cortex, retrouvés, entre autres, au niveau du complexe hippocampique, et plus particulièrement de l’amygdale [8]. De fait, la consolidation en mémoire de tout événement perturbateur implique non seulement le cortex préfrontal et l’hippocampe, mais également l’amygdale, qui appartient au lobe limbique du cerveau, une région cérébrale reconnue pour son implication dans l’analyse du caractère émotif d’un stimulus [3]. Plusieurs études ont démontré le rôle primordial que joue l’amygdale dans l’identification et la mémorisation d’événements traumatisants, chez l’animal comme chez l’homme [3, 11, 12].
Effets des émotions sur la mémoire humaine
Phénomène de la mémoire flash (flashbulb memory)
Plus une information revêt d’importance, plus l’attention qui lui est portée est grande, et plus elle sera solidement mémorisée. Un événement traumatisant, contrairement à toute situation banale, est suffisamment saillant pour capter toutes les ressources attentionnelles d’un individu, ce qui optimise son emmagasinage et sa consolidation en mémoire [13].
Ainsi, plusieurs d’entre nous, se souvenant clairement des attentats du 11 septembre 2001 à New York et à Washington, se souviennent également de l’heure qu’il était, des gens avec qui ils étaient ou encore de ce qu’ils étaient en train de faire lorsqu’ils ont appris la nouvelle. En revanche, le déroulement d’une journée quotidienne quelques jours avant les événements du 11 septembre n’aura pas été conservé aussi fortement en mémoire. Récemment, Scott et Pondosa [14] ont démontré que ce phénomène de la mémoire flash, c’est-à-dire le très fort souvenir qu’on a d’un événement perturbateur, est créé aussi bien par des émotions positives que négatives. En étudiant la qualité du rappel de différentes situations émotives, ces chercheurs ont rapporté qu’un fait positif tel que la sortie de prison de Nelson Mandela était aussi bien mémorisé qu’un fait négatif comme l’explosion de la navette spatiale Challenger.
Rôle de la noradrénaline
De nombreuses études ont proposé que la hausse significative des catécholamines dans l’amygdale optimiserait la consolidation en mémoire des événements traumatisants [8, 11]. L’amygdale est en effet une région riche en récepteurs α- et β-adrénergiques. Lorsque la noradrénaline active les récepteurs β-adrénergiques, en particulier, l’amygdale accorde une connotation émotive, donc importante, aux informations à mémoriser. Une attention soutenue serait portée aux événements négatifs et l’hippocampe s’assurerait de la bonne consolidation en mémoire des informations modulées par l’amygdale [11]. Cette théorie suggère donc que l’administration, lors de l’apprentissage d’un événement perturbateur, d’une substance pouvant bloquer les récepteurs adrénergiques centraux empêcherait la noradrénaline d’optimiser la consolidation de l’événement en mémoire.
Chez l’être humain, plusieurs études ont tenté de vérifier cette hypothèse en utilisant des substances capables de bloquer les récepteurs β-adrénergiques aux niveaux périphérique et central, telles que le propranolol. Cette substance est un β-bloquant très liposoluble qui franchit aisément la barrière hémato-encéphalique [15]. De plus, elle se lie également à des protéines plasmatiques, dont l’orosomucoïde (glycoprotéine α1-acidique), qui traversent également la barrière hématoencéphalique. Une fois à destination, les molécules de propranolol se détachent promptement des protéines et, puisqu’elles sont très liposolubles, se distribuent rapidement et équitablement dans les tissus périphériques et dans différentes régions du cerveau, dont l’amygdale et l’hippocampe [15].
Cahill et al. [16], en utilisant le propranolol, ont été les premiers à démontrer que la noradrénaline était impliquée dans les processus de mémoire émotive chez l’homme. Ces chercheurs ont présenté à deux groupes de sujets des histoires à valence émotive neutre (condition neutre) et, à deux autres groupes, des histoires à valence émotive négative (condition émotive). Deux des groupes de sujets recevaient un placebo, tandis que les deux autres groupes recevaient du propranolol. Les volontaires, croyant participer à une étude sur la réactivité physiologique manifestée face à des stimulus, étaient soumis à une tâche de mémoire incidente, c’està- dire pour laquelle l’expérimentateur n’avisait pas les sujets qu’ils devraient ultérieurement se rappeler le matériel présenté [7]. Les participants recevaient alors la consigne de regarder attentivement les histoires présentées, pendant que des moniteurs enregistraient leur rythme cardiaque et leur tension artérielle. Un test de mémoire « surprise » a eu lieu une semaine plus tard (le rappel étant d’autant meilleur que l’intervalle de temps après application de stimulus émotifs est long [17]). Les résultats démontrent que les sujets du groupe placebo se rappellent un plus grand nombre d’éléments de l’histoire émotive que les sujets du groupe propranolol, tandis que, dans la condition neutre, la performance au rappel des deux groupes est similaire. Des résultats semblables ont également été obtenus par Van Stegeren et al. [18] et par O’Carroll et al. [19]. Ils tendent à démontrer que la noradrénaline est essentielle à la mémorisation des événements émotifs.
Effets du stress sur la mémoire humaine
Phénomène de l’interférence
Lorsque trop d’informations demandent à être traitées en même temps, les ressources attentionnelles d’un individu ne suffisent plus à la demande. Distinguer les stimulus qu’il est important d’apprendre devient difficile, ce qui nuit au rappel immédiat ou différé des items [2]. Plusieurs facteurs comme le froid ou le bruit créent du stress et engendrent une telle situation d’interférence. On observe ainsi que des individus soumis à un apprentissage d’items à valence émotive neutre dans un environnement bruyant ne se rappellent, immédiatement après, qu’un faible pourcentage des éléments présentés [2].
Afin de caractériser l’impact d’un stress psychologique sur la mémoire humaine, des chercheurs ont développé une épreuve appelée le TSST (trier social stress test [20]). Un stress de type psychologique est un stress issu de toute confrontation entre un individu et une situation jugée par ce dernier comme étant nouvelle, imprévisible, incontrôlable, inattendue ou surprenante [2]. Les sujets soumis au TSST doivent discourir à propos d’un sujet neutre, mais difficile à développer, et résoudre des problèmes arithmétiques en public. L’impact de cette épreuve sur la mémoire est mesuré en soumettant des individus au TSST et, aussitôt après, à l’apprentissage d’items à valence émotive neutre. Le stress engendré par le TSST nuit à la performance mnésique des sujets, puisque ces derniers ne se rappellent, immédiatement après le codage des items, qu’un petit nombre de stimulus [21].
Rôle du cortisol
Il a été suggéré que le cortisol sécrété par l’organisme confronté à un « stresseur » tel que le TSST serait l’un des facteurs responsables des effets néfastes du stress sur la mémoire [21]. Les chercheurs ont tenté de confirmer cette hypothèse en observant le profil cognitif de certains patients dont les taux de cortisol endogène sont chroniquement élevés (patients souffrant de dépression majeure ou du syndrome de Cushing, c’està- dire d’un état d’hypercorticisme chronique, par exemple): les résultats montrent l’existence d’importants déficits de la mémoire déclarative chez ces patients [22].
Il a alors été proposé que les effets du stress sur la mémoire seraient dus à la saturation, par des taux de cortisol élevés, des récepteurs des glucocorticoïdes situés dans le cortex préfrontal et dans l’hippocampe [23, 24]. Plusieurs études animales ont souligné l’implication de ces récepteurs dans le fonctionnement des processus mnésiques: les récepteurs des glucocorticoïdes de type I jouent un rôle lors de la sélection des informations à retenir, tandis que les récepteurs de type II sont sollicités lors de la mémorisation de ces informations [24, 25].
Pour imiter les effets physiologiques du stress, des glucocorticoïdes synthétiques (hydrocortisone et cortisone) ont été administrés à de jeunes sujets sains avant de les soumettre à l’apprentissage d’une liste de mots neutres. D’une façon attendue, l’augmentation des taux de cortisol causée par l’administration des glucocorticoïdes synthétiques s’accompagnait de troubles mnésiques, puisque les sujets ayant reçu des glucocorticoïdes synthétiques ont mémorisé un plus petit nombre de mots que les sujets ayant reçu un placebo [21]. De Quervain et al. [26] ont quant à eux observé des troubles de la mémoire déclarative après l’administration de cortisone une heure avant le rappel de mots, alors qu’aucun déficit mnésique n’était enregistré lors d’une administration de cortisone une heure avant, ou immédiatement après, l’apprentissage des items. Ces résultats laissent sous-entendre que les processus de rappel, tout comme ceux de codage ou de consolidation de stimulus, seraient vulnérables à une hausse des taux de cortisol.
Toutefois, l’hypothèse selon laquelle les glucocorticoïdes auraient des effets modulateurs, et non pas exclusivement négatifs, sur la mémoire humaine a récemment été proposée. Lupien et al. [27] ont d’abord administré, à de jeunes sujets sains, de la métyrapone, un inhibiteur de la synthèse de cortisol, puis ont ramené les taux de cortisol des sujets à leur niveau de base en administrant de l’hydrocortisone (condition expérimentale). La performance mnésique des sujets a été évaluée dans ces deux situations, et a été comparée à la performance obtenue pour la même tâche de mémoire effectuée sous placebo (condition témoin). Les résultats montrent qu’une diminution des taux de cortisol, comparativement au placebo, nuit à la mémoire déclarative, et qu’une administration d’hydrocortisone annule les effets de la métyrapone et ramène les capacités mnésiques à leur niveau optimal de fonctionnement. Ces auteurs ont également démontré dans la même étude que l’administration d’hydrocortisone dans l’après-midi, alors que les taux de cortisol sont physiologiquement bas en raison des variations circadiennes de sa sécrétion [4], facilite le rappel d’une liste de mots, comparativement à l’administration d’un placebo. Ces résultats suggèrent que les effets des glucocorticoïdes sur la mémoire humaine sont relatifs plutôt qu’absolus. L’impact d’une augmentation des taux de cortisol ne serait pas nécessairement négatif, mais dépendrait plutôt du niveau des taux de glucocorticoïdes circulants au moment de l’augmentation de la sécrétion de cortisol.
Émotions et stress : deux phénomènes distincts?
De nombreuses études ont démontré que les émotions et le stress sont deux entités distinctes qui n’ont pas le même impact sur la mémoire. Alors que les émotions optimisent la mémorisation des événements traumatisants, le stress engendré par une situation perturbatrice nuit à l’apprentissage de toute information. On constate que deux domaines d’étude indépendants ont traité de l’impact des émotions et du stress sur la mémoire. Dans le premier, les émotions négatives, en augmentant la concentration sanguine des catécholamines, optimisent la mémoire de l’événement ayant induit l’émotion. Dans le second, les effets négatifs du stress sur la mémoire sont dus à l’élévation de la cortisolémie, ce qui nuit au bon fonctionnement de l’hippocampe.
Bien que cette hypothèse de la spécificité des mécanismes d’action ait longtemps paru appropriée pour décrire les effets différentiels du stress et des émotions négatives sur la mémoire, elle est sérieusement remise en question, du fait qu’au moins deux divergences méthodologiques majeures existent entre les protocoles expérimentaux de recherche de ces deux domaines d’étude.
Utilisation de différentes tâches de mémoire
Lorsqu’un événement perturbateur survient, toute l’attention d’un individu est captée par cet événement. Dans les protocoles expérimentaux utilisés par les études évaluant l’impact des émotions sur la mémoire, les chercheurs ont mesuré la capacité d’un individu de se remémorer l’événement qui a induit l’émotion. Puisque les catécholamines sécrétées lors de l’émotion dirigeraient toute l’attention d’un individu sur l’événement négatif, au détriment d’ailleurs de tous détails concernant la situation [13], il n’est pas surprenant de constater que le rappel d’un événement négatif est optimisé en mémoire.
Les études mesurant l’impact du stress sur la mémoire, en revanche, se sont attachées à mesurer les capacités d’un individu de mémoriser des informations qui ne sont pas liées à la source de stress. Lorsqu’un individu doit mémoriser des informations ne concernant pas l’événement ayant induit les émotions ou le stress, l’apprentissage de ces items supplémentaires devient beaucoup plus difficile. Disposant de ressources attentionnelles limitées, un individu ne peut pas traiter à la fois des informations concernant l’événement perturbateur (ici, le stresseur) et des items liés à la tâche de mémoire. Les effets différentiels des émotions et du stress sur la mémoire pourraient donc s’expliquer par le fait qu’on ne mesure pas, dans les protocoles méthodologiques des deux domaines de recherche, la mémorisation d’items ayant la même valence émotive (négatif versus neutre) et revêtant la même signification pour le sujet (items ayant induit l’émotion versus item banal non lié à la source de stress).
Sexe des sujets sélectionnés : rôle de la noradrénaline
Les recherches évaluant les effets du stress sur la mémoire ont été effectuées, en grande majorité, auprès d’échantillons seulement constitués d’hommes, plus réactifs que les femmes au stress [21, 28]. Les chercheurs évaluant l’impact du stress sur la mémoire ont ainsi délibérément choisi de constituer des échantillons de sujets ne comprenant que des hommes, après avoir constaté que les hormones sexuelles féminines influençaient la réactivité cortisolémique au stress [28]. Ainsi, les femmes en phase lutéale (jours 15 à 28 du cycle menstruel), dont les concentrations sanguines d’œstrogènes sont très élevées, ont une réponse cortisolémique similaire à celle des hommes lorsqu’elles sont soumises à un « stresseur ». En revanche, les femmes en phase folliculaire (jours 5 à 13 du cycle menstruel; concentrations sanguines d’œstrogènes peu élevées) ou prenant des anovulatoires (concentrations sanguines d’œstro gènes moyennement élevées) présentent une réactivité cortisolémique au stress beaucoup moins importante que les hommes ou que les femmes en phase lutéale [28]. Les œstrogènes semblant moduler la hausse des taux de cortisol, il semblait nécessaire de contrôler cette variable concomitante dans les études visant à évaluer l’impact du stress sur la mémoire.
Les recherches portant sur les émotions ont, quant à elles, eu plus souvent recours à des sujets de sexe féminin que masculin, car les femmes sont plus réactives que les hommes à des stimulus émotifs [11]. Si la vigilance des femmes est particulièrement sollicitée par ce type de stimulus, il est fort probable que le niveau d’attention qu’elles porteront aux événements perturbateurs sera plus important que celui porté par les hommes aux mêmes stimulus. Sélectionner, dans un échantillon, des sujets qui répondent plus fortement aux stimulus émotifs mènera évidemment à conclure, sans trop de difficulté, que la mémoire d’événements traumatisants est optimisée.
Dans le cadre des études portant sur les émotions, choisir majoritairement des femmes pose un second problème car, outre le cortisol, les œstrogènes influencent également la sécrétion de noradrénaline: stimulation de la synthèse, augmentation de la sensibilité des récepteurs noradrénergiques et inhibition du catabolisme de la noradrénaline en inhibant la monoamine oxydase [29]. Les femmes, qui ont bien sûr des taux d’œstrogènes plus élevés que les hommes, risquent donc de présenter des concentrations sanguines de noradrénaline plus élevées que les hommes. Lorsqu’un échantillon de sujets est constitué majoritairement de femmes, il y a ainsi de fortes chances que la mémoire des événements perturbateurs soit optimisée chez les sujets de ce groupe, puisque la bonne performance des femmes haussera la performance moyenne du groupe.
Il en va de même pour les femmes prenant des anovulatoires. Ces dernières ont bien sûr des taux de noradrénaline plus élevés que les hommes, mais aussi plus élevés que les femmes ne prenant pas d’anovulatoires. En effet, les taux élevés d’œstrogènes retrouvés chez les femmes utilisant des anovulatoires risquent d’augmenter davantage leurs taux de noradrénaline, par rapport aux femmes ne prenant pas la pilule contraceptive. Les femmes faisant usage d’anovulatoires peuvent donc être encore plus stimulées à diriger leur attention sur l’événement perturbateur que les autres sujets de l’échantillon, ce qui améliorera encore la performance moyenne du groupe.
Enfin, l’effet des β-bloquants est également soumis à l’influence de la prise d’anovulatoires, d’où encore la difficulté d’inclure, dans les échantillons expérimentaux, une quantité élevée de femmes. En effet, Kendall et al. [30] rapportent que les anovulatoires inhibent l’activité des enzymes hépatiques, ce qui diminue la vitesse de dégradation des β-bloquants, lesquels restent alors plus longtemps dans le sang. Le blocage des récepteurs noradrénergiques par les β-bloquants et, par conséquent, l’impossibilité pour la noradrénaline de rejoindre ses récepteurs sont donc des effets optimisés à plus long terme chez les femmes faisant usage d’anovulatoires. Majoritaires dans un échantillon de sujets auxquels est administré un β-bloquant, les femmes prenant des anovulatoires risquent de présenter plus de difficulté que les autres sujets du groupe (hommes ou femmes ne prenant pas la pilule contraceptive) à mémoriser un événement émotif. La performance moyenne pour l’ensemble des sujets du groupe en est alors affaiblie, laissant sousentendre qu’un déficit en noradrénaline empêche, chez tout individu, l’optimisation de la mémoire d’un événement perturbateur.
Conclusions
Émotions et stress semblent donc être deux entités distinctes puisqu’ils présentent un impact différent sur la mémoire: les émotions optimiseraient le rappel d’un événement traumatisant, alors que le stress nuirait à l’apprentissage de toute information lors d’une situation perturbatrice. Cependant, avant de conclure qu’émotions et stress ont effectivement un impact contraire sur la mémoire, les divergences méthodologiques que nous avons mises en relief entre ces deux domaines d’études devront être contrôlées et vérifiées par de futures études. De plus, les émotions et le stress sont régularisés par des mécanismes d’action psychologique et physiologique complexes et multiples, qui n’impliquent pas la sécrétion d’une seule hormone. En fait, plusieurs hormones et neurotransmetteurs s’activent au cours de ces réactions affectives, comme la sérotonine, la dopamine et les œstrogènes. Comprendre le rôle joué par chacun(e) de ces hormones et neurotransmetteurs, ainsi que les interactions qu’elles partagent, serait nécessaire pour bien définir les effets d’une situation traumatisante en termes de mémorisation.
Il semble également fort souhaitable de mieux comprendre le fonctionnement de certaines structures cérébrales sollicitées lors de situations traumatisantes. L’amygdale, par exemple, renferme des récepteurs capables de reconnaître la noradrénaline, le cortisol et les œstrogènes, et entretient des liens étroits avec l’hippocampe. Bien comprendre son fonctionnement devrait permettre de mieux concevoir les effets modulateurs des hormones sur les processus mnésiques.
Remerciements
Les travaux de F.S.M. sont subventionnés par une bourse des Instituts canadiens de recherche en santé (ICRS). Les travaux de S.J.L. sont subventionnés par le Conseil de recherches en sciences naturelles et en génie du Canada (CRSNG).
Références
- Lupien SJ, Brière S. Memory and stress. In: Fink G, ed. The encyclopedia of stress. San Diego: Academic Press, 2000 : 721–8. [Google Scholar]
- Mandler G. Mind and body, the psychology of emotion and stress. New York: W.W. Norton and Co, 1984 : 330 p. [Google Scholar]
- LeDoux J. The emotional brain. New York: Simon and Schuster Inc, 1996 : 384 p. [Google Scholar]
- Norman AW, Litwack G. Hormones, 2e ed. San Diego: Academic Press, 1997 : 558 p. [Google Scholar]
- Sanchez MM, Young LJ, Plotsky PM, Insel TR. Distribution of corticosteroid receptors in the rhesus brain: relative absence of glucocorticoid receptors in the hippocampal formation. J Neurosci 2000; 20: 4657–68. [Google Scholar]
- McEwen BS, Weiss JM, Schwartz LS. Selective retention of corticosterone by limbic structures in rat brain. Nature 1968; 220: 911–2. [Google Scholar]
- Tulving E, Craik FIM. The Oxford handbook of memory. New York: Oxford University Press, 2000 : 700 p. [Google Scholar]
- McGaugh JL. Memory: a century of consolidation. Science 2000; 287: 248–51. [Google Scholar]
- Wyss JM, Donovan MK. A direct projection from the kidney to the brainstem. Brain Res 1984; 298: 130–4. [Google Scholar]
- Zardetto-Smith AM, Gray TS. Organization of peptidergic and catecholaminergic efferents from the nucleus of the solitary tract to the rat amygdala. Brain Res Bull 1990; 25: 875–87. [Google Scholar]
- Cahill L. Neurobiological mechanisms of emotionally influenced, long-term memory. Prog Brain Res 2000; 126: 29–37. [Google Scholar]
- Phelps EA, Anderson AK. Emotional memory: what does the amygdala do? Curr Biol 1997; 7: R311–4. [Google Scholar]
- Christianson SA. Emotional stress and eyewitness memory: a critical review. Psychol Bull 1992; 112: 284–309. [Google Scholar]
- Scott D, Ponsoda V. The role of positive and negative affect in flashbulb memory. Psychol Rep 1996; 79: 467–73. [Google Scholar]
- Tanaka H, Mizojiri K. Drugprotein binding and bloodbrain barrier permeability. J Pharmacol Exp Ther 1999; 288: 912–8. [Google Scholar]
- Cahill L, Prins B, Weber M, McGaugh JL. β-adrenergic activation and memory for emotional events. Nature 1994; 371: 702–4. [Google Scholar]
- Kleinsmith LJ, Kaplan S. Paired-associate learning as a function of arousal and interpolated interval. J Exp Psychol Genet 1963; 65: 190–3. [Google Scholar]
- Van Stegeren AH, Everaerd W, Cahill L, McGaugh JL, Gooren LJG. Memory for emotional events: differential effects of centrally versus peripherally acting β-blocking agents. Psychopharmacology 1998; 138: 305–10. [Google Scholar]
- O’Carroll RE, Drysdale E, Cahill L, Shajahan P, Ebmeier KP. Stimulation of the noradrenergic system enhances and blockade reduces memory for emotional material in man. Psychol Med 1999; 29: 1083–8. [Google Scholar]
- Kirschbaum C, Pirke KM, Hellhammer DH. The trier social stress test: a tool for investigation psychobiological stress responses in a laboratory setting. Neuropsychobiology 1993; 28: 76–81. [Google Scholar]
- Lupien SJ, McEwen BS. The acute effects of corticosteroids on cognition: integration of animal and human model studies. Brain Res Brain Res Rev 1997; 24: 1–27. [Google Scholar]
- Sapolsky RM. Glucocorticoids and hippocampal atrophy in neuropsychiatric disorders. Arch Gen Psychiatry 2000; 57: 925–33. [Google Scholar]
- Lupien SL, Lepage M. Stress, memory, and the hippocampus: can’t live with it, can’t live without it. Behav Brain Res 2001; 126: 137–58. [Google Scholar]
- De Kloet ER, Oitzl MS, Joëls M. Stress and cognition: are corticosteroids good or bad guys? Trends Neurosci 1999; 22: 422–6. [Google Scholar]
- De Kloet ER. Stress in the brain. Eur J Pharmacol 2000; 405: 187–98. [Google Scholar]
- De Quervain DJF, Roozendaal B, Nitsch RM, McGaugh JL, Hock C. Acute cortisone administration impairs retrieval of long-term declarative memory in humans. Nat Neurosci 2000; 3: 313–4. [Google Scholar]
- Lupien SL, Wilkinson CW, Brière S, Ménard C, Ng Yin Kin NMK, Nair NPV. The modulatory effects of corticosteroids on cognition: studies in young human populations. Psychoneuroendocrinology 2002; 27: 401–16. [Google Scholar]
- Kirschbaum C, Kudiela BM, Gaab J, Schommer NC, Hellhammer DH. Impact of gender, menstrual cycle phase, and oral contraceptives on the activity of the hypothalamuspituitary- adrenal axis. Psychosom Med 1999; 61: 154–62. [Google Scholar]
- McEwen BS. Non-genomic and genomic effects of steroids on neural activity. Trends Pharmacol Sci 1991; 12: 141–7. [Google Scholar]
- Kendall MJ, Jack DB, Quarterman CP, Smith SR, Zaman R. β-adrenoceptor blocker pharmacokinetics and the oral contraceptive pill. Br J Clin Pharmacol 1984; 17: 87S–9. [Google Scholar]
Liste des figures
 |
Figure 1. Activation du système noradrénergique. Le cerveau, après avoir interprété un événement comme étant traumatisant, stimule l’hypothalamus, qui, à son tour, mobilise le système nerveux autonome (SNA). Ce dernier active la médullo-surrénale qui déclenche alors la sécrétion des catécholamines - adrénaline et noradrénaline - responsables de l’activation du nerf vague et du tractus solitaire. Les influx nerveux en provenance du tractus solitaire stimulent le locus coeruleus, ce qui déclenche l’activation du système noradrénergique central. La noradrénaline sécrétée par le locus coeruleus rejoint les noyaux noradrénergiques centraux de l’amygdale et de l’hippocampe. Notons que l’hypothalamus peut activer lui-même les cellules du locus coeruleus, et stimuler ainsi la sécrétion de noradrénaline avant même que les catécholamines périphériques en provenance de la médullo-surrénale n’en donnent l’ordre au locus coeruleus |
| Dans le texte | |
 |
Figure 2. Activation et rétrocontrôle de l’axe hypothalamo-hypophyso-surrénalien (HHS) lors d’un événement traumatisant. La sécrétion de CRH (corticotropinreleasing hormone) par l’hypothalamus stimule la production d’ACTH (hormone corticotrope) par l’hypophyse. La corticosurrénale détecte les concentrations sanguines d’ACTH et, en réponse à cette activation de l’hypophyse, sécrète du cortisol. Celui-ci rejoint ses récepteurs, situés en périphérie et au niveau cérébral: récepteurs des glucocorticoïdes de type II surtout dans le cortex préfrontal et récepteurs de type I et II dans l’hippocampe. Ces deux structures corticales sont responsables du contrôle négatif de l’axe HHS, par l’envoi d’un message inhibiteur à l’hypothalamus entraînant l’arrêt de la libération de CRH. Le cortisol circulant adresse également un message inhibiteur à l’hypothalamus, pour faire cesser la sécrétion de CRH, et à l’hypophyse, pour faire cesser la sécrétion d’ACTH. Enfin, l’ACTH circulant envoie un message inhibiteur à l’hypothalamus, chargé de limiter la sécrétion de CRH. Par ces boucles de rétrocontrôle négatif, l’organisme peut réduire, et ramener à une valeur basale, les concentrations sanguines de cortisol après un événement traumatisant. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




