| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
|
|
|---|---|---|
| Page(s) | 866 - 868 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2025221 | |
| Published online | 12 December 2025 | |
Les virus oncolytiques influencent la biogenèse et l’immunogénicité des vésicules extracellulaires d’origine tumorale
Oncolytic viruses influence the biogenesis and immunogenicity of tumor-derived extracellular vesicles
Nantes université, Inserm UMR 1307, CNRS UMR 6075, Université d’Angers, Centre de recherche en cancérologie et immunologie intégrée Nantes-Angers (CRCI2NA), Nantes, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Les virus oncolytiques sont des agents thérapeutiques qui ont d’abord été développés pour leur capacité à infecter et éliminer spécifiquement les cellules tumorales présentant des défauts de réponse antivirale. De nombreux travaux ont ensuite montré leur propension à activer différents acteurs de l’immunité anti-tumorale, ce qui a conduit à leur intégration dans des stratégies d’immunothérapie [1]. Ces virus présentent ainsi des propriétés uniques permettant de reprogrammer le microenvironnement tumoral, en favorisant par exemple le recrutement de cellules immunitaires, et en modifiant favorablement le phénotype et les fonctions des différents types cellulaires qui le constituent. Malgré la mise sur le marché de l’herpèsvirus Talimogene laherparepvec (T-Vec) en 2015 pour le traitement du mélanome métastatique [2] et le succès attendu d’autres virus oncolytiques [3], une utilisation médicale plus étendue de ces virus nécessite de mieux caractériser leurs mécanismes d’action.
En agissant directement ou indirectement sur différents types cellulaires au sein des tumeurs, les virus oncolytiques influencent la communication intercellulaire. Les vésicules extracellulaires sont des médiateurs de la communication intercellulaire dont le rôle est très étudié dans des contextes pathologiques tels que le cancer [4]. Il s’agit d’un ensemble hétérogène de particules submicrométriques sécrétées par tous les types cellulaires, et qui sont souvent classifiées selon leur taille. Les petites vésicules extracellulaires, d’une taille comprise entre 30 et 150 nm, comprennent les exosomes, formés par invagination de la membrane des endosomes précoces, et les ectosomes, formés par bourgeonnement de la membrane plasmique. Dans le contexte tumoral, les vésicules extracellulaires ont été associées au processus métastatique, et joueraient un rôle dans l’immunosuppression et la résistance thérapeutique [5].
Le stress cellulaire induit par les infections virales entraîne généralement une augmentation de la quantité de vésicules extracellulaires produites et une modification de leur contenu par des molécules d’origine cellulaire ou virale [6]. Certaines études montrent notamment que les particules produites dans des contextes d’infection virale présentent des caractéristiques partagées entre les vésicules extracellulaires et les particules virales. Ces particules peuvent en effet contenir à la fois des protéines cellulaires et des protéines virales, voire des fragments du génome viral, ce qui crée un continuum d’entités difficiles à définir précisément [7]. On connaît mal l’impact des vésicules extracellulaires sur la communication intercellulaire dans le contexte d’une infection par un virus oncolytique. Plusieurs équipes ont cependant montré que les produits des transgènes insérés dans le génome des virus oncolytiques, par exemple des molécules de la famille du facteur de nécrose tumorale ( tumor-necrosis factor, TNF), ou des micro-ARN, peuvent être chargés dans les vésicules extracellulaires des cellules tumorales infectées et avoir un impact thérapeutique [8, 9].
Nous avons cherché à caractériser l’influence de deux virus oncolytiques, le virus de la stomatite vésiculaire et le virus de la vaccine, sur les propriétés des vésicules extracellulaires produites par des cellules humaines de mélanome ou de cancers thoraciques [7]. Nous avons d’abord montré que les cellules tumorales infectées par ces virus produisaient de plus grandes quantités de vésicules extracellulaires que les cellules non infectées (Figure 1). Ces vésicules extracellulaires – ou plutôt ce continuum allant des vésicules extracellulaires aux particules virales – contiennent des protéines d’origine virale abondamment produites par la cellule infectée, notamment la glycoprotéine G dans le cas du virus de la stomatite vésiculaire. Cette protéine est très utilisée en vectorisation virale puisque son large tropisme permet de transduire efficacement une grande variété de types cellulaires en favorisant notamment la fusion membranaire et l’accès au cytoplasme des cellules cibles. Le transfert de protéines et d’acides nucléiques d’une cellule à une autre via les vésicules extracellulaires étant un processus relativement rare dans des conditions normales, nous nous sommes demandé si la présence de la glycoprotéine G à la surface de ces vésicules modifiait leur capacité à transférer des biomolécules aux cellules environnantes. Dans un modèle de sphéroïdes tumoraux contenant des cellules immunitaires rapportrices, nous avons montré que les vésicules extracellulaires possédant cette protéine pouvaient délivrer leur contenu à ces cellules, même lorsque celles-ci étaient situées dans des couches profondes des sphéroïdes.
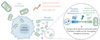 |
Figure 1 Les virus oncolytiques modifient la production des vésicules extracellulaires par les cellules tumorales. L’infection des cellules tumorales par un virus oncolytique provoque une augmentation de la production de vésicules extracellulaires par ces cellules. Ces vésicules constituent un continuum de particules qui possèdent des marqueurs des vésicules extracellulaires canoniques (tétraspanines, etc) et des particules virales (glycoprotéines d’enveloppe, génomes ADN ou ARN, etc), ce qui modifie leur capacité de transfert intercellulaire et leur immunogénicité. Figure créée avec BioRender. |
Une analyse protéomique différentielle de cellules de mélanome infectées ou non par le virus de la stomatite vésiculaire ou par le virus de la vaccine a montré, dans le cas de l’infection par le virus de la stomatite vésiculaire, un enrichissement des protéines liées à la réponse antivirale. Dans cette condition, nous avons ainsi identifié des protéines codées par des gènes stimulés par les interférons de type I, en accord avec l’induction d’une réponse antivirale innée dans les cellules infectées, ainsi que d’autres protéines associées à la réponse immunitaire adaptative (complexe majeur d’histocompatibilité de classe I, antigènes tumoraux, etc). En revanche, pour le virus de la vaccine, nous n’avons pas identifié de protéines liées à l’immunité, mais davantage de protéines associées au trafic intracellulaire et au transport vésiculaire.
Nous avions précédemment montré que les vésicules extracellulaires produites par des cellules humaines de mélanome avaient une activité inhibitrice sur l’activité de lymphocytes T anti-tumoraux [10]. En prenant en considération les facteurs immunogènes identifiés dans l’analyse protéomique, nous nous sommes demandé si les vésicules extracellulaires produites dans un contexte oncolytique pouvaient contrebalancer cette immunosuppression. En utilisant deux clones de lymphocytes T CD8+ spécifiques de l’antigène de mélanome Melan-A, nous avons montré que l’infection oncolytique et la modification associée des vésicules extracellulaires produites par les cellules tumorales annulait effectivement l’effet immunosuppresseur des vésicules extracellulaires et restaurait partiellement l’activité de ces lymphocytes. Les fonctions effectrices des cellules T CD8+ étaient améliorées, en particulier la sécrétion de granzyme-B, ainsi que leurs propriétés lytiques vis-à-vis de cellules tumorales. En revanche, nous n’avons pas constaté de modification de la sécrétion des cytokines immunostimulatrices interféron-γ et TNF-α.
Nous avons donc montré que l’infection oncolytique de cellules tumorales humaines a un réel impact sur la biogenèse des vésicules extracellulaires en augmentant leur sécrétion et en modifiant leur contenu. Nos résultats indiquent que le chargement de protéines d’origine virale, issues du génome viral per se ou codées par les transgènes exogènes, peut modifier les propriétés de ces vésicules extracellulaires : ces protéines amélioreraient notamment le transfert de biomolécules vers d’autres cellules non infectées, en particulier grâce à leurs propriétés fusogènes facilitant l’échappement endosomique et le transfert cytoplasmique. Les virus oncolytiques influenceraient donc les communications intercellulaires impliquant les vésicules extracellulaires, y compris dans des environnements complexes, comme nous l’avons montré avec le modèle des sphéroïdes. Certains résultats indiquent en outre que le transfert de protéines immunogènes, corrélé à l’induction ou au contrôle de la réponse antivirale innée par les virus oncolytiques, participe à l’effet thérapeutique de ces virus.
Nos résultats confirment ceux d’études précédentes montrant que les protéines codées par des virus oncolytiques peuvent être chargées dans les vésicules extracellulaires [8], et indiquent que ce processus est commun à différents types de virus et observable dans différents modèles tumoraux. Il restera à élucider les mécanismes du chargement de ces protéines dans les vésicules extracellulaires, même si nos observations suggèrent un chargement passif et donc un contenu des vésicules extracellulaires similaire à celui de la cellule d’origine. Les virus oncolytiques seraient donc des outils de choix pour exploiter les communications intercellulaires impliquant les vésicules extracellulaires. La modification précise de ces virus pourrait permettre d’utiliser les vésicules extracellulaires pour disséminer des protéines et acides nucléiques thérapeutiques intracellulaires dans l’ensemble du microenvironnement tumoral.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Bommareddy PK, Shettigar M, Kaufman HL. Integrating oncolytic viruses in combination cancer immunotherapy. Nat Rev Immunol 2018 ; 18 : 498–513. [Google Scholar]
- Andtbacka RHI, Kaufman HL, Collichio F, et al. Talimogene laherparepvec improves durable response rate in patients with advanced melanoma. J Clin Oncol 2015 ; 33 : 2780–8. [Google Scholar]
- Todo T, Ito H, Ino Y, et al. Intratumoral oncolytic herpes virus G47∆ for residual or recurrent glioblastoma: a phase 2 trial. Nat Med 2022 ; 28 : 1630–9. [Google Scholar]
- Niel G van, D’Angelo G, Raposo G. Shedding light on the cell biology of extracellular vesicles. Nat Rev Mol Cell Biol 2018 ; 19 : 213–28. [CrossRef] [PubMed] [Google Scholar]
- Marar C, Starich B, Wirtz D. Extracellular vesicles in immunomodulation and tumor progression. Nat Immunol 2021 ; 22 : 560–70. [CrossRef] [PubMed] [Google Scholar]
- Moulin C, Crupi MJF, Ilkow CS, et al. Extracellular vesicles and viruses: Two intertwined entities. Int J Mol Sci 2023 ; 24 : 1036. [Google Scholar]
- Hirigoyen U, Guilbaud C, Krejbich M, et al. Oncolytic viruses alter the biogenesis of tumor extracellular vesicles and influence their immunogenicity. Mol Ther Oncol 2024 ; 32 : 200887. [Google Scholar]
- Labani-Motlagh A, Naseri S, Wenthe J, et al. Systemic immunity upon local oncolytic virotherapy armed with immunostimulatory genes may be supported by tumor-derived exosomes. Mol Ther Oncolytics 2021 ; 20 : 508–18. [Google Scholar]
- Wedge M-E, Jennings VA, Crupi MJF, et al. Virally programmed extracellular vesicles sensitize cancer cells to oncolytic virus and small molecule therapy. Nat Commun 2022 ; 13 : 1898. [Google Scholar]
- Vignard V, Labbé M, Marec N, et al. MicroRNAs in tumor exosomes drive immune escape in melanoma. Cancer Immunol Res 2020 ; 8 : 255–67. [Google Scholar]
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Les virus oncolytiques modifient la production des vésicules extracellulaires par les cellules tumorales. L’infection des cellules tumorales par un virus oncolytique provoque une augmentation de la production de vésicules extracellulaires par ces cellules. Ces vésicules constituent un continuum de particules qui possèdent des marqueurs des vésicules extracellulaires canoniques (tétraspanines, etc) et des particules virales (glycoprotéines d’enveloppe, génomes ADN ou ARN, etc), ce qui modifie leur capacité de transfert intercellulaire et leur immunogénicité. Figure créée avec BioRender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




