| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
|
|
|---|---|---|
| Page(s) | 839 - 842 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2025211 | |
| Published online | 12 décembre 2025 | |
Récupération d’un circuit neuronal fonctionnel après une lésion du nerf optique chez la souris adulte
Neuronal circuit recovery after an optic nerve lesion in the adult mouse
Univ. Grenoble Alpes, Inserm U1216, Grenoble Institut des neurosciences, Grenoble, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
**
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Le développement du système nerveux central inclut la formation des circuits neuronaux. Les trajectoires stéréotypées des faisceaux d’axones sont déterminées en majeure partie grâce à la présence, dans les zones clés (comme la ligne médiane par exemple), d’une combinaison de facteurs de guidage [1]. Dans l’organisme adulte, ces circuits peuvent être rompus par diverses lésions du système nerveux central, et les axones ne sont alors pas capables de régénérer spontanément, ce qui provoque des pertes fonctionnelles irréversibles. Ainsi, l’un des grands défis pour la médecine neurologique est d’obtenir la reconstruction de circuits neuronaux fonctionnels. Depuis la découverte, en 2008, que l’activation de la voie de signalisation impliquant mTOR (mammalian target of rapamycin) dans les neurones du système nerveux central induit la régénération axonale [2], diverses autres voies de signalisation impliquées dans la régénération ont été identifiées. Aujourd’hui, plusieurs modèles de régénération axonale à longue distance permettent notamment la repousse de fibres nerveuses depuis la rétine jusqu’au cerveau chez la souris adulte [3-7]. Toutefois, la plupart des axones en cours de régénération présentent de graves défauts de navigation, empêchant la reformation d’un circuit fonctionnel [3, 5, 6], ce qui suggère l’existence d’informations topographiques de guidage axonal spécifiques du cerveau mature.
Pour tenter d’identifier certains de ces signaux de guidage, nous avons réalisé une cartographie moléculaire, par spectrométrie de masse, des principaux noyaux impliqués dans le traitement de l’information visuelle chez l’adulte [8]. Nous avons découvert que ces noyaux produisent un grand nombre de facteurs de guidage et de molécules impliquées dans la formation de circuits neuronaux. La plupart de ces facteurs de guidage ont été décrits comme ayant une activité répulsive lors du développement, et nous avons montré que les neurones en cours de régénération intègrent ces signaux répulsifs, expliquant ainsi en partie les défauts de trajectoires axonales constatés [8].
Nous avons alors cherché à savoir s’il était possible de rétablir des circuits neuronaux fonctionnels en permettant un guidage axonal approprié dans le cerveau adulte. Nous avons choisi comme modèle d’étude le circuit neuronal entre la rétine et le noyau suprachiasmatique [9]. Ce noyau situé dans la partie ventrale de l’hypothalamus, juste au-dessus du chiasma optique, est le premier noyau sur le trajet du nerf optique. Il n’est pas impliqué dans la formation d’images, mais dans le contrôle des rythmes circadiens. Il est innervé exclusivement par une souspopulation de cellules ganglionnaires de la rétine : les cellules ganglionnaires intrinsèquement photosensibles, qui produisent le photopigment mélanopsine [10]. Une autre particularité de ces cellules est leur résilience à la lésion, puisque leur taux de survie après une lésion est très supérieur à celui des autres sous-populations de cellules ganglionnaires [11].
Nous avons donc analysé la régénération axonale et l’innervation du noyau suprachiasmatique après une lésion du nerf optique. L’activation simultanée des voies mTOR, JAK/STAT et c-myc permet une régénération axonale à très longue distance [3]. En effet, quatre semaines après la lésion, les axones en cours de régénération dépassent le chiasma optique et naviguent jusqu’aux noyaux les plus éloignés. Cependant, malgré cette régénération intensive, très peu d’axones pénètrent dans les noyaux du système visuel, notamment dans le noyau suprachiasmatique (Figure 1B-C). L’analyse de souris qui produisent la protéine fluorescente verte (green fluorescent protein, GFP) sous le contrôle du promoteur du gène de la mélanopsine montre que les cellules ganglionnaires intrinsèquement photosensibles de la rétine non seulement survivent à la lésion, mais aussi sont capables de régénérer leurs axones jusqu’au noyau suprachiasmatique. Ce résultat a été confirmé par un traçage rétrograde du circuit : l’injection de la sousunité B de la toxine cholérique dans le chiasma optique a permis d’identifier, dans la rétine, des cellules ganglionnaires intrinsèquement photosensibles marquées par la toxine. Ainsi, les axones de ces cellules régénèrent, mais ne sont pas capables d’innerver leur noyau cible, le noyau suprachiasmatique, qui semble exercer sur eux une action répulsive. Celle-ci a pu être confirmée dans des cocultures organotypiques d’explants de rétine mature dans lesquels les voies mTOR, JAK/STAT et c-myc étaient activées, avec des explants de noyau suprachiasmatique mature : les axones qui sortent de l’explant rétinien poussent du côté opposé à l’explant du noyau suprachiasmatique. À l’origine de cette activité répulsive du noyau suprachiasmatique, nous avons identifié les molécules de guidage Slit (Slit 1/2/3), qui agissent en se liant à leurs récepteurs Robo (Robo 1/2) situés sur le cône de croissance des axones, et dont l’activité répulsive sur les axones au cours du développement était connue [12]. De plus, l’inhibition de cette signalisation lors du développement du système visuel conduit aux mêmes phénotypes que ceux observés chez l’animal adulte dans un contexte de régénération axonale : une désorganisation du chiasma optique et une perturbation des trajectoires axonales [13]. Les cocultures organotypiques avec un explant de noyau suprachiasmatique n’exprimant plus les molécules Slit perdent l’effet répulsif sur les axones des cellules ganglionnaires rétiniennes précédemment constaté. Nous avons ensuite modifié cette signalisation in vivo en inhibant l’expression des récepteurs Robo1/2 dans les cellules ganglionnaires de la rétine en cours de régénération, et avons alors constaté que leurs axones pénétraient dans le noyau suprachiasmatique (Figure 1B,C). Cependant, ils y pénètrent par le coté dorsal de ce noyau, alors que lors du développement normal, ils y pénètrent par le côté ventral. Néanmoins, en utilisant des virus de la rage modifiés, capables de traverser une connexion synaptique, nous avons montré que ces axones régénérés forment des synapses fonctionnelles avec les neurones du noyau suprachiasmatique. Incidemment, une autre sous-population de cellules ganglionnaires de la rétine, les cellules ganglionnaires α, projetaient leurs axones de façon ectopique dans ce noyau également.
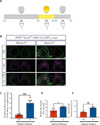 |
Figure 1 Récupération fonctionnelle après réinnervation du noyau suprachiasmatique. A. Schéma représentant la procédure expérimentale d’activation du noyau suprachiasmatique (NSC). Les souris sont maintenues dans l’obscurité durant 4 heures. Elles sont ensuite placées dans la lumière durant 30 minutes, puis replacées dans l’obscurité pendant 30 minutes avant de prélever leur cerveau. B. Images par microscopie confocale de coupes coronales du noyau suprachiasmatique, 4 semaines après la lésion du nerf optique, d’une souris PTENf/f/Socs3f/f/Robo1+/+/Robo2+/+ (exprimant les récepteurs Robo 1 et 2 dans les cellules ganglionnaires de la rétine) et d’une souris PTENf/f/Socs3f/f/Robo1-/-/Robo2f/f (privée de l’expression des récepteurs Robo 1 et 2 dans les cellules ganglionnaires de la rétine) qui ont reçu une injection intra-oculaire de AAV-Cre ; CNTF (facteur neurotrophique ciliaire); c-myc. La protéine c-Fos est colorée en magenta par immunomarquage avec un anticorps fluorescent, et les axones en cours de régénération sont colorés en vert par marquage avec la sous-unité B de la toxine cholérique (CTB). Barre d’échelle : 100 mm. C. Diagramme quantifiant la proportion des axones qui pénètrent dans le noyau suprachiasmatique. Comparaison des proportions observées par le test du χ2 (*** : p < 0,001). D. Diagramme quantifiant le nombre de cellules exprimant c-Fos dans le noyau suprachiasmatique. E. Diagramme quantifiant l’intensité de fluorescence de la protéine c-Fos dans les cellules du noyau suprachiasmatique. Comparaison des moyennes entre les deux groupes de souris par le test t (* : p < 0,05 ; ** : p < 0,01). |
Pour tester la fonctionnalité de ce circuit neuronal régénéré, nous avons soumis les souris à une stimulation lumineuse et analysé un marqueur de la réponse des neurones du noyau suprachiasmatique à cette stimulation (Figure 1A) : la forte augmentation transitoire de l’expression du protooncogène c-Fos. Aucune production de la protéine c-Fos n’est détectée lorsque les souris sont gardées dans l’obscurité ou après une lésion de leurs deux nerfs optiques. Nous avons ensuite effectué la même expérience chez les souris dont nous avions induit la régénération axonale (par activation des signalisations mTOR, Jak-STAT, et myc) avec ou sans inhibition de l’expression des récepteurs Robo 1 et 2 dans les cellules ganglionnaires de la rétine. Comme attendu, l’activation de la régénération axonale seule n’a pas permis d’augmenter la synthèse de c-Fos dans le noyau suprachiasmatique après la stimulation lumineuse (Figure 1A,B,D,E). En revanche, l’activation de de la régénération axonale accompagnée de l’inhibition de la signalisation Slit/Robo a permis l’augmentation de la synthèse de c-Fos, indiquant la transmission de l’information lumineuse (Figure 1). Enfin, nous avons testé la récupération fonctionnelle de ce circuit neuronal par une analyse comportementale du cycle circadien de l’activité des souris dans ces différentes conditions. Avant la lésion des nerf optiques, l’activité de toutes les souris présente une période d’environ 24 heures, avec une alternance entre l’intense activité nocturne et l’inactivité diurne. Après la lésion des deux nerfs optiques, les souris perdent cette alternance d’activité entre la nuit et le jour et la périodicité de 24 heures, mais si l’on rétablit la connexion entre la rétine et le noyau suprachiasmatique en inhibant la signalisation Slit/Robo, ces souris retrouvent progressivement une périodicité d’activité de 24 heures, même si elles restent incapables de distinguer visuellement les périodes de jour et de nuit.
En inhibant la signalisation Slit/Robo chez la souris adulte, il a donc été possible, après une lésion du nerf optique, de reformer un circuit neuronal fonctionnel depuis la rétine jusqu’au noyau suprachiasmatique. Cependant, d’autres mécanismes non encore élucidés sont impliqués dans le processus physiologique d’innervation de ce noyau par les axones des neurones ganglionnaires de la rétine au cours du développement, comme en témoigne notamment l’anomalie du site de pénétration des axones dans le noyau au cours de la régénération post-lésionnelle.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Nawabi H, Castellani V. Axonal commissures in the central nervous system: how to cross the midline? Cell Mol Life Sci 2011 ; 68 : 2539–53. [Google Scholar]
- Park KK, Liu K, Hu Y, et al. Promoting axon regeneration in the adult CNS by modulation of the PTEN/mTOR pathway. Science 2008 ; 322 : 963–6. [Google Scholar]
- Belin S, Nawabi H, Wang C, et al. Injury-induced decline of intrinsic regenerative ability revealed by quantitative proteomics. Neuron 2015 ; 86 : 1000–14. [Google Scholar]
- de Lima S, Koriyama Y, Kurimoto T, et al. Full-length axon regeneration in the adult mouse optic nerve and partial recovery of simple visual behaviors. Proc Natl Acad Sci USA 2012 ; 109 : 9149–54. [Google Scholar]
- Lim JH, Stafford BK, Nguyen PL, et al. Neural activity promotes long-distance, target-specific regeneration of adult retinal axons. Nat Neurosci 2016 ; 19 : 1073–84. [Google Scholar]
- Luo X, Salgueiro Y, Beckerman SR, et al. Three-dimensional evaluation of retinal ganglion cell axon regeneration and pathfinding in whole mouse tissue after injury. Exp Neurol 2013 ; 247 : 653–62. [Google Scholar]
- Sun F, Park KK, Belin S, et al. Sustained axon regeneration induced by co-deletion of PTEN and SOCS3. Nature 2011 ; 480 : 372–5. [Google Scholar]
- Vilallongue N, Schaeffer J, Hesse AM, et al. Guidance landscapes unveiled by quantitative proteomics to control reinnervation in adult visual system. Nat Commun 2022 ; 13 : 6040. [Google Scholar]
- Delpech C, Schaeffer J, Vilallongue N, et al. Axon guidance during mouse central nervous system regeneration is required for specific brain innervation. Dev Cell 2024 ; 59 : 3213-28.e8. [Google Scholar]
- Hattar S, Liao HW, Takao M, et al. Melanopsin-containing retinal ganglion cells: architecture, projections, and intrinsic photosensitivity. Science 2002 ; 295 : 1065–70. [CrossRef] [PubMed] [Google Scholar]
- Tran NM, Shekhar K, Whitney IE, et al. Single-cell profiles of retinal ganglion cells differing in resilience to injury reveal neuroprotective genes. Neuron 2019 ; 104 : 1039-55 e12. [Google Scholar]
- Blockus H, Chedotal A. Slit-Robo signaling. Development 2016 ; 143 : 3037–44. [Google Scholar]
- Plump AS, Erskine L, Sabatier C, et al. Slit1 and Slit2 cooperate to prevent premature midline crossing of retinal axons in the mouse visual system. Neuron 2002 ; 33 : 219–32. [Google Scholar]
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Récupération fonctionnelle après réinnervation du noyau suprachiasmatique. A. Schéma représentant la procédure expérimentale d’activation du noyau suprachiasmatique (NSC). Les souris sont maintenues dans l’obscurité durant 4 heures. Elles sont ensuite placées dans la lumière durant 30 minutes, puis replacées dans l’obscurité pendant 30 minutes avant de prélever leur cerveau. B. Images par microscopie confocale de coupes coronales du noyau suprachiasmatique, 4 semaines après la lésion du nerf optique, d’une souris PTENf/f/Socs3f/f/Robo1+/+/Robo2+/+ (exprimant les récepteurs Robo 1 et 2 dans les cellules ganglionnaires de la rétine) et d’une souris PTENf/f/Socs3f/f/Robo1-/-/Robo2f/f (privée de l’expression des récepteurs Robo 1 et 2 dans les cellules ganglionnaires de la rétine) qui ont reçu une injection intra-oculaire de AAV-Cre ; CNTF (facteur neurotrophique ciliaire); c-myc. La protéine c-Fos est colorée en magenta par immunomarquage avec un anticorps fluorescent, et les axones en cours de régénération sont colorés en vert par marquage avec la sous-unité B de la toxine cholérique (CTB). Barre d’échelle : 100 mm. C. Diagramme quantifiant la proportion des axones qui pénètrent dans le noyau suprachiasmatique. Comparaison des proportions observées par le test du χ2 (*** : p < 0,001). D. Diagramme quantifiant le nombre de cellules exprimant c-Fos dans le noyau suprachiasmatique. E. Diagramme quantifiant l’intensité de fluorescence de la protéine c-Fos dans les cellules du noyau suprachiasmatique. Comparaison des moyennes entre les deux groupes de souris par le test t (* : p < 0,05 ; ** : p < 0,01). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




