| Issue |
Med Sci (Paris)
Volume 41, Number 12, Décembre 2025
La santé des femmes : au-delà de la procréation
|
|
|---|---|---|
| Page(s) | 975 - 985 | |
| Section | Maladies cardiovasculaires | |
| DOI | https://doi.org/10.1051/medsci/2025225 | |
| Published online | 6 janvier 2026 | |
Particularités de l’infarctus du myocarde chez la femme
Features of myocardial infarction in women
1
Fédération de cardiologie, Hôpital de la Croix-Rousse et Hôpital Lyon Sud, Institut de cardiologie, Hospices Civils de Lyon, Lyon, France
2
Service de Physiologie, Hôpital Bichat, Assistance Publique des Hôpitaux de Paris, Paris
3
Université Paris Cité, INSERM U1148, LVTS, Paris, France
4
Université de Lyon, CREATIS, CNRS UMR5220, INSERM U1044, INSA-Lyon, Université Claude Bernard Lyon 1, Lyon, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
L’infarctus du myocarde est un problème majeur de santé publique chez les femmes. Les taux d’hospitalisation sont en augmentation, en particulier chez les jeunes femmes. Cette tendance est probablement liée à une prévalence croissante des facteurs de risque cardiovasculaires et à des maladies spécifiques susceptibles d’augmenter le risque d’infarctus du myocarde : ménopause précoce, contraception œstroprogestative, endométriose et radiothérapie thoracique pour cancer du sein. D’un point de vue physiopathologique, les femmes présentent des caractéristiques distinctes de celles des hommes. Une proportion plus élevée d’infarctus du myocarde sans obstruction coronaire est observée chez la femme, notamment, la dissection spontanée des artères coronaires, qui peut parfois survenir pendant la grossesse. Les femmes ont des artères coronaires et radiales plus petites, avec des tortuosités plus fréquentes, ce qui peut compliquer les procédures interventionnelles. De plus, la prise en charge de l’infarctus du myocarde chez les femmes est inégale car : elles ont tendance à consulter plus tard et sont donc moins susceptibles de bénéficier de stratégies invasives (revascularisation ou pontage aorto-coronarien). En conclusion, l’infarctus du myocarde chez la femme présente de nombreuses spécificités cliniques et physiopathologiques. Des efforts supplémentaires sont nécessaires pour adapter les soins aux spécificités féminines et garantir une prise en charge équitable.
Abstract
Myocardial infarction is a major public health concern for women. Hospitalization rates are increasing, particularly among young women. This trend is probably linked to the growing prevalence of cardiovascular risk factors and specific conditions that can increase the risk of myocardial infraction, such as early menopause, estrogen-progestogen contraception, endometriosis and chest radiation therapy for breast cancer. From a patho-physiological perspective, women have distinct characteristics. They have a higher proportion of myocardial infraction without significant coronary obstruction, including spontaneous coronary dissection, which can occur during pregnancy. Women also have smaller coronary and radial arteries with more frequent tortuosity, which can complicate interventional procedures. Additionally, disparities in the management of myocardial infraction in women have been observed. They tend to seek medical attention later and are less likely to benefit from invasive strategies, such as revascularization or coronary artery bypass grafting. In conclusion, myocardial infraction in women have many clinical and pathophysiological specificities. Additional efforts are needed to improve care and ensure equality in treatment by taking into account the specific characteristics of women.
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.

Vignette (© Freepik)
Longtemps considérée comme une maladie masculine, la maladie coronarienne constitue pourtant un enjeu majeur de santé publique chez la femme. En France, les maladies cardiovasculaires représentent la première cause de mortalité féminine, les cardiopathies ischémiques étant en deuxième position derrière les maladies cérébrovasculaires. L’infarctus du myocarde est classé en deux grandes catégories selon l’aspect de l’électrocardiogramme (ECG) : le STEMI (ST-elevation myocardial infarction ou syndrome coronarien aigu1 avec sus-décalage du segment ST (ou SCA ST+), caractérisé par une élévation persistante du segment ST2 sur l’ECG, traduisant une obstruction complète d’une artère coronaire, et le NSTEMI (non-ST-elevation myocardial infarction ou SCA ST-), sans élévation du segment ST, mais avec d’autres anomalies de l’ECG et une élévation des biomarqueurs cardiaques, correspondant le plus souvent à une obstruction partielle d’une artère coronaire [1] (→).
(→) Voir m/s n° 4, 2004, page 402
Après standardisation sur l’âge, les taux d’hospitalisation pour infarctus du myocarde restent inférieurs chez les femmes par rapport aux hommes, celles-ci représentant entre un quart et un tiers des patients admis (25 % pour les STEMI et 30 % pour les NSTEMI) [2]. Cependant, une augmentation préoccupante est observée chez les femmes de moins de 65 ans. Entre 2008 et 2013, le taux d’hospitalisation pour maladie coronarienne des femmes de 45 à 54 ans a progressé de 4,8 % par an [3]. Cette tendance pourrait être, en partie, expliquée par une augmentation de l’exposition aux facteurs de risque cardiovasculaires, notamment le tabagisme et l’obésité. Une meilleure compréhension des spécificités de l’infarctus du myocarde chez la femme est donc essentielle pour adapter les stratégies de prévention, de diagnostic et de prise en charge.
L’objectif de cet article est de comparer la présentation clinique, l’anatomie coronaire et la prise en charge selon le sexe afin de mettre en lumière les spécificités de l’infarctus du myocarde chez la femme.
Présentation clinique
L’infarctus du myocarde présente des particularités épidémiologiques notables chez la femme, notamment en ce qui concerne l’âge, les comorbidités et les facteurs de risque cardiovasculaires.
Un âge moyen plus élevé à l’hospitalisation et au décès
Les femmes hospitalisées pour un syndrome coronarien aigu sont en moyenne plus âgées d’une dizaine d’années que les hommes (en 2019, 75 ans pour les femmes contre 67 ans pour les hommes) [3-5].
De même, l’âge moyen au décès par infarctus du myocarde est plus élevé chez les femmes (85 ans) que chez les hommes (76,5 ans) [6]. Cette différence d’âge pourrait s’expliquer en partie par une prévalence plus marquée des facteurs de risque cardiovasculaires chez les hommes à un âge plus jeune, notamment par une dyslipidémie plus fréquente et un tabagisme plus important, comme le suggère l’étude INTERHEART [7]. Toutefois, la proportion de femmes jeunes hospitalisées pour infarctus du myocarde reste significative [2].
Des comorbidités plus fréquentes
Les femmes hospitalisées pour infarctus du myocarde présentent généralement un profil de comorbidités plus marqué que les hommes, avec des taux plus élevés d’obésité, de diabète, d’hypertension artérielle et de dyslipidémie. En revanche, le tabagisme reste moins répandu chez les femmes, bien qu’il constitue un facteur de risque majeur [2, 4, 5, 8]. Par ailleurs, les femmes ont souvent moins d’antécédents coronariens que les hommes [2, 8].
Ainsi, les déterminants de la maladie coronarienne semblent similaires entre les hommes et les femmes, mais sont observés à des âges différents.
Les symptômes
L’infarctus du myocarde chez les femmes se manifeste par des symptômes qui peuvent différer de ceux observés chez les hommes, rendant parfois le diagnostic plus complexe et retardant la prise en charge dont la rapidité peut améliorer le pronostic de la maladie.
Parmi les symptômes, la douleur thoracique reste fréquente mais est plus volontiers atypique (localisation au cou, à la mâchoire, au dos, ou associée à une grande fatigue ou à des troubles digestifs) [2, 9]. Les femmes présentent souvent une forme clinique plus sévère à l’admission, avec une fréquence accrue d’insuffisance cardiaque, jusqu’au choc cardiogénique (correspondant à une défaillance circulatoire aiguë, avec chute du débit cardiaque en lien avec une dysfonction cardiaque sévère) [8, 10].
L’infarctus du myocarde à « coronaires saines »
L’infarctus du myocarde dit « à coronaires saines » ou MINOCA (myocardial infarction with non-obstructive coronary arteries) désigne une ischémie3 myocardique survenant en l’absence de sténose4 coronaire significative observée au cours de la coronarographie. Cette entité concerne préférentiellement les femmes et pose des défis diagnostiques et thérapeutiques spécifiques.
La présentation clinique en cas de MINOCA est similaire à celle d’un infarctus du myocarde par occlusion coronaire, la plainte principale étant la douleur thoracique. Toutefois, il est plus fréquent chez les femmes : l’étude VIRGO (variation in recovery: role of gender on outcomes of young AMI patients) rapporte une prévalence cinq fois plus élevée chez celles-ci (tableau 1) [11]. Les patientes atteintes de MINOCA présentent souvent moins de facteurs de risque cardiovasculaires traditionnels et moins de modifications de l’électrocardiogramme [11, 12].
Type d’infarctus en fonction du sexe. On constate une prévalence plus importante des infarctus à « coronaires saines » chez les femmes, qui représentent jusqu’à 15 % des infarctus selon les séries, soit 5 fois plus que les hommes. IDM : Infarctus du myocarde ; STEMI : syndrome coronarien aigu avec sus-décalage du segment ST ; NSTEMI : syndrome coronarien aigu sans sus-décalage du segment ST ; MINOCA : myocardial infarction with non obstructive coronary arteries.
Les MINOCA peuvent être secondaires à : une rupture de plaque athéromateuse sans occlusion artérielle, un vasospasme coronaire, une dysfonction microvasculaire, un embole5 d’origine intracardiaque, une dissection coronaire spontanée également appelée SCAD (spontaneous coronary artery dissection), ou encore un infarctus du myocarde de type 2 (déséquilibre entre les apports et la consommation d’oxygène au niveau coronaire).
La dissection coronaire spontanée : une cause fréquente chez la femme jeune
La dissection spontanée des artères coronaires est une cause spécifique de MINOCA rare (moins de 1 % des syndromes coronariens aigus). Elle correspond à une déchirure de la paroi d’une artère coronaire, créant un faux chenal sanguin au sein de la paroi qui peut réduire, voire bloquer, le flux sanguin. Contrairement aux infarctus classiques, la dissection coronaire spontanée touche préférentiellement les femmes jeunes (moins de 50 ans) avec peu de comorbidités [13, 14]. Certains travaux suggèrent l’implication de mécanismes héréditaires, avec certains variants génétiques prédisposant à la dissection coronaire [15] (→).
(→) Voir m/s n° 8-9, 2019, page 605
La figure 1 illustre des exemples de dissections coronaires en angiographie.
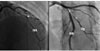 |
Figure 1 Images de dissection coronaire en coronarographie. À gauche : dissection coronaire sur l’artère interventriculaire antérieure avec flap intimal (flèche). À droite : dissection coronaire étendue sur l’artère interventriculaire antérieure proximale avec extension sur la première diagonale. IVA : interventriculaire antérieure ; Dg : diagonale. |
L’infarctus du myocarde chez la femme présente donc des spécificités épidémiologiques, cliniques et physiopathologiques, avec des femmes souvent plus âgées ayant plus de comorbidités et parfois des symptômes atypiques.
Le syndrome de tako-tsubo
Également appelé « cardiomyopathie de stress », on l’évoque en échographie devant un ventricule gauche en forme d’amphore pendant la systole, évoquant un piège à pieuvre japonais appelé « tako-tsubo ». Dans sa forme classique, on observe une sidération de l’apex du ventricule gauche et une hyperkinésie des segments basaux. Il fait partie de principaux diagnostics différentiels de l’infarctus du myocarde chez la femme. Cette maladie touche jusqu’à 90 % des patientes. Dans les deux tiers des cas, on retrouve un facteur déclenchant lié soit à une émotion forte (décès, agression, accident…), soit à un stress physique (chirurgie, affection du système nerveux central, détresse respiratoire,…). La physiopathologie est complexe, probablement liée à un déséquilibre sympatho-vagal favorisé par la carence œstrogénique, entraînant une libération intense de catécholamine ayant des effets myocardique [16] (→).
(→) Voir m/s n° 2, 2024, page 130
Le syndrome de tako-tsubo peut se compliquer initialement d’une insuffisance cardiaque ou de troubles du rythme, mais l’évolution est généralement favorable, avec une récupération myocardique. Le traitement standard repose généralement sur l’introduction de bétabloquants et d’inhibiteurs de l’enzyme de conversion de l’angiotensinogène6 bien que le niveau de preuve scientifique reste limité [17].
Éléments gynécologiques modulateurs du risque coronarien
Impact de la contraception
Les pilules microprogestatives seules ne semblent pas augmenter le risque de cardiopathie ischémique7, indépendamment de la génération de progestatif employée [18]. Elles constituent ainsi une option contraceptive privilégiée pour les femmes présentant des facteurs de risque cardiovasculaires.
L’association d’un œstrogène et d’un progestatif peut, en revanche, entraîner une augmentation du risque d’événements cardiovasculaires, en particulier les accidents vasculaires cérébraux (AVC) et les infarctus du myocarde (avec une augmentation du risque pouvant aller jusqu’à 2,5 fois) [18, 19].
Si le risque absolu reste faible chez les femmes jeunes et en bonne santé, il doit être pris en compte lors de la prescription des contraceptifs, notamment en présence de facteurs de risque cardiovasculaires associés.
La grossesse
Bien que rare, l’infarctus du myocarde pendant la grossesse représente une complication grave.
L’infarctus du myocarde survient dans environ 0,05 % des grossesses, avec une augmentation progressive du risque au cours de la grossesse, le risque étant maximal en post-partum (jusqu’à 0,2 %) [20]. Plusieurs facteurs de risque ont été identifiés, notamment : l’âge maternel avancé (supérieur à 30 ans), les comorbidités cardiovasculaires (telles que l’hypertension artérielle, le diabète et le tabagisme), les anomalies de la coagulation (thrombophilie8), ainsi que les complications obstétricales (telles que la prééclampsie9, les infections du post-partum, les transfusions, l’accouchement prématuré, et la mort fœtale) [21].
Physiopathologie et présentation clinique
Le principal mécanisme en cause est la dissection coronaire spontanée, responsable de 43 % des cas, suivie par l’athérosclérose et l’embolie coronaire. Une revue de 150 cas d’infarctus du myocarde survenus pendant la grossesse a montré une nette prédominance des formes STEMI (75 %), dans le territoire myocardique antérieur dans environ 70 % des cas.
Les mécanismes physiopathologiques impliqueraient les variations hormonales de la grossesse, notamment la progestérone et les œstrogènes, qui induisent des modifications de la matrice extracellulaire et un état inflammatoire favorisant la fragilisation vasculaire, avec relargage d’enzymes protéolytiques.
Pronostic et prise en charge
L’atteinte myocardique est souvent sévère, avec une altération de la fraction d’éjection ventriculaire gauche (FEVG < 40 %) chez plus de la moitié des patientes. La prise en charge doit être adaptée afin de limiter le risque de dissection coronaire iatrogène lors des procédures de revascularisation, celles-ci étant privilégiées en cas de STEMI ou de NSTEMI à haut risque, tout en restant limitées au strict nécessaire pour éviter une propagation de la dissection. On évite donc, en général, l’implantation de stents, car celle-ci peut aggraver la situation dans cette prise en charge très spécifique.
La ménopause
Modifications métaboliques et cardiovasculaires
On observe une altération du profil lipidique à la ménopause avec une augmentation du cholestérol total et des triglycérides ainsi qu’une diminution du HDL-cholestérol10. De plus, on constate une augmentation de la prévalence du syndrome métabolique, incluant l’obésité abdominale, le diabète et l’hypertension artérielle. Une rétention hydrosodée accentuée à la ménopause pourrait, au moins en partie, expliquer des valeurs tensionnels plus élevés [22, 23].
Impact de l’âge à la ménopause
Si certaines études ne montrent pas d’augmentation significative du risque coronaire chez les femmes ménopausées naturellement par rapport aux femmes en préménopause, le risque est doublé en cas d’ovariectomie bilatérale sans traitement hormonal substitutif. Cette augmentation du risque semble compensée par un traitement substitutif à base d’œstrogènes [24]. Par ailleurs, une ménopause précoce (avant 40 ans), qu’elle soit naturelle ou chirurgicale, est associée à une augmentation du risque cardiovasculaire par rapport aux femmes ménopausées après 40 ans, notamment en ce qui concerne les maladies coronariennes, dont le risque peut être accru de 30 à 50 % en comparaison avec celui des femmes ménopausées après 50 ans [25, 26].
La dysfonction endothéliale
On retrouve dans la littérature un effet protecteur rapporté des œstrogènes sur l’endothélium vasculaire [27]. En conditions normales, les œstrogènes protègent l’endothélium en favorisant la production d’oxyde nitrique, un vasodilatateur majeur, et en régulant l’action de l’endothéline-1 et de la noradrénaline, deux agents vasoconstricteurs. Lors de la carence hormonale induite par la ménopause, cette régulation est perdue : l’oxyde nitrique devient moins disponible, l’activité d’ET-1 (endothelin 1) et de la noradrénaline s’intensifie, et s’y ajoutent souvent un excès de stress oxydatif ainsi que des perturbations des voies de signalisation des récepteurs aux œstrogènes. Ainsi, l’arrêt de la production d’œstrogènes s’accompagne d’une dysfonction endothéliale qui s’amplifie au cours du temps, contribuant à une rigidité vasculaire accrue, à une susceptibilité accrue aux événements coronariens et aux vasospasmes [28].
Au total, bien que la ménopause soit associée à des altérations métaboliques défavorables, l’augmentation du risque coronarien apparaît principalement en cas de ménopause précoce.
Les bénéfices et les risques du traitement hormonal substitutif de la ménopause
Le traitement hormonal de la ménopause est classiquement envisagé comme une stratégie de prévention des maladies cardiovasculaires chez les femmes ménopausées.
Une réduction de l’incidence de la maladie coronaire est observée lorsque le traitement hormonal de la ménopause est initié dans les dix ans suivant la ménopause [29]. Par ailleurs, une diminution du risque d’insuffisance cardiaque a également été rapportée, à condition que le traitement soit introduit précocement [30].
Par contre, l’utilisation d’un traitement hormonal de la ménopause par voie orale peut entraîner une augmentation du risque thromboembolique veineux. Une initiation tardive dix ans après la ménopause ne présente pas de caractère de protection cardiovasculaire notamment sur la survenue de maladie coronaire [29, 30]. À l’inverse, le traitement hormonal de la ménopause semble avoir un effet protecteur lorsqu’il est débuté précocement après la ménopause et administré par voie transdermique. Toutefois, l’évaluation du profil de risque individuel est essentielle avant d’initier le traitement.
Impact de maladies spécifiques de la femme sur le risque cardiovasculaire
Le syndrome des ovaires polykystiques (SOPK)
Le syndrome des ovaires polykystiques touche entre 5 et 15 % des femmes en âge de procréer. Il s’agit d’une maladie hormonale dont le diagnostic repose sur la présence d’au moins deux critères parmi les trois suivants : oligo- ou anovulation, hyperandrogénisme clinique ou biologique, et ovaires polykystiques à l’échographie.
Chez les femmes atteintes du syndrome des ovaires polykystiques, le risque cardiovasculaire est classiquement considéré comme accru, en raison de la fréquence élevée de facteurs de risque métaboliques tels que l’hypertension artérielle, le diabète de type 2 et les anomalies lipidiques [25]. L’hypothèse d’un rôle aggravant de l’inflammation chronique, induite par le syndrome des ovaires polykystiques, sur les lésions myocardiques ischémiques a également été avancée [31].
Cependant, une méta-analyse portant sur 23 études a nuancé ce lien en mettant en évidence une augmentation du risque d’hypertension artérielle, de diabète de type 2 et du cholestérol total, sans pour autant démontrer une augmentation du risque d’événements coronariens. Cette absence de lien direct est corroborée par l’absence d’élévation significative des taux de LDL-cholestérol11 et de triglycérides dans cette population [32].
Ainsi, bien qu’une augmentation du risque cardiométabolique soit avérée chez les femmes atteintes de syndrome des ovaires polykystiques, elle ne semble pas se traduire par une augmentation manifeste du risque coronarien.
L’ endométriose
L’endométriose, qui touche environ une femme sur dix en France, est une maladie gynécologique caractérisée par la présence de tissu endométrial en dehors de la cavité utérine. Elle est aujourd’hui reconnue comme une maladie systémique, impliquant des mécanismes d’inflammation chronique et de stress oxydatif [33].
Plusieurs études ont suggéré un lien entre l’endométriose et un risque accru de maladies cardiovasculaires. Les données mettent en évidence une altération du profil lipidique et une tendance à l’augmentation du risque d’athérosclérose chez les femmes concernées [33]. Une méta-analyse de grande ampleur a rapporté une augmentation significative du risque de cardiopathie ischémique chez les patientes atteintes d’endométriose [34].
Ce surrisque semble persister indépendamment de l’existence d’une insuffisance ovarienne précoce, mais il est accentué lorsque le diagnostic d’endométriose est posé à un âge plus jeune [33]. Par ailleurs, les traitements fréquemment associés à la prise en charge de la maladie – notamment l’hystérectomie12, l’annexectomie13 ou l’induction d’une ménopause artificielle précoce — constituent souvent des facteurs de risque cardiovasculaire supplémentaires.
Le cancer du sein
Le cancer du sein est le cancer le plus fréquent chez la femme, pour lequel la survie à dix ans dépasse désormais 80 %. Cette amélioration du pronostic pose toutefois la question des effets secondaires à long terme des traitements, notamment d’un point de vue cardiovasculaire.
Plusieurs études ont rapporté une élévation de l’incidence de la maladie coronarienne chez les femmes ayant eu un cancer du sein [35]. Un lien particulier a été mis en évidence entre un âge jeune lors du diagnostic et un risque accru d’infarctus du myocarde ultérieur [36].
Une cohorte de population générale a également montré une augmentation du risque de cardiopathie ischémique dans l’année suivant le diagnostic de cancer du sein, suggérant le rôle potentiel d’un stress émotionnel intense en période post-diagnostique [37]. D’autres travaux ont renforcé cette hypothèse en identifiant, chez des femmes ayant déjà présenté un infarctus, une sensibilité accrue à l’ischémie myocardique induite par le stress, possiblement liée à une dysfonction microcirculatoire plus marquée chez les femmes [38].
Par ailleurs, certains traitements adjuvants du cancer du sein sont eux-mêmes associés à un surrisque cardiovasculaire. L’utilisation d’inhibiteurs de l’aromatase14 est corrélée à une augmentation du risque de cardiopathie ischémique, contrairement à l’usage du tamoxifène15 [37]. Les anthracyclines16 et le trastuzumab17 sont également impliqués, avec des effets délétères précoces ou retardés, parfois survenant cinq ans ou plus après le traitement, principalement via des risques de dysfonction systolique du ventricule gauche [39].
La radiothérapie mammaire adjuvante est couramment utilisée après une chirurgie conservatrice ou en présence d’atteinte ganglionnaire. Dans certains cas, notamment lors d’une irradiation de la chaîne mammaire interne, une irradiation cardiaque concomitante peut survenir, notamment en cas de cancer du sein gauche. La cardiotoxicité associée à la radiothérapie serait liée à un stress oxydatif chronique induit par l’irradiation des tissus cardiaques [40]. Une large étude cas-témoin menée au Danemark et en Suède sur plus de 2 000 femmes a mis en évidence une augmentation linéaire du risque de cardiopathie ischémique en fonction de la dose reçue, avec une élévation du risque débutant quelques années après le traitement et persistant pendant plus de vingt ans [41]. Cependant, des travaux plus récents n’ont pas confirmé cette association. Plusieurs études suggèrent l’absence d’augmentation du risque cardiovasculaire, probablement en lien avec une amélioration des techniques de radiothérapie [37]. Il semble que l’on observe actuellement les conséquences post-radiques chez des patientes irradiées il y a 20 à 30 ans, qui ont été exposées à des doses beaucoup plus élevées au niveau cardiaque.
Si le risque absolu reste faible, il est néanmoins aggravé en présence de facteurs de risque cardiovasculaires associés [40].
Différentes stratégies sont actuellement utilisées pour réduire l’exposition cardiaque, telles que le positionnement en décubitus18 latéral, l’inspiration forcée ou le fractionnement des doses. Par ailleurs, des approches pharmacologiques sont actuellement évaluées, incluant l’usage d’antioxydants, de statines, ou encore de candésartan19 en monothérapie, qui pourraient conférer une cardioprotection dans ce contexte [40].
Ainsi, le risque de cardiopathie ischémique chez la femme peut être influencé par des particularités gynécologiques, résumées dans la Figure 2.
 |
Figure 2 Impact des particularités gynécologiques sur le risque de cardiopathie ischémique. IDM : infarctus du myocarde ; COP : contraception oestroprogestative ; SOPK : syndrome des ovaires polykystiques. |
Particularités anatomiques et physiopathologiques des artères coronaires chez la femme
Des formes dites « non obstructive » plus fréquentes
Chez les femmes admises pour un NSTEMI, les coronarographies révèlent plus fréquemment l’absence de lésion significative (définie par une sténose supérieure à 50 %) par rapport aux hommes ce qui définit une fréquence accrue d’infarctus du myocarde à « coronaires saines » [2]. Pourtant, les données issues d’études anatomopathologiques et d’imagerie intracoronaire ont montré que les femmes présentent une charge athéromateuse comparable à celle des hommes, avec une quantité similaire de plaques et de calcifications [23]. Ces plaques s’accompagnent cependant plus fréquemment d’un remodelage vasculaire excentrique ou dit « positif », permettant de maintenir une lumière artérielle relativement préservée.
Taille et morphologie des artères coronaires
Les femmes présentent des artères coronaires de plus petit diamètre que les hommes, y compris après ajustement en fonction de la surface corporelle [23, 42, 43]. Cette différence est particulièrement marquée au niveau des segments proximaux, et le diamètre des artères coronaires féminines est estimé à environ 90 % de celui des hommes. Bien qu’on ne retrouve pas d’association entre le sexe féminin et la tortuosité des artères coronaires dans la littérature (la méthodologie de ces études étant souvent peu robuste et peu de travaux ayant été publiés sur ce sujet), on note dans la pratique des tortuosités plus marquées chez les femmes, rendant parfois les procédures d’angioplastie plus complexes.
Mécanisme thrombotique : une physiopathologie distincte
En cas d’infarctus, l’évènement déclencheur du thrombus semble différer entre les sexes. Alors que les hommes présentent plus fréquemment une rupture de plaque, chez les femmes, la formation du thrombus est deux fois plus souvent liée à une érosion de plaque (rupture superficielle de la plaque fibreuse sans libération du cœur lipidique) [23].
Sur le plan histologique, une plaque érodée se compose souvent d’une chape épaisse avec peu de lipides ainsi qu’une altération de la matrice sous-endothéliale, riche en protéoglycanes, hyaluronane et cellules musculaires lisses. L’érosion de plaque entraîne rarement une thrombose extensive et une occlusion complète de l’artère. Au contraire, une plaque rompue présente, le plus souvent, une chape fibreuse fine avec un cœur riche en lipides. Plusieurs mécanismes semblent impliqués dans l’érosion, notamment des modifications de la matrice extracellulaire ainsi qu’une dysfonction endothéliale [44].
L’hypothèse d’une dysfonction endothéliale
L’un des mécanismes sous-jacents évoqués pour expliquer la fréquence accrue des syndromes ischémiques sans sténose significative chez la femme est une dysfonction endothéliale. Cette dernière correspond à une incapacité de l’endothélium vasculaire à produire de manière adéquate de l’oxyde nitrique, essentiel à la vasodilatation et à l’adaptation au stress myocardique. Ce dysfonctionnement pourrait rendre les femmes plus vulnérables à l’ischémie myocardique, même en l’absence de sténose significative détectable en angiographie.
La dissection coronaire spontanée : une cause spécifique d’infarctus chez la femme jeune
La dissection coronaire spontanée constitue une cause particulière de syndrome coronarien aigu, touchant préférentiellement les femmes jeunes, souvent sans facteurs de risque cardiovasculaires traditionnels. Elle est retrouvée dans 25 à 35 % des infarctus du myocarde chez les femmes de moins de 50 ans [45].
Quatre types angiographiques ont été décrits [45] :
Type I : visualisation d’un flap intimal20 avec une double lumière, pathognomonique21 lorsqu’elle est présente.
Type II : réduction diffuse du calibre artériel, le plus fréquent. Le sous-type IIa est limité par des segments de calibre normal en amont et en aval, tandis que le IIb s’étend jusqu’à l’extrémité distale du vaisseau.
Type III : sténose focale ou tubulaire de moins de 20 mm, pouvant mimer une sténose athéromateuse.
Type IV : occlusion complète de la lumière artérielle par le faux chenal.
Plusieurs critères orientent vers le diagnostic de dissection coronaire spontanée [13] : (1) l’absence d’athérome sur les autres artères coronaires, (2) la présence d’un flap radiotransparent délimitant deux lumières (Figure 1), (3) une stagnation du produit de contraste dans la lumière artérielle, (4) des limites nettes de la zone anormale, souvent au niveau d’une branche collatérale, (5) une réduction longue du calibre artériel, régulière ou en aspect de sténoses multiples, mimant une silhouette de « phasme » ou de « radis ».
Dans les formes douteuses, l’imagerie endocoronaire (notamment par tomographie par cohérence optique) [46] (→) permet de confirmer le diagnostic sans majorer le risque de complication, si elle est réalisée avec précaution.
(→) Voir m/s n° 10, 2006, page 859
Prise en charge et pronostic de l’infarctus du myocarde chez les femmes
L’infarctus du myocarde chez les femmes présente des spécificités thérapeutiques notables, résumées dans le Tableau II.
Particularités liées au sexe dans la prise en charge de l’infarctus du myocarde.
Prise en charge initiale et pronostic
Plusieurs études françaises ont mis en évidence un délai plus long entre l’apparition des symptômes et la première consultation médicale chez les femmes par rapport aux hommes. Ce « délai patient » est en moyenne prolongé d’une vingtaine de minutes, probablement à cause d’une moindre tendance à solliciter rapidement les services d’urgence. En revanche, une fois le diagnostic d’infarctus établi, le délai de prise en charge par reperfusion (par exemple par angioplastie en cas de STEMI) ne montre pas de différence notable entre les sexes (Tableau II) [4].
La mortalité hospitalière est plus élevée chez les femmes que chez les hommes, particulièrement en cas de STEMI. En France, elle est environ deux fois plus importante dans cette situation [6]. Toutefois, plusieurs travaux indiquent que cette différence s’atténue après la prise en compte de facteurs tels que l’âge plus avancé et la fréquence accrue du diabète chez les patientes [10].
Il apparaît ainsi que la mortalité précoce est plus élevée chez les femmes, ce qui s’explique par une présentation clinique initiale plus sévère, observée chez des patientes généralement plus âgées et présentant davantage de comorbidités ; toutefois, le sexe ne constitue pas en lui-même un facteur prédictif indépendant de mortalité accrue.
Stratégies thérapeutiques : médicaments, angioplastie, chirurgie
Les médicaments
Malgré des recommandations thérapeutiques communes à l’ensemble des patients, des différences dans l’utilisation des médicaments ont été observées chez les femmes présentant un infarctus du myocarde.
En phase préhospitalière, elles reçoivent moins souvent certains traitements antiplaquettaires que les hommes, alors que l’usage de la fibrinolyse ne varie pas selon le sexe [2, 4].
En ce qui concerne le traitement post-NSTEMI, les femmes se voient moins souvent prescrire des inhibiteurs de P2Y12 (le récepteur de l’ADP sur les plaquettes), une classe d’antiagrégants plaquettaires, en particulier lorsqu’elles ne bénéficient pas d’une angioplastie [47]. Ceci pourrait s’expliquer par des contre-indications plus fréquentes chez les femmes, notamment liées au poids.
Enfin, plusieurs études nord-américaines montrent que ces écarts sont encore plus marqués chez les femmes jeunes, qui reçoivent moins souvent des traitements de prévention secondaire tels que les hypolipémiants22, les antiagrégants et les bêtabloquants [8].
L’angioplastie
La revascularisation myocardique est un élément clé de la prise en charge de l’infarctus du myocarde. Les données actuelles indiquent qu’elle est aussi bénéfique chez les femmes que chez les hommes, en particulier dans les formes à haut risque [48]. Toutefois, certains travaux ont suggéré un bénéfice moindre chez les femmes atteintes de NSTEMI, avec une augmentation de la mortalité précoce observée dans cette population [47].
Les données issues des registres récents révèlent un recours similaire à la coronarographie entre les sexes [2]. Cependant, les femmes bénéficient moins fréquemment d’une angioplastie primaire, et lorsqu’elle est réalisée, on observe un moindre usage des stents actifs au profit d’une angioplastie au ballon seul [47]. Ces éléments pourraient être expliqués par la présence d’un réseau coronaire plus tortueux qui engendre des procédures plus difficiles notamment pour acheminer le matériel nécessaire à l’angioplastie (Figure 3A). De plus, la voie radiale, aujourd’hui privilégiée pour ses bénéfices en termes de sécurité et de confort, est moins souvent utilisée chez les femmes, ce qui s’explique par un diamètre de l’artère radial réduit (Figure 3B) [10, 49]. Les femmes présentent également plus fréquemment des boucles radiales (Figure 3C), qui peuvent être une source d’échec de la voie d’abord23 [50]. Ceci les expose aux complications associées à l’abord fémoral, avec notamment un risque d’hématome au point de ponction multiplié par dix [51].
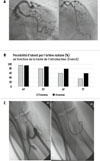 |
Figure 3 Difficultés procédurales en lien avec l’anatomie vasculaire chez les femmes. A. Coronarographie mettant en évidence un réseau coronaire gauche très tortueux. B. Possibilité de pratiquer la procédure par l’artère radiale (%) en fonction de la taille de l’introducteur dans l’artère radiale (désilet) qui permet de faire progresser le matériel dans l’artère radiale jusqu’aux artères coronaires (F : French, 1 French équivaut à 0,33 mm de diamètre). Pour une taille de désilet de 6 French, quasiment une femme sur deux ne pourra pas bénéficier d’un abord radial. C. Angiographie d’une boucle radiale, rendant la montée des sondes plus délicate. |
Parmi les patients hospitalisés pour STEMI en 2022, les femmes non revascularisées au cours de l’hospitalisation étaient significativement plus nombreuses que les hommes [4, 6, 51, 52].
Un cas particulier mérite une attention spécifique : celui de la dissection coronarienne spontanée. Dans ce contexte, il est recommandé d’éviter une revascularisation invasive, en raison du risque d’extension de la dissection. Une prise en charge conservatrice est privilégiée, sans recours systématique à l’angioplastie ni aux traitements antithrombotiques agressifs [13].
La chirurgie
Le pontage aorto-coronarien constitue une option thérapeutique majeure dans le traitement des maladies coronariennes étendues ou complexes. Toutefois, plusieurs travaux suggèrent une mortalité postopératoire plus élevée chez les femmes que chez les hommes. Une méta-analyse de grande ampleur a, par exemple, montré un excès de décès précoces chez les patientes, tendance confirmée dans de larges cohortes, même après la prise en compte de l’âge [53, 54].
Plusieurs hypothèses physiopathologiques ont été avancées pour expliquer cette différence, au premier rang desquelles figurent la plus petite taille des artères coronaires chez les femmes. En outre, les femmes accédant à la chirurgie sont, statistiquement, plus âgées, et présentent davantage de comorbidités que leurs homologues masculins [55]. Il convient de souligner que la plupart des données disponibles proviennent d’études anciennes, qui doivent être réévaluées de façon prospective.
Conclusion
L’infarctus du myocarde chez la femme présente un certain nombre de spécificités physiopathologiques, cliniques, anatomiques et thérapeutiques. Si les données restent parfois discordantes quant à la prise en charge, il est établi que les femmes présentent, en moyenne, une survenue de l’événement coronarien plus tardive, souvent dans un contexte clinique plus sévère, avec un profil de comorbidités plus important.
On observe par ailleurs une augmentation préoccupante de l’incidence de l’infarctus du myocarde chez les femmes jeunes, probablement liée avec la progression des facteurs de risque cardiovasculaire dans cette population. En France, la prise en charge médicamenteuse initiale et la prévention secondaire semble globalement comparable entre les sexes. Toutefois, une tendance à un moindre recours aux stratégies invasives chez les femmes persiste.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Bensouda C, Otel I, Danchin N. Aspects cliniques des syndromes coronariens aigus. Med Sci (Paris) 2004 ; 20 : 402–7. [Google Scholar]
- Simon T, Puymirat E, Lucke V, et al. Acute myocardial infarction in women. Initial characteristics, management and early outcome. The FAST-MI registry. Ann Cardiol Angeiol (Paris) 2013 ; 62 : 221–6. [Google Scholar]
- Gabet A. Infarctus du myocarde chez la femme : évolutions des taux d’hospitalisation et de mortalité, France, 2002-2013. BEH 2016 ; 7 : 100–8 [Google Scholar]
- Manzo-Silberman S, Couturaud F, Charpentier S, et al. Influence of gender on delays and early mortality in ST-segment elevation myocardial infarction: Insight from the first French Metaregistry, 2005-2012 patient-level pooled analysis. Int J Cardiol 2018 ; 262 : 1–8. [Google Scholar]
- Grave C, Gabet A, Cinaud A, et al. Nationwide time trends in patients hospitalized for acute coronary syndrome: a worrying generational and social effect among women. Eur J Prev Cardiol 2024 ; 31 : 116–27. [Google Scholar]
- Grave C, Gabet A, Danchin N, et al. Epidemiology of ischaemic heart disease in France. Arch Cardiovasc Dis 2024 ; 117 : 725–37. [Google Scholar]
- Anand SS, Islam S, Rosengren A, et al. Risk factors for myocardial infarction in women and men: insights from the INTERHEART study. Eur Heart J 2008 ; 29 : 932–40. [Google Scholar]
- Arora S, Stouffer GA, Kucharska-Newton AM, et al. Twenty year trends and sex differences in young adults hospitalized with acute myocardial infarction. Circulation 2019 ; 139 : 1047–56. [Google Scholar]
- Thuresson M, Jarlöv MB, Lindahl B, et al. Symptoms and type of symptom onset in acute coronary syndrome in relation to ST elevation, sex, age, and a history of diabetes. Am Heart J 2005 ; 150 : 234–42. [Google Scholar]
- Barthélémy O, Degrell P, Berman E, et al. Sex-related differences after contemporary primary percutaneous coronary intervention for ST-segment elevation myocardial infarction. Arch Cardiovasc Dis 2015 ; 108 : 428–36. [Google Scholar]
- Safdar B, Spatz ES, Dreyer RP, et al. Presentation, clinical profile, and prognosis of young patients with myocardial infarction with nonobstructive coronary arteries (minoca): results from the VIRGO study. J Am Heart Assoc 2018 ; 7 : e009174. [Google Scholar]
- Pasupathy S, Air T, Dreyer RP, et al. Systematic review of patients presenting with suspected myocardial infarction and nonobstructive coronary arteries. Circulation 2015 ; 131 : 861–70. [Google Scholar]
- Motreff P, Malcles G, Combaret N, et al. How and when to suspect spontaneous coronary artery dissection: novel insights from a single-centre series on prevalence and angiographic appearance. EuroIntervention J Eur Collab Work Group Interv Cardiol Eur Soc Cardiol 2017 ; 12 : e2236–43. [Google Scholar]
- Saw J, Aymong E, Mancini GBJ, et al. Nonatherosclerotic coronary artery disease in young women. Can J Cardiol 2014 ; 30 : 814–19. [Google Scholar]
- Georges A, Bouatia-Naji N. La génétique établit le lien entre plusieurs maladies cardiovasculaires affectant préférentiellement les femmes. Med Sci (Paris) 2019 ; 35 : 605–7. [Google Scholar]
- Yoganathan T, Tavitian B. Syndrome de takotsubo - Le métabolisme cardiaque au cœur du problème ? Med Sci (Paris) 2024 ; 40 : 130–2. [Google Scholar]
- Ghadri J-R, Wittstein IS, Prasad A, et al. International expert consensus document on Takotsubo syndrome (part ii): diagnostic workup, outcome, and management. Eur Heart J 2018 ; 39 : 2047–62. [Google Scholar]
- Roach REJ, Helmerhorst FM, Lijfering WM, et al. Combined oral contraceptives: the risk of myocardial infarction and ischemic stroke. Cochrane Database Syst Rev 2015 ; 2015 : CD011054. [Google Scholar]
- Lidegaard Ø, Løkkegaard E, Jensen A, et al. Thrombotic stroke and myocardial infarction with hormonal contraception. N Engl J Med 2012 ; 366 : 2257–66. [CrossRef] [PubMed] [Google Scholar]
- Elkayam U, Jalnapurkar S, Barakkat MN, et al. Pregnancy-associated acute myocardial infarction: a review of contemporary experience in 150 cases between 2006 and 2011. Circulation 2014 ; 129 : 1695–702. [Google Scholar]
- Oliver-Williams CT, Heydon EE, Smith GCS, et al. Miscarriage and future maternal cardiovascular disease: a systematic review and meta-analysis. Heart Br Card Soc 2013 ; 99 : 1636–44. [Google Scholar]
- Pechère-Bertschi A, Burnier M. Female sex hormones, salt, and blood pressure regulation. Am J Hypertens 2004 ; 17 : 994–1001. [Google Scholar]
- Bellasi A, Raggi P, Merz CNB, et al. New insights into ischemic heart disease in women. Cleve Clin J Med 2007 ; 74 : 585–94. [Google Scholar]
- Colditz GA, Willett WC, Stampfer MJ, et al. Menopause and the risk of coronary heart disease in women. N Engl J Med 1987 ; 316 : 1105–10. [Google Scholar]
- Wild RA, Carmina E, Diamanti-Kandarakis E, et al. Assessment of cardiovascular risk and prevention of cardiovascular disease in women with the polycystic ovary syndrome: a consensus statement by the androgen excess and polycystic ovary syndrome (AE-PCOS) Society. J Clin Endocrinol Metab 2010 ; 95 : 2038–49. [Google Scholar]
- Honigberg MC, Zekavat SM, Aragam K, et al. Association of premature natural and surgical menopause with incident cardiovascular disease. JAMA 2019 ; 322 : 2411–21. [Google Scholar]
- Chakrabarti S, Morton JS, Davidge ST. Mechanisms of estrogen effects on the endothelium: an overview. Can J Cardiol 2014 ; 30 : 705–12. [Google Scholar]
- Moreau KL, Hildreth KL, Meditz AL, et al. Endothelial function is impaired across the stages of the menopause transition in healthy women. J Clin Endocrinol Metab 2012 ; 97 : 4692–700. [Google Scholar]
- Boardman HMP, Hartley L, Eisinga A, et al. Hormone therapy for preventing cardiovascular disease in post-menopausal women. Cochrane Database Syst. Rev 2015 ; 2015 : CD002229. [Google Scholar]
- Schierbeck LL, Rejnmark L, Tofteng CL, et al. Effect of hormone replacement therapy on cardiovascular events in recently postmenopausal women: randomised trial. BMJ 2012 ; 345 : e6409. [Google Scholar]
- Gao L, Zhao Y, Wu H, et al. Polycystic ovary syndrome fuels cardiovascular inflammation and aggravates ischemic cardiac injury. Circulation 2023 ; 148 : 1958–73. [Google Scholar]
- Wekker V, Dammen L van, Koning A, et al. Long-term cardiometabolic disease risk in women with PCOS: a systematic review and meta-analysis. Hum Reprod Update 2020 ; 26 : 942–60. [CrossRef] [PubMed] [Google Scholar]
- Blom JN, Velez MP, McClintock C, et al. Endometriosis and cardiovascular disease: a population-based cohort study. CMAJ Open 2023 ; 11 : E227–36. [Google Scholar]
- Poeta do Couto C, Policiano C, Pinto FJ, et al. Endometriosis and cardiovascular disease: A systematic review and meta-analysis. Maturitas 2023 ; 171 : 45–52. [Google Scholar]
- Khan NF, Mant D, Carpenter L, et al. Long-term health outcomes in a British cohort of breast, colorectal and prostate cancer survivors: a database study. Br J Cancer 2011 ; 105 Suppl 1 : S29–37. [Google Scholar]
- Liang J, Pan Y, Zhang W, et al. Associations of age at diagnosis of breast cancer with incident myocardial infarction and heart failure: A prospective cohort study. eLife 2024 ; 13 : RP95901. [Google Scholar]
- Yang H, Bhoo-Pathy N, Brand JS, et al. Risk of heart disease following treatment for breast cancer - results from a population-based cohort study. eLife 2022 ; 11 : e71562. [Google Scholar]
- Vaccarino V, Sullivan S, Hammadah M, et al. Mental stress-induced-myocardial ischemia in young patients with recent myocardial infarction: sex differences and mechanisms. Circulation 2018 ; 137 : 794–805. [Google Scholar]
- Vo JB, Ramin C, Veiga LHS, et al. Long-term cardiovascular disease risk after anthracycline and trastuzumab treatments in US breast cancer survivors. J Natl Cancer Inst 2024 ; 116 : 1384–94. [Google Scholar]
- Kammerer E, Le Guévelou J, Jacob S, et al. Cardiac complications of breast radiation therapy. Bull. Cancer (Paris) 2019 ; 106 : 379–88. [Google Scholar]
- Darby SC, Ewertz M, McGale P, et al. Risk of ischemic heart disease in women after radiotherapy for breast cancer. N Engl J Med 2013 ; 368 : 987–98. [CrossRef] [PubMed] [Google Scholar]
- Sheifer SE, Canos MR, Weinfurt KP, et al. Sex differences in coronary artery size assessed by intravascular ultrasound. Am Heart J 2000 ; 139 : 649–53. [Google Scholar]
- Dodge JT, Brown BG, Bolson EL, et al. Lumen diameter of normal human coronary arteries. Influence of age, sex, anatomic variation, and left ventricular hypertrophy or dilation. Circulation 1992 ; 86 : 232–46. [Google Scholar]
- Jager SCA de, Meeuwsen JAL, Pijpen FM van, et al. Preeclampsia and coronary plaque erosion: Manifestations of endothelial dysfunction resulting in cardiovascular events in women. Eur J Pharmacol 2017 ; 816 : 129–37. [Google Scholar]
- Adlam D, Alfonso F, Maas A, et al. European society of cardiology, acute cardiovascular care association, SCAD study group: a position paper on spontaneous coronary artery dissection. Eur Heart J 2018 ; 39 : 3353–68. [Google Scholar]
- Dubois A, Boccara C. L’OCT plein champ. Med Sci (Paris) 2006 ; 22 : 859–64. [Google Scholar]
- Cenko E, Ricci B, Kedev S, et al. Invasive versus conservative strategy in acute coronary syndromes: The paradox in women’s outcomes. Int J Cardiol 2016 ; 222 : 1110–5. [Google Scholar]
- O’Donoghue M, Boden WE, Braunwald E, et al. Early invasive vs conservative treatment strategies in women and men with unstable angina and non-st-segment elevation myocardial infarction: a meta-analysis. JAMA 2008 ; 300 : 71–80. [Google Scholar]
- Haq MA ul, Tsay IM, Dinh DT, et al. Prevalence and outcomes of trans-radial access for percutaneous coronary intervention in contemporary practise. Int. J. Cardiol. 2016 ; 221 : 264–268. [Google Scholar]
- Lo TS, Nolan J, Fountzopoulos E, et al. Radial artery anomaly and its influence on transradial coronary procedural outcome. Heart Br Card Soc 2009 ; 95 : 410–5. [Google Scholar]
- Agostoni P, Biondi-Zoccai GGL, Benedictis ML de, et al. Radial versus femoral approach for percutaneous coronary diagnostic and interventional procedures; Systematic overview and meta-analysis of randomized trials. J Am Coll Cardiol 2004 ; 44 : 349–56. [Google Scholar]
- Gail D’Onofrio, Basmah Safdar, Judith H Lichtman, Kelly M Strait et al. Sex differences in reperfusion in young patients with ST-segment-elevation myocardial infarction: results from the VIRGO study. Circulation 2015 ; 131 : 1324–32. [Google Scholar]
- Shi D, Zhang B, Motamed M, et al. Higher mortality in women after coronary artery bypass: meta-analysis and bias analysis of confounding. Ann Thorac Sur. 2022 ; 113 : 674–80. [Google Scholar]
- Johnston A, Mesana TG, Lee DS, et al. Sex differences in long-term survival after major cardiac surgery: a population-based cohort study. J Am Heart Assoc 2019 ; 8 : e013260. [Google Scholar]
- Esmaeilzadeh S, Vinzant N, Ramakrishna H. Outcomes in women undergoing coronary artery bypass grafting: analysis of new data and operative trends. J Cardiothorac Vasc Anesth 2025 ; 39 : 532–7. [Google Scholar]
Le syndrome coronarien aigu (SCA) désigne un ensemble de conditions résultant d’une diminution brutale du flux sanguin vers le cœur, causée par une obstruction partielle ou totale d’une artère coronaire. Il regroupe trois entités cliniques : l’angor instable (SCA ST-troponine -), le NSTEMI (SCA ST-troponine +) et le STEMI (SCA ST+).
Le segment ST est une partie de l’ECG qui représente le début de la repolarisation ventriculaire et correspond à la phase de repolarisation lente en « plateau » des myocytes ventriculaires (ndlr).
L’ischémie est l’interruption à la fois de l’apport d’oxygène et de nutriment, mais cela interrompt également l’élimination des molécules toxiques résultant du métabolisme cellulaire (ndlr).
Une sténose est une modification anatomique qui se traduit par un rétrécissement d’une structure (canal, vaisseau) (ndlr).
Un embole est un élément qui flotte dans un vaisseau et qui se bloque, pouvant être un caillot de sang, une bulle de gaz, une boule de graisse ou un bout de calcaire (ndlr).
L’angiotensinogène (également connu sous le nom d’hypertensinogène) est une glycoprotéine précurseur de l’angiotensine I, un peptide biologiquement actif qui régule la pression artérielle et est impliqué dans un certain nombre d’autres processus dans le corps (ndlr).
La cardiopathie ischémique est une maladie du cœur due au manque d’oxygène dans les artères coronaires (ndlr).
La thrombophilie correspond à une prédisposition pathologique à la formation de caillots sanguins (thrombus). Cette maladie résulte d’un déséquilibre du système de coagulation, favorisant la thrombose (ndlr).
La prééclampsie est une maladie de la grossesse qui associe une hypertension artérielle et une protéinurie (ndlr).
Le HDL-cholestérol (ou « bon cholestérol ») est une forme de cholestérol transportée dans le sang par des lipoprotéines appelées HDL (high density lipoproteins, ou lipoprotéines de haute densité) (ndlr).
Le taux de LDL-cholestérol (souvent appelé « mauvais cholestérol ») mesure la quantité de cholestérol transportée dans le sang par les lipoprotéines de basse densité (low density lipoproteins) (ndlr).
L’hystérectomie consiste en l’ablation chirurgicale de l’utérus (ndlr).
L’annexectomie est une intervention chirurgicale qui consiste à retirer les ovaires et les trompes de Fallope (ndlr).
L’aromatase est une enzyme impliquée dans la production d’œstrogènes, et qui agit en catalysant la conversion de la testostérone (un androgène) en estradiol (un œstrogène). On utilise les inhibiteurs de l’aromatase car ils privent la tumeur des œstrogènes dont elle dépend pour se développer (ndlr).
Le tamoxifène est une molécule qui se fixe sur les récepteurs aux œstrogènes (ER) dans les cellules tumorales et empêche les œstrogènes de stimuler leur croissance. Le choix entre tamoxifène et inhibiteurs de l’aromatase dépend surtout du statut ménopausique et du profil de risque de la patiente (ndlr).
Les anthracyclines sont des chimiothérapies qui détruisent les cellules cancéreuses. Le trastuzumab est un anticorps monoclonal humanisé dirigé contre le récepteur HER2 exprimé par environ 15-20 % des cancers du sein (ndlr).
Le trastuzumab est un anticorps monoclonal recombinant qui bloque le récepteur HER2 (human epidermal growth factor receptor 2) impliqué notamment dans certains cancers du sein (ndlr).
Décubitus désigne un corps allongé à l’horizontale, avec différentes positions possibles selon l’orientation et l’inclinaison (ndlr).
Le candésartan est un médicament de la classe des antagonistes des récepteurs de l’angiotensine II (ndlr).
Un flap intimal est une séparation de l’intima, la couche la plus interne d’une artère, de la média, la couche intermédiaire. Ce détachement crée un nouveau canal, appelé fausse lumière, par lequel le sang s’écoule à côté de la vraie lumière d’origine (ndlr).
Pathognomonique est un adjectif qualifiant les signes caractéristiques, spécifiques d’une maladie et qui permettent de poser un diagnostic sans hésitation, sans ambiguïté (ndlr).
Les hypolipémiants sont des médicaments qui font diminuer le taux de graisses dans le sang (ndlr).
Voie utilisée par le chirurgien pour accéder à un organe ou à une région anatomique donnée (ndlr).
Liste des tableaux
Type d’infarctus en fonction du sexe. On constate une prévalence plus importante des infarctus à « coronaires saines » chez les femmes, qui représentent jusqu’à 15 % des infarctus selon les séries, soit 5 fois plus que les hommes. IDM : Infarctus du myocarde ; STEMI : syndrome coronarien aigu avec sus-décalage du segment ST ; NSTEMI : syndrome coronarien aigu sans sus-décalage du segment ST ; MINOCA : myocardial infarction with non obstructive coronary arteries.
Particularités liées au sexe dans la prise en charge de l’infarctus du myocarde.
Liste des figures
 |
Figure 1 Images de dissection coronaire en coronarographie. À gauche : dissection coronaire sur l’artère interventriculaire antérieure avec flap intimal (flèche). À droite : dissection coronaire étendue sur l’artère interventriculaire antérieure proximale avec extension sur la première diagonale. IVA : interventriculaire antérieure ; Dg : diagonale. |
| Dans le texte | |
 |
Figure 2 Impact des particularités gynécologiques sur le risque de cardiopathie ischémique. IDM : infarctus du myocarde ; COP : contraception oestroprogestative ; SOPK : syndrome des ovaires polykystiques. |
| Dans le texte | |
 |
Figure 3 Difficultés procédurales en lien avec l’anatomie vasculaire chez les femmes. A. Coronarographie mettant en évidence un réseau coronaire gauche très tortueux. B. Possibilité de pratiquer la procédure par l’artère radiale (%) en fonction de la taille de l’introducteur dans l’artère radiale (désilet) qui permet de faire progresser le matériel dans l’artère radiale jusqu’aux artères coronaires (F : French, 1 French équivaut à 0,33 mm de diamètre). Pour une taille de désilet de 6 French, quasiment une femme sur deux ne pourra pas bénéficier d’un abord radial. C. Angiographie d’une boucle radiale, rendant la montée des sondes plus délicate. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




