| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
|
|
|---|---|---|
| Page(s) | 848 - 850 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2025214 | |
| Published online | 12 décembre 2025 | |
Localisation axonale des ARN messagers et formation des mémoires à long terme
Axonal mRNA localization and long-term memory formation
Université Côte d’Azur, CNRS UMR7277, Inserm U1091, Institut de Biologie Valrose, Nice, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Le cerveau est un organe capable de s’adapter aux expériences et de stocker des informations pour les retrouver ultérieurement, sous forme de souvenirs. Le modèle actuel en neurosciences est que les souvenirs sont encodés par le renforcement des connexions synaptiques. Avec une estimation de 86 milliards de neurones interconnectés par environ 100 trillions de synapses, le cerveau humain représente un réservoir presque infini pour le stockage d’informations sous forme de souvenirs. À ce jour, les mécanismes moléculaires qui sous-tendent le renforcement synaptique - en d’autres termes, ce qu’est physiquement un souvenir dans le cerveau - restent en grande partie à élucider. Ce processus doit être suffisamment spécifique pour que les molécules nécessaires à la mémorisation soient produites au bon endroit, au bon moment, et en réponse au signal neuronal approprié.
Les protéines, qui sont les molécules essentielles à la réalisation des processus intracellulaires, sont synthétisées à partir d’ARN messagers (ARNm), qui transmettent les instructions de l’ADN. Il est établi que les mémoires à court terme, d’une durée de quelques minutes à quelques heures, reposent sur la modification de protéines déjà présentes, tandis que la formation des mémoires à long terme, qui peuvent persister des jours, des mois, voire toute une vie, requiert la synthèse de nouvelles protéines [1]. Dans les neurones qui possèdent des prolongements cellulaires (axones ou dendrites) longs, cela représente un véritable défi logistique. Certaines synapses sont situées à des centaines de micromètres du corps cellulaire, rendant l’acheminement de protéines, à partir du corps cellulaire, lent et difficile à cibler. Pour s’affranchir de cette contrainte, les neurones acheminent, le long de leurs axones ou de leurs dendrites, des ARNm, qui sont ensuite traduits localement, « à la demande », en protéines [2]. Ce mécanisme permet des réponses rapides et spatialement précises aux signaux externes, une condition essentielle au renforcement synaptique.
Des mécanismes du transport neuronal de l’ARNm dans des tranches de cerveau ou des cultures cellulaires ont été décrits, mais il restait à montrer qu’ils contribuent effectivement à la formation de mémoires pérennes in vivo. Notre étude a établi le lien entre le transport sélectif des ARNm dans les axones et des comportements associés à la formation de mémoires à long terme dans un organisme vivant [3]. Cette découverte ouvre de nouvelles perspectives sur le fonctionnement et l’organisation moléculaire des circuits neuronaux impliqués dans la mémoire, ainsi que pour la compréhension des troubles mnésiques dans les maladies neurodégénératives.
Localisation sélective d’ARN messagers dans les terminaisons synaptiques in vivo
Nous avons choisi comme modèle d’étude la mouche drosophile, dont les circuits cérébraux sont entièrement cartographiés [4] et moins complexes que dans l’espèce humaine. La découverte d’un mutant qui altère spécifiquement le transport des ARN [5] nous a offert une opportunité unique : pouvoir perturber la localisation des ARNm dans les axones sans affecter d’autres processus cellulaires.
Nous avons d’abord développé une méthode permettant d’isoler des fractions cellulaires enrichies en terminaisons synaptiques (ou synaptosomes) à partir du cerveau de drosophiles adultes. Le séquençage de leur contenu en ARN a révélé l’existence de centaines d’ARNm différents accumulés dans ces terminaisons synaptiques, et qui permettent de synthétiser localement des protéines aux fonctions variées, telles que des molécules de signalisation, des protéines sécrétées, ou des régulateurs du cytosquelette, potentiellement impliquées dans les changements structurels de longue durée [3].
Par ailleurs, nous sommes parvenus à visualiser des molécules individuelles d’ARNm dans les neurones du corps pédonculé, la structure cérébrale majeure impliquée dans l’apprentissage et la mémoire chez la drosophile, par microscopie confocale de haute résolution (Figure 1A). Alors que certains ARNm sont présents dans les terminaisons axonales de ces neurones, d’autres - même fortement exprimés – restent confinés au corps cellulaire, ce qui indique que le transport des ARNm vers les synapses est un processus actif, sélectif et régulé. Nous avons également constaté l’accumulation régionalisée de certains ARNm dans des compartiments spécifiques le long de l’axone [3] (Figure 1B). Ces données nous renseignent sur la nature des marques moléculaires impliquées dans la modulation locale des synapses et le stockage des souvenirs. De plus, la spécificité de ces patrons de localisation des ARNm nous a incités à approfondir l’étude des mécanismes assurant le transport des ARN vers les axones.
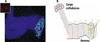 |
Figure 1. Image par microscopie confocale (A) ou modèle schématique (B) du centre de mémorisation du cerveau de la drosophile (corps pédonculé). Les molécules d’ARN (points rouges) se localisent dans les corps cellulaires (encadré) et le long des prolongements axonaux des neurones de la mémoire (bleu) qui forment ensemble le corps pédonculé. Différents sous-compartiments (dont l’un est marqué en vert), caractérisés par leur signature moléculaire et leur connexion avec des neurones et des circuits dédiés, peuvent être définis le long des axones. |
Transport axonal des ARNm et mémoire à long terme
Les ARNm nouvellement synthétisés dans les neurones ne se déplacent pas spontanément vers les synapses. Ils doivent se lier à certaines protéines, et sont alors transportés sous forme de complexes ARN-protéines le long de « pistes » constituées de microtubules [6]. L’une de ces protéines, Imp/ IGF2BP (insulin-like growth factor 2 mRNA-binding protein), impliquée dans le transport des ARN dans différentes espèces, se localise sélectivement dans les axones des neurones des corps pédonculés chez la drosophile [7]. Cette protéine est-elle nécessaire pour l’acheminement des ARNm vers les régions pré-synaptiques de ces neurones, et quelle est l’importance de ce processus pour la mémoire ?
Nous avons montré que chez les mouches possédant une version mutée de la protéine Imp, toujours capable de se lier aux ARNm mais incapable d’être transportée dans les axones, plusieurs ARNm normalement présents dans les axones n’y étaient plus détectés. Empêcher le transport de cette protéine perturbe donc l’acheminement de certains ARNm [3] (Figure 2).
 |
Figure 2. Mécanisme de localisation de l’ARNm impliqué dans la formation de la mémoire à long terme chez la drosophile. A. Dans des conditions physiologiques, les ARNm sont emballés avec des protéines de liaison à l’ARN, telles que Imp, dans des complexes ARNm-protéines. Ces complexes se déplacent le long du cytosquelette, de sorte que les ARNm peuvent parvenir à proximité des synapses et être traduits localement en protéines fonctionnelles. B. Chez le mutant Imp, les complexes ARN-Imp ne sont plus transportés vers les axones, ce qui entrave sélectivement l’acheminement des ARNm vers les régions synaptiques. Ces mouches mutantes perdent également leur capacité à former des souvenirs à long terme, alors que leur mémoire à court terme reste intacte. |
Ce mutant nous a ensuite permis de tester si le transport axonal sélectif des ARNm par une protéine de liaison à l’ARN telle que Imp est nécessaire à la mémoire à long terme. En entraînant les drosophiles à former des mémoires à court terme (une heure d’entraînement) ou à long terme (sept heures d’entraînement), nous avons constaté, chez les mouches mutantes, une déficience spécifique à former une mémoire à long terme, alors que leur mémoire à court terme était intacte. Pour écarter un effet lié à un défaut de développement neuronal, nous avons inactivé Imp uniquement chez les mouches adultes. La persistance du défaut de mémoire à long terme dans ces conditions a confirmé que la localisation axonale de certains ARNm joue un rôle essentiel dans les circuits de mémoire matures [3].
Ces résultats apportent la preuve que le transport sélectif d’ARN vers les axones est nécessaire à la formation de souvenirs durables, et valident l’hypothèse ancienne selon laquelle la traduction locale des ARNm est cruciale pour la consolidation de la mémoire. Ils révèlent également le rôle clé de la localisation axonale des molécules d’ARNm dans l’établissement de compartiments synaptiques distincts au sein des circuits neuronaux impliqués dans la mémorisation.
Perspectives de recherche et implications médicales
Ainsi, il semble que des pools synaptiques d’ARNm soient utilisés pour une synthèse locale de protéines, permettant aux neurones d’ajuster leurs connexions avec une remarquable précision temporelle et spatiale. Ce mécanisme pourrait permettre le « marquage » de certaines synapses spécifiques lors de la formation d’un souvenir.
De nombreuses perspectives de recherche s’ouvrent désormais : visualiser directement la traduction des ARNm localisés aux sites synaptiques des circuits de mémoire, et identifier les signaux déclencheurs de cette synthèse locale de protéines. Notre étude indique d’ores et déjà un rôle important de l’activité neuronale, puisque l’accumulation régionalisée des ARNm dans des compartiments spécifiques le long des axones ne se produit que lorsque les neurones innervant ces compartiments sont actifs [3].
Sur le plan médical, des altérations du métabolisme des ARNm et des protéines de liaison à l’ARN ont été associées à des maladies neurodégénératives telles que la sclérose latérale amyotrophique, la démence fronto-temporale, ou encore la maladie d’Alzheimer. Mieux comprendre comment la localisation des ARNm dans les compartiments neuronaux influence la mémoire ouvre la voie à de nouvelles approches thérapeutiques, incluant l’utilisation de molécules ciblant spécifiquement les populations d’ARNm synaptiques.
Liens d’intérêt
Les auteures déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Kandel ER, Dudai Y, Mayford MR. The molecular and systems biology of memory. Cell 2014 ; 157 : 163–86. [CrossRef] [PubMed] [Google Scholar]
- Bourke AM, Schwarz A, Schuman EM. De-centralizing the Central Dogma: mRNA translation in space and time. Mol Cell 2023 ; 83 : 452–68. [Google Scholar]
- de Queiroz BR, Laghrissi H, Rajeev S, et al. Axonal RNA localization is essential for long-term memory. Nat Commun 2025 ; 16 : 2560. [Google Scholar]
- Dorkenwald S, Matsliah A, Sterling AR, et al. Neuronal wiring diagram of an adult brain. Nature 2024 ; 634 : 124–38. [Google Scholar]
- Vijayakumar J, Perrois C, Heim M, et al. The prion-like domain of Drosophila Imp promotes axonal transport of RNP granules in vivo. Nat Commun 2019 ; 10 : 2593. [Google Scholar]
- Bauer KE, de Queiroz BR, Kiebler MA, Besse F. RNA granules in neuronal plasticity and disease. Trends Neurosci 2023 ; 46 : 525–38. [Google Scholar]
- Medioni C, Ramialison M, Ephrussi A, Besse F. Imp promotes axonal remodeling by regulating profilin mRNA during brain development. Curr Biol 2014 ; 24 : 793–800. [Google Scholar]
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Image par microscopie confocale (A) ou modèle schématique (B) du centre de mémorisation du cerveau de la drosophile (corps pédonculé). Les molécules d’ARN (points rouges) se localisent dans les corps cellulaires (encadré) et le long des prolongements axonaux des neurones de la mémoire (bleu) qui forment ensemble le corps pédonculé. Différents sous-compartiments (dont l’un est marqué en vert), caractérisés par leur signature moléculaire et leur connexion avec des neurones et des circuits dédiés, peuvent être définis le long des axones. |
| Dans le texte | |
 |
Figure 2. Mécanisme de localisation de l’ARNm impliqué dans la formation de la mémoire à long terme chez la drosophile. A. Dans des conditions physiologiques, les ARNm sont emballés avec des protéines de liaison à l’ARN, telles que Imp, dans des complexes ARNm-protéines. Ces complexes se déplacent le long du cytosquelette, de sorte que les ARNm peuvent parvenir à proximité des synapses et être traduits localement en protéines fonctionnelles. B. Chez le mutant Imp, les complexes ARN-Imp ne sont plus transportés vers les axones, ce qui entrave sélectivement l’acheminement des ARNm vers les régions synaptiques. Ces mouches mutantes perdent également leur capacité à former des souvenirs à long terme, alors que leur mémoire à court terme reste intacte. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




