| Numéro |
Med Sci (Paris)
Volume 34, Numéro 10, Octobre 2018
|
|
|---|---|---|
| Page(s) | 799 - 805 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2018205 | |
| Publié en ligne | 19 novembre 2018 | |
La prématurité spontanée et le microbiote maternel
Spontaneous preterm birth and the maternal microbiome
1
Département d’obstétrique-gynécologie et département de microbiologie et infectiologie, université de Sherbrooke, 3001 12 e avenue Nord, Sherbrooke, Québec ( J1H 5H3), Canada
2
Département d’obstétrique-gynécologie, université de Sherbrooke, 3001 12 e avenue Nord, Sherbrooke, Québec ( J1H 5H3), Canada
*
nathalie.cote10@usherbrooke.ca
Des millions d’enfants naissent prématurément chaque année et les cliniciens restent démunis face à la difficulté de maîtriser la physiopathologie associée, ce qui limite les options thérapeutiques. Récemment, il a été suggéré que le microbiote maternel pouvait contribuer au bon déroulement de la grossesse et qu’une dysbiose pourrait entraîner une naissance avant terme. Certaines espèces commensales de Lactobacillus participeraient à une fonction de « filtre vaginal », empêchant une propagation ascendante de pathogènes vers la cavité utérine. Ce compartiment peut par ailleurs être colonisé par des bactéries buccales, suggérant la possibilité de leur dissémination par voie hématogène vers l’utérus.
Abstract
Preterm birth is the leading cause of perinatal mortality and morbidity. Despite the efforts spent over the past 40 years to solve the physiopathological processes involved in the triggering of prematurity, efficient therapeutics are still lacking. Recently, growing body of evidence suggests that the maternal microbiome is a major player for a normal pregnancy and that dysbiosis is associated with preterm birth. The vaginal microbiome and its commensal Lactobacillus species may protect the uterus of ascending dissemination of pathogens. The uterus can also be contaminated with oral bacteria by the blood stream. Thus, the maternal microbiome can play both a protective role or a causal role in the triggering of preterm birth.
© 2018 médecine/sciences – Inserm
Le microbiote et la grossesse
Véritable écosystème composé de milliards de bactéries, virus, levures et mycètes colonisant la bouche, la peau, les voies uro-génitales et l’intestin, le microbiote est maintenant considéré comme un organe. Il est un acteur majeur pour le maintien de notre santé en agissant comme un compétiteur face aux pathogènes et en participant au renouvellement de l’épithélium, au métabolisme et à l’extraction énergétique des nutriments au niveau de l’intestin [1]. Une dysbiose (c’est-à-dire un déséquilibre du microbiote) débutant dès la naissance ou l’enfance est associée à certaines pathologies comme l’obésité, des maladies inflammatoires de l’intestin ou une atopie (voir [2] pour une revue). Cette dysbiose pourrait avoir comme origine une exposition à certains facteurs environnementaux, comme les perturbateurs endocriniens ou les antibiotiques, ou être favorisée par la modalité d’accouchement (césarienne versus accouchement vaginal ou par voies basses) et le mode d’alimentation (allaitement versus lait maternisé).
Au cours de la grossesse, parallèlement aux changements hormonaux, métaboliques et immunitaires, ces écosystèmes se modifient. La flore vaginale devient moins diversifiée et plus stable, avec une augmentation de la proportion de bactéries du genre Lactobacillus [3]. Selon l’abondance des espèces dominantes, 5 types de flores, ou CST (community state type), ont été décrites (Tableau I) [4]. Les changements du microbiote intestinal (MI) apparaissant à la fin de la grossesse pourraient ainsi contribuer à soutenir les besoins énergétiques accrus nécessaires pour assurer le développement fœtal. Cette hypothèse peut être illustrée par des expériences de transplantations de MI qui ont été menées dans un modèle murin, par gavage de préparations fécales provenant de femmes au 1er ou au 3e trimestre de grossesse. Les animaux ont développé des caractéristiques de grossesse spécifiques (augmentation de l’adiposité et de la résistance à l’insuline) s’ils étaient gavés avec des préparations de selles provenant de femmes au 3e trimestre de leur grossesse, mais pas s’ils avaient reçu des préparations prélevées au 1er trimestre [5]. Ces observations suggèrent ainsi un véritable rôle du microbiote dans la physiologie de la grossesse.
Répartition des CST chez les femmes en dehors de la grossesse (d’après [4]).
Des particularités du microbiote ont été révélées pour certaines pathologies obstétricales avec, en cas de diabète gestationnel par exemple, une modification de l’abondance de certains groupes bactériens. Ceci pourrait permettre d’identifier dès le début de la grossesse les femmes à risque et d’adapter leur parcours de soins [6]. D’autres travaux ont montré que la survenue d’une rupture prématurée et préterme des membranes (RPPM) était précédée dans un tiers des cas par un appauvrissement en Lactobacillus, des bacteries protectrices de la flore vaginale [7]. Une dysbiose pourrait donc jouer un rôle de biomarqueur associé à la pathologie, comme c’est le cas pour le diabète gestationnel, mais aussi être directement impliquée dans les processus physiopathologiques.
Ces analyses de communautés microbiennes bénéficient des développements récents dans le domaine de la biologie moléculaire. Les étapes limitantes de mise en culture bactérienne, prérequis à l’identification taxonomique, ont longtemps restreint le nombre d’espèces pouvant être identifiées dans des échantillons de faible biomasse microbienne, comme le placenta ou le liquide amniotique. Les approches combinant amplification par PCR (polymerase chain reaction) et séquençage à haut débit ont permis de montrer que, même en l’absence de toute pathologie, il existe un microbiote placentaire [8, 9, 41] (→) et que certains genres bactériens, comme Streptococcus, Mycoplasma, Ureaplasma et Gardnerella, sont préférentiellement détectés dans des contextes de prématurité, et plus particulièrement lors de chorioamnionite (infection de la cavité utérine). De manière surprenante, ce microbiote placentaire apparaît plus similaire à celui de la cavité buccale de femmes non enceintes qu’à celui du tractus intestinal ou des voies génitales. Ceci évoque donc une dissémination hématogène des microorganismes. Ces observations nécessitent toutefois un regard critique : d’autres études proposent que les bactéries identifiées dans les échantillons de placenta proviendraient plutôt d’une contamination des réactifs de laboratoire… [10]. Nous décrirons ci-dessous comment un microbiote vaginal (MV) équilibré peut contribuer au déroulement d’une grossesse saine et à terme et nous verrons au contraire la façon dont une dysbiose vaginale peut initier une cascade inflammatoire menant à la prématurité (PT), un syndrome encore considéré comme un fléau des temps modernes.
(→) Voir la Synthèse de R. Gschwind et al., m/s n° 4, avril 2018, page 331
La prématurité spontanée, un syndrome complexe
La prématurité (PT) n’est pas une entité unique. Elle regroupe toutes les situations associées à la survenue d’une naissance avant 37 semaines d’aménorrhée. Il convient de distinguer la PT induite à la suite d’une décision médicale, principalement dans des cas de pré-éclampsie ou de retard de croissance intra-utérin, de la PT spontanée (PTs). Les mécanismes initiant la PTs débutent durant une phase subclinique. Ils se compliquent avec des symptômes cliniques repérables tardivement, sous la forme d’un travail prématuré ou d’une RPPM. La prise en charge du travail prématuré consiste en l’administration de tocolytiques1 pour interrompre les contractions. Ce traitement est cependant peu efficace puisqu’il ne prolonge la grossesse que de 48 heures en moyenne [11]. À la suite d’une RPPM, des antibiotiques seront prescrits afin de réduire le risque de survenue d’une chorioamnionite et pour prolonger la période de latence (moment entre la RPPM et l’accouchement) qui, malgré ce traitement, sera en moyenne de 9 jours [12]. Ainsi, en dépit de tous les progrès de la médecine, il existe peu de moyens de prévenir la PT et les cliniciens sont confrontés à un véritable défi pour la prise en charge d’un syndrome complexe et multifactoriel pour lequel les thérapeutiques disponibles aujourd’hui sont limitées et peu efficaces.
Les mécanismes de la prématurité spontanée
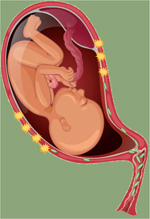
Les mécanismes pouvant conduire à la PTs sont multiples et, outre les voies impliquant le stress maternel et fœtal par la libération de cortisol ou une incompétence mécanique du col utérin, l’inflammation, subclinique dans 50 % des cas, serait un facteur majeur associé à la naissance prématurée. Son rôle est classiquement décrit comme une cascade (Figure 1) [13] qui débute par une modification du microbiote vaginal, avec une diminution des Lactobacillus protecteurs - ce qui permet à des pathogènes comme Gardnerella vaginalis ou Mycoplasma hominis de proliférer. Ces bactéries pourraient alors passer par le col utérin et contaminer l’espace chorio-décidual. La production accrue de cytokines inflammatoires, résultat de la réponse immune face à cette agression, stimulerait le recrutement de neutrophiles, la production de prostaglandines et la synthèse de métalloprotéases. Cette suite d’événements favoriserait la contractilité utérine, le raccourcissement du col, une fragilisation des membranes fœtales et pourrait aboutir à un accouchement prématuré. La contamination bactérienne vaginale initiale peut se poursuivre au niveau du fœtus via le liquide amniotique et le placenta. Dans 30 % des cas, le placenta présente des lésions inflammatoires microscopiques et des bactéries intestinales ont été identifiées dans le liquide amniotique [14]. Les séquelles dues à l’exposition du nouveau-né prématuré à un environnement inflammatoire intra-utérin se cumuleront à celles de son immaturité développementale, ce qui peut résulter en des troubles néonataux précoces et graves, telles une entérocolite nécrosante, une leucomalacie périventriculaire kystique ou une dysplasie broncho-pulmonaire.
 |
Figure 1. Cascade inflammatoire pouvant mener à la prématurité. Un déséquilibre de la flore vaginale permet la prolifération de pathogènes (1) et leur migration via le col utérin (2) vers l’espace chorio-décidual (3). Cette contamination va entraîner une production de cytokines pro-inflammatoires et de prostaglandine, le recrutement de neutrophiles et la synthèse de métalloprotéases. Ces événements peuvent mener à un accouchement prématuré suite à une contractilité du myomètre, au raccourcissement du col utérin ou à la rupture des membranes. |
Les deux principales modalités de colonisation bactérienne pouvant être évoquées pour expliquer l’infection de la cavité utérine seront décrites plus en détail : une colonisation ascendante en provenance du vagin ou de l’intestin et transitant par le col utérin et une transmission hématogène acheminant au placenta des bactéries en provenance de la circulation systémique.
Le microbiote vaginal
Un déséquilibre du microbiote vaginal, une vaginose bactérienne (VB) par exemple, caractérisée par une prolifération de bactéries anaérobies et un pH vaginal supérieur à 4,5, est associé à une augmentation de 40 % du risque de PTs [15]. Le traitement antibiotique de la VB ne diminue cependant pas ce risque et 50 % des femmes traitées vivront une récidive dans les 3 à 6 mois [16]. Cette constatation clinique soulève des questions quant à la pertinence de l’antibiothérapie dans ce contexte. Pour mieux comprendre le lien entre une flore vaginale déséquilibrée et la PTs, considérons tout d’abord la manière dont les Lactobacillus contribuent à l’équilibre du compartiment vaginal.
Les Lactobacillus vaginaux
Les Lactobacillus maintiennent un pH bas (3 à 4,5) et produisent du lactate, générant un environnement vaginal défavorable pour de nombreux pathogènes. Certaines espèces de Lactobacillus produisent des bactériocines, des peptides antimicrobiens qui affectent des pathogènes comme Enterococcus fæcalis ou Gardnerella vaginalis [17, 18] ou des médiateurs de l’immunité mucosale ciblant Escherichia coli [19]. Par sa capacité à adhérer à l’épithélium vaginal, la flore commensale, non pathogène, diminue les sites disponibles pour des pathogènes [20]. Une dysbiose vaginale pouvant être induite par un traitement antibiotique ou des changements hormonaux perturbera donc ce fragile équilibre. S’il se produit durant la grossesse, ce déséquilibre pourrait contribuer à enclencher ou à ne pas freiner la cascade infectieuse/inflammatoire pouvant mener à la PTs. Les particularités propres aux principales espèces bactériennes composant la flore apportent un éclairage sur leur lien avec l’issue de la grossesse. Stafford et ses collègues ont en effet décrit les CST et les caractéristiques métaboliques des espèces associées chez des femmes enceintes (Tableau II) [21]. Une CST de type I est dominée par L. crispatus, une espèce produisant une grande quantité d’acide lactique et plus particulièrement l’isomère de forme D. Cette flore, aussi décrite comme possédant un haut niveau d’inhibition de l’activité d’E. coli [22] et de L. gasseri (CST II), est la plus fréquemment identifiée en début de grossesse chez des femmes accouchant à terme. L’espèce L. iners (CST III) produit pour sa part la forme isomérique L de l’acide lactique qui possède la propriété de pouvoir induire l’expression de métalloprotéases au niveau de la matrice extracellulaire vaginale. Ces protéines peuvent agir sur l’intégrité du col utérin, favorisant son raccourcissement. Un fort taux de femmes (entre 58 et 85 % selon les études) accouchant avant terme présente une CST III [23]. Une flore dominée par L. jensenii (CST V) est, quant à elle, retrouvée deux fois moins fréquemment en début de grossesse chez les femmes qui accouchent à terme. Tout comme pour L. iners, cette espèce serait associée à une flore instable, plus susceptible de transiter d’une CST à une autre [24]. Un accouchement à terme serait donc plus fréquent avec une flore de type CST I et II : l’environnement vaginal créé par les espèces bactériennes dominantes et la diversité des protéines bactéricides qu’elles produisent freineraient la prolifération des espèces pathogènes. La diversité en Lactobacillus est un autre point à considérer dans la liste des facteurs associant la flore vaginale au risque de PTs [25]. Avec une unique espèce de lactobacilles, ce risque est plus élevé, d’autant plus si cette espèce est L. iners. Une CST III serait un état transitoire, signant une dysbiose pouvant évoluer vers une VB. Étant donné qu’une recolonisation par L. iners est fréquente à la suite d’un traitement antibiotique [26], ces données pourraient en partie expliquer l’inefficacité des traitements visant à diminuer la PT à la suite d’une VB.
Répartition des CST selon le type de naissance et description des principales caractéristiques des espèces de Lactobacillus. SA : semaines d’aménorrhée (d’après [20]).
La flore vaginale devrait être considérée comme un facteur modulable que l’on pourrait rééquilibrer en cas de dysbiose. Mesurer sa diversité et sa constitution permettrait de définir sa qualité et pourrait être réalisé par l’établissement d’un score de Nugent2 [27]. Cette identification microscopique des groupes bactériens présents dans les sécrétions vaginales serait une approche intéressante à explorer, en particulier chez les patientes avec des antécédents inexpliqués de PTs, ou avec une grossesse compliquée par un raccourcissement du col utérin. La détermination des CST n’est cependant pas possible à établir par la microscopie, mais cette méthode pourrait toutefois fournir des informations précieuses permettant d’évaluer la pertinence d’utiliser une approche thérapeutique à base de probiotiques.
Les autres sources de colonisation de l’utérus
La colonisation intra-utérine peut se produire à partir du transport sanguin de bactéries, un mode de dissémination qui a été mis en évidence dans des modèles murins par la détection placentaire de microorganismes marqués et inoculés par voie sanguine ou orale [28, 29]. L’hypothèse d’une transmission hématogène permettrait d’expliquer les observations cliniques associant parodontites et PTs. En effet, la bactérie Fusobacterium nucleatum, une espèce présente dans la plaque dentaire et fréquemment identifiée dans le placenta ou le liquide amniotique lors d’accouchements prématurés, pourrait faciliter ce mode de propagation par sa capacité à altérer la perméabilité des vaisseaux sanguins avec pour conséquence l’inefficacité de la barrière placentaire [30]. Le traitement de la parodontite a pu apparaître comme une approche intéressante pour prévenir la PTs, mais un essai clinique a montré qu’elle était inefficace [31]. Ces travaux soulèvent plusieurs questions : celle du moment auquel le traitement a été appliqué (le second trimestre de la grossesse), mais aussi celle de la nécessité de distinguer les cellules bactériennes vivantes des fragments d’ADN bactérien libres dans les échantillons biologiques. Si ce sont des bactéries vivantes qui auraient disséminé par voie sanguine, les mécanismes de leur transport restent à élucider. Les fragments bactériens peuvent diffuser vers le placenta et y être identifiés par des techniques de biologie moléculaire. Il est donc possible qu’ils ne soient pas impliqués dans la physiopathologie de la PTs et qu'ils ne jouent aucun rôle dans la biologie du placenta. Ils peuvent néanmoins être à l’origine de processus inflammatoires.
L’intestin héberge environ 4 x 1013 microorganismes classés en environ 3 000 groupes taxonomiques [32]. Le vagin n’est colonisé que par environ 300 taxons. La proximité anatomique entre intestin et région génitale pourrait permettre le transit de pathogènes intestinaux via le périnée, le vagin, puis le col utérin pour éventuellement pénétrer la cavité utérine. Ce parcours serait facilité par la présence chez les femmes à risque d’un bouchon muqueux qui serait déficient et trop perméable [33, 42] (→).
(→) Voir la Synthèse de B. Demouveaux et al., page ??? de ce numéro
La translocation bactérienne à travers la barrière mucosale de l’intestin vers l’utérus est un mode de propagation qui a aussi été suggéré. Les trompes de Fallope peuvent également constituer une porte d’entrée vers l’utérus, en laissant pénétrer des bactéries présentes dans la cavité péritonéale. Notons que ces différents modes de dissémination de bactéries vers l’utérus peuvent advenir en dehors de la grossesse, puisque cet organe possède aussi son propre microbiote [34]. À ce jour, aucune étude n’a évalué le lien entre la détection de certaines bactéries avant le début de la grossesse et son déroulement.
La prématurité, un syndrome polymicrobien ?
Les microorganismes impliqués dans la PTs et ceux de la flore commensale vaginale sont en interaction complexe. Cette situation peut être illustrée par E. coli qui profite de la fragilisation de l’endothélium des vaisseaux sanguins induite par la bactérie buccale F. nucleatum afin d’envahir le placenta et l’utérus. Une seconde voie possible pour E. coli serait de transiter au sein d’une flore vaginale permissive, riche en L. iners. Des travaux menés dans un modèle murin ont montré qu’une infection par le virus MHV-68 (murine gammaherpesvirus 68) diminue la capacité du col utérin à prévenir une infection bactérienne ascendante (provenant du vagin) et permet le passage de la bactérie Ureaplasma au niveau de l’utérus [35]. En l’absence de cette bactérie, MHV-68 n’a aucune conséquence sur le déroulement de la grossesse. Ces constatations font émerger un nouveau concept, celui d’une origine polymicrobienne de la PTs [36] qui, par opposition au terme « polybactérien », implique tous les microorganismes pouvant être présents chez l’hôte et qui constituent son microbiote. Le microbiote regroupe en effet non seulement les bactéries, mais aussi les virus, les levures et les mycètes, élargissant la diversité des microorganismes pouvant être associés à la PTs. En particulier, un virome (l’ensemble des génomes d’une population virale) vaginal très diversifié a été retrouvé chez des femmes ayant accouché prématurément [37]. La majorité des études portant sur le microbiote ne prennent pas actuellement en considération la présence d’une infection préexistante ou concomitante par un autre agent microbien. Une synergie ou une potentialisation des effets de ces pathogènes pourrait déclencher une cascade inflammatoire à l’origine de l’accouchement prématuré. Ainsi, l’observation de signes cliniques distincts tels qu’un début de travail prématuré ou le maintien d’une quiescence utérine chez des patientes présentant une infection par le même microorganisme pourrait s’expliquer par ce concept polymicrobien de la PT.
Perspectives
Pendant longtemps, des bactéries détectées dans le compartiment utérin étaient considérées comme un risque ou une cause de PTs. Un fœtus né à terme devait nécessairement s’être développé dans une cavité utérine stérile. Ce paradigme est désormais remis en question par des travaux récents ayant identifié des microorganismes dans le placenta et le liquide amniotique lors de grossesses menées à terme en l’absence de pathologie. Cette colonisation de faible niveau pourrait emprunter la voie hématogène ou résulter d’une translocation de bactéries provenant du MI à travers les épithéliums. La voie vaginale et cervicale n’est pas à exclure. Dans ce cas, certains Lactobacillus joueraient un rôle de filtre protégeant contre l’ascension de pathogènes intestinaux. Une antibiothérapie peut engendrer une perturbation de ce filtre vaginal et créer un environnement favorable au déclenchement d’une cascade d’évènements à l’origine d’une prématurité. Trente-neuf pour cent des nouveau-nés ont été exposés à une antibiothérapie anténatale [38]. Or des études suggèrent que ces traitements entraîneraient une augmentation de la transmission verticale de gènes de résistance aux antibiotiques entre bactéries et un accroissement du risque pour les nouveau-nés de développer une dermatite atopique ou de l’asthme durant l’enfance [6, 39]. Ces données sont particulièrement inquiétantes : le traitement par antibiotiques est en effet celui qui est le plus fréquemment prescrit durant la grossesse. Il apparaît donc primordial d’améliorer la prise en charge des patientes enceintes en proposant des alternatives ou des compléments thérapeutiques pour compenser les effets néfastes de cette médication sur les flores commensales.
L’utilisation de probiotiques apparaît de plus en plus comme une piste à explorer. En particulier, ils pourraient aider à rétablir une flore vaginale saine à la suite d’une VB et diminuer les risques de récidive. Des résultats prometteurs ont été obtenus avec des probiotiques administrés à des patientes présentant une RPPM. Ceux-ci ont en effet conduit, par rapport à un placebo, à une période de latence plus longue et à une amélioration de la santé du nouveau-né [40]. L’efficacité et la faisabilité d’auto-transplantations de microbiote pour restaurer une flore équilibrée au cours de la grossesse pourraient également être évaluées. Notons que ces thérapies modifiant la flore n’ont cependant le plus souvent qu’un effet transitoire.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Kim S, Covington A, Pamer EG. The intestinal microbiota: antibiotics, colonization resistance, and enteric pathogens. Immunol Rev 2017 ; 279 : 90–105. [CrossRef] [PubMed] [Google Scholar]
- Stiemsma LT, Michels KB. The role of the microbiome in the developmental origins of health and disease. Pediatrics 2018; 14. pii: e20172437. [PubMed] [Google Scholar]
- Romero R, Hassan SS, Gajer P, et al. The composition and stability of the vaginal microbiota of normal pregnant women is different from that of non-pregnant women. Microbiome 2014 ; 2 : 1. [CrossRef] [PubMed] [Google Scholar]
- Gajer P, Brotman RM, Bai G, et al. Temporal dynamics of the human vaginal microbiota. Sci Transl Med 2012; 4 : 132ra52. [CrossRef] [PubMed] [Google Scholar]
- Koren O, Goodrich JK, Cullender TC, et al. Host remodeling of the gut microbiome and metabolic changes during pregnancy. Cell 2012 ; 150 : 470–480. [CrossRef] [PubMed] [Google Scholar]
- Kuang YS, Lu JH, Li SH, et al. Connections between the human gut microbiome and gestational diabetes mellitus. Gigascience 2017 ; 6 : 1–12. [CrossRef] [Google Scholar]
- Brown RG, Marchesi JR, Lee YS, et al. Vaginal dysbiosis increases risk of preterm fetal membrane rupture, neonatal sepsis and is exacerbated by erythromycin. BMC Med 2018 ; 16 : 9. [CrossRef] [PubMed] [Google Scholar]
- Aagaard K, Ma J, Antony KM, et al. The placenta harbors a unique microbiome. Sci Transl Med 2014; 6 : 237ra65. [Google Scholar]
- Doyle RM, Alber DG, Jones HE, et al. Term and preterm labour are associated with distinct microbial community structures in placental membranes which are independent of mode of delivery. Placenta 2014 ; 35 : 1099–1101. [CrossRef] [PubMed] [Google Scholar]
- Lauder AP, Roche AM, Sherill-Mix S, Bailey A, et al. Comparison of placenta samples with contamination controls does not provide evidence for a distinct placenta microbiota. Microbiome 2016 ; 4 : 29. [CrossRef] [PubMed] [Google Scholar]
- Hackney DN, Olson-Chen C, Thornburg LL. What do we know about the natural outcomes of preterm labour? A systematic review and meta-analysis of women without tocolysis in preterm labour. Paediatr Perinat Epidemiol 2013 ; 27 : 452–460. [CrossRef] [PubMed] [Google Scholar]
- Peaceman AM, Lai Y, Rouse DJ, et al. Length of latency with preterm premature rupture of membranes before 32 weeks’ gestation. Am J Perinatol 2015 ; 32 : 57–62. [PubMed] [Google Scholar]
- Romero R, Mazor M. Infection and preterm labor. Clin Obstet Gynecol 1988 ; 31 : 553–584. [CrossRef] [PubMed] [Google Scholar]
- Mueller-Heubach E, , Rubinstein DN, Schwarz SS. Histologic chorioamnionitis and preterm delivery in different patient populations. Obstet Gynecol 1990 ; 75 : 622–626. [PubMed] [Google Scholar]
- Hillier SL, Nugent RP, Eschenbach DA, et al. Association between bacterial vaginosis and preterm delivery of a low-birth-weight infant. The vaginal infections and prematurity study group. N Engl J Med 1995 ; 333 : 1737–1742. [CrossRef] [PubMed] [Google Scholar]
- Borges S, Silva J, Teixeira P. The role of lactobacilli and probiotics in maintaining vaginal health. Arch Gynecol Obstet 2014 ; 289 : 479–489. [CrossRef] [PubMed] [Google Scholar]
- Vera Pingitore E, Hebert EM, Nader-Macias ME, Sesma F. Characterization of salivaricin CRL 1328, a two-peptide bacteriocin produced by Lactobacillus salivarius CRL 1328 isolated from the human vagina. Res Microbiol 2009; 160 : 401–8. [CrossRef] [PubMed] [Google Scholar]
- Aroutcheva A, Gariti D, Simon M, et al. Defense factors of vaginal lactobacilli. Am J Obstet Gynecol 2001 ; 185 : 375–379. [CrossRef] [Google Scholar]
- Kalyoussef S, Nieves E, Dinerman E, et al. Lactobacillus proteins are associated with the bactericidal activity against E. coli of female genital tract secretions. PLoS One 2012 ; 7 : e49506. [CrossRef] [PubMed] [Google Scholar]
- Boris S, Suarez JE, Vazquez F, Barbes C. Adherence of human vaginal lactobacilli to vaginal epithelial cells and interaction with uropathogens. Infect Immun 1998 ; 66 : 1985–1989. [PubMed] [Google Scholar]
- Stafford GP, Parker JL, Amabebe E, et al. Spontaneous preterm birth is associated with differential expression of vaginal metabolites by Lactobacilli-dominated microflora. Front Physiol 2017 ; 8 : 615. [CrossRef] [PubMed] [Google Scholar]
- Ghartey JP, Smith BC, Chen Z, et al. Lactobacillus crispatus dominant vaginal microbiome is associated with inhibitory activity of female genital tract secretions against Escherichia coli. PLoS One 2014 ; 9 : e96659. [CrossRef] [PubMed] [Google Scholar]
- Petricevic L, Domig KJ, Nierscher FJ, et al. Characterisation of the vaginal Lactobacillus microbiota associated with preterm delivery. Sci Rep 2014 ; 4 : 5136. [CrossRef] [PubMed] [Google Scholar]
- Verstraelen H, Verhelst R, Claeys G, et al. Longitudinal analysis of the vaginal microflora in pregnancy suggests that L. crispatus promotes the stability of the normal vaginal microflora and that L. gasseri and/or L. iners are more conducive to the occurrence of abnormal vaginal microflora. BMC Microbiol 2009 ; 9 : 116. [CrossRef] [PubMed] [Google Scholar]
- Haque MM, Merchant M, Kumar PN, et al. First-trimester vaginal microbiome diversity: A potential indicator of preterm delivery risk. Sci Rep 2017 ; 7 : 16145. [CrossRef] [PubMed] [Google Scholar]
- Witkin SS, Alvi S, Bongiovanni AM, et al. Lactic acid stimulates interleukin-23 production by peripheral blood mononuclear cells exposed to bacterial lipopolysaccharide. FEMS Immunol Med Microbiol 2011 ; 61 : 153–158. [CrossRef] [Google Scholar]
- Nugent RP, Krohn MA, Hillier SL. Reliability of diagnosing bacterial vaginosis is improved by a standardized method of gram stain interpretation. J Clin Microbiol 1991 ; 29 : 297–301. [PubMed] [Google Scholar]
- Fardini Y, Chung P, Dumm R, et al. Transmission of diverse oral bacteria to murine placenta: evidence for the oral microbiome as a potential source of intrauterine infection. Infect Immun 2010 ; 78 : 1789–1796. [CrossRef] [PubMed] [Google Scholar]
- Jiménez E, Marín ML, , Martín R, et al. Is meconium from healthy newborns actually sterile?. Res Microbiol 2008 ; 159 : 187–193. [CrossRef] [PubMed] [Google Scholar]
- Fardini Y, Wang X, Temoin S, et al. Fusobacterium nucleatum adhesin FadA binds vascular endothelial cadherin and alters endothelial integrity. Mol Microbiol 2011 ; 82 : 1468–1480. [CrossRef] [PubMed] [Google Scholar]
- Newnham JP, Newnham IA, Ball CM, et al. Treatment of periodontal disease during pregnancy: a randomized controlled trial. Obstet Gynecol 2009 ; 114 : 1239–1248. [CrossRef] [PubMed] [Google Scholar]
- Sender R, Fuchs S et Milo R. Revised estimates for the number of human and bacteria cells in the body. PLoS Biol 2016; 14 : e1002533. [CrossRef] [PubMed] [Google Scholar]
- Smith-Dupont KB, , Wagner CE, Witten J, Conroy K, et al. Probing the potential of mucus permeability to signify preterm birth risk. Sci Rep 2017 ; 7 : 10302. [CrossRef] [PubMed] [Google Scholar]
- Chen C, Song X, Wei W, et al. The microbiota continuum along the female reproductive tract and its relation to uterine-related diseases. Nat Commun 2017 ; 8 : 875. [CrossRef] [PubMed] [Google Scholar]
- Racicot K, Cardenas I, Wunsche V, et al. Viral infection of the pregnant cervix predisposes to ascending bacterial infection. J Immunol 2013 ; 191 : 934–941. [CrossRef] [PubMed] [Google Scholar]
- Payne MS, Bayatibojakhi S. Exploring preterm birth as a polymicrobial disease: an overview of the uterine microbiome. Front Immunol 2014 ; 5 : 595. [CrossRef] [PubMed] [Google Scholar]
- Wylie KM, Wylie TN, Cahill AG, Macones GA, et al. The vaginal eukaryotic virome and preterm birth. Am J Obstet Gynecol 2018; 219 : 189.e1–189.e12. [CrossRef] [Google Scholar]
- Azad MB, Konya T, Persaud RR, et al. Impact of maternal intrapartum antibiotics, method of birth and breastfeeding on gut microbiota during the first year of life: a prospective cohort study. BJOG 2016 ; 123 : 983–993. [CrossRef] [PubMed] [Google Scholar]
- Nogacka A, Salazar N, Suarez M, et al. Impact of intrapartum antimicrobial prophylaxis upon the intestinal microbiota and the prevalence of antibiotic resistance genes in vaginally delivered full-term neonates. Microbiome 2017 ; 5 : 93. [CrossRef] [PubMed] [Google Scholar]
- Daskalakis GJ, Karambelas AK. Vaginal probiotic administration in the management of preterm premature rupture of membranes. Fetal Diagn Ther 2016 ; 42 : 92–98. [CrossRef] [PubMed] [Google Scholar]
- Gschwind R, Fournier T, Butel MJ, Wydau-Dematteis S, Établissement du microbiote : une colonisation in utero déterminante pour la santé future ?. Med Sci (Paris) 2018 ; 34 : 331–337. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Demouveaux B, Gouyer V, Magnien M, et al. La structure des mucines conditionne les propriétés viscoélastiques des gels de mucus. Med Sci (Paris) 2018; 34 : ???. [Google Scholar]
Liste des tableaux
Répartition des CST chez les femmes en dehors de la grossesse (d’après [4]).
Répartition des CST selon le type de naissance et description des principales caractéristiques des espèces de Lactobacillus. SA : semaines d’aménorrhée (d’après [20]).
Liste des figures
 |
Figure 1. Cascade inflammatoire pouvant mener à la prématurité. Un déséquilibre de la flore vaginale permet la prolifération de pathogènes (1) et leur migration via le col utérin (2) vers l’espace chorio-décidual (3). Cette contamination va entraîner une production de cytokines pro-inflammatoires et de prostaglandine, le recrutement de neutrophiles et la synthèse de métalloprotéases. Ces événements peuvent mener à un accouchement prématuré suite à une contractilité du myomètre, au raccourcissement du col utérin ou à la rupture des membranes. |
| Dans le texte | |
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.




