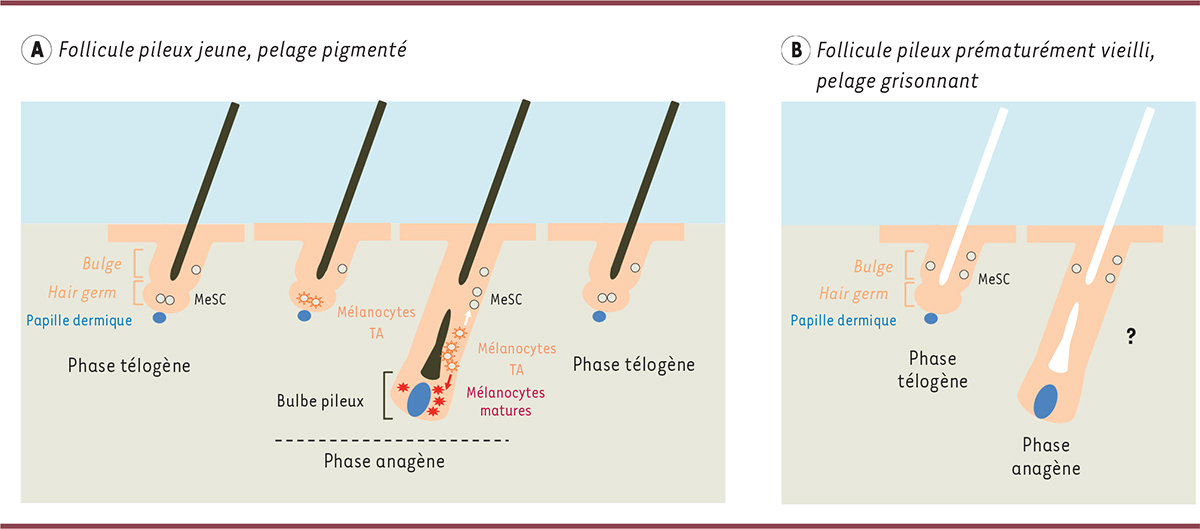
Figure 1.
Télécharger l'image originale
A. Le maintien des cellules souches des mélanocytes (MeSC) du follicule pileux repose sur la dédifférenciation cellulaire. En phase télogène, la partie inférieure du follicule pileux se compose du bulge et du hair germ (HG). Bulge et HG contiennent les cellules souches du follicule pileux (hair follicle stem cells, HFSC, non représentées) distinguables par l’expression de CD34 (bulge) et de la P-cadhérine (HG). Juste en dessous du HG, des cellules mésenchymateuses spécialisées forment la papille dermique (en bleu), qui contrôle l’activation des HFSC et la régénération du follicule pileux [1, 2, 4–6, 14, 15]. Dans la plupart des follicules pileux en phase télogène de la souris jeune (pigmentée), les MeSC (en blanc) sont exclusivement présentes dans le HG, où elles forment une population étroitement rassemblée. Une petite minorité des follicules pileux présentent en plus des MeSC dans le bulge (cas représenté ici). Au début de la phase anagène, les MeSC du HG sont activées par l’induction du signal Wnt [7, 8]. Elles engendrent une population de cellules intermédiaires, les mélanocytes TA (transit-amplifying) (en orange), qui migrent vers la base du follicule pileux en croissance. Une partie des mélanocytes TA maintiennent un signal Wnt actif et achèvent leur différenciation (flèche rouge) en mélanocytes matures pigmentés (en rouge) dans le bulbe pileux. Une autre partie des mélanocytes TA remontent vers le bulge ou l’ORSup (upper outer root sheath), une région située juste en dessous du bulge en phase anagène [1, 8]. Dans ce cas, la migration est associée à une extinction du signal Wnt et à une dédifférenciation (flèche blanche) en MeSC, qui se relocalisent généralement dans le HG lors de la phase télogène suivante (cas représenté), ou restent parfois dans le bulge. Notons que les MeSC du bulge présentent une faible prolifération (non représentée) en milieu ou fin de phase anagène [8]. Chez les souris transgéniques (Oca2creER ; RosaLSL-tdTomato) utilisées pour mettre en évidence la dédifférenciation des mélanocytes en MesC, la séquence codant la recombinase conditionnelle creER est insérée (knock-in) dans le gène du marqueur tardif de la différenciation mélanocytaire Oca2. L’activation transcriptionnelle de Oca2 s’accompagne donc de celle de creER, qui, en présence de l’inducteur tamoxifène, déclenche l’expression irréversible (transmise à toute la descendance de la cellule) de la protéine fluorescente rouge tdTomato, détectable directement par un procédé non invasif. L’expression de tdTomato atteste donc d’au moins un engagement dans la différenciation mélanocytaire jusqu’au stade OCA2+, et les MeSC tdTomato+ sont par conséquent issues de la dédifférenciation de mélanocytes (partiellement) différenciés (mélanocytes TA OCA2+). Pour le suivi des MeSC pendant un cycle pilaire complet à partir de la phase télogène, une autre lignée de souris a été utilisée (TyrcreER;RosaLSL-tdTomato) permettant de déclencher le marquage dans les MeSC lors de la phase télogène initiale. Dans les deux lignées de souris, le suivi en direct (live imaging) est réalisé lors du premier cycle pilaire (à partir de l’âge de 21 jours environ) : un même follicule pileux est observé à plusieurs reprises lors du cycle et les conditions choisies permettent une analyse clonale (déclenchement du marquage dans une seule cellule par follicule pileux) [8]. B. Mécanisme proposé pour le grisonnement précoce des souris dans un modèle de vieillissement accéléré du follicule pileux. Le vieillissement des follicules pileux a été artificiellement accéléré par des épilations répétées en phase télogène pour induire sept cycles pilaires (ou six, suivis d’un vieillissement naturel pendant 8 mois). À l’issue de cette période, les souris grisonnent, et la répartition des MeSC est fortement modifiée : elles ont disparu du HG dans un dixième des follicules pileux, mais sont présentes dans le bulge de la majorité d’entre eux, où elles apparaissent dispersées. Dans certains follicules pileux vieillissants (cas représenté), les MeSC sont situées exclusivement dans le bulge. Dans d’autres cas (non représentés), des MeSC s’accumulent dans le bulge, mais sont aussi encore présentes dans le HG [8]. Chez la souris jeune (pigmentée), les (rares) MeSC du bulge n’engendrent pas de mélanocytes matures lors de la phase anagène, à la différence de celles du HG [8]. Les auteurs postulent donc que, dans ce modèle de follicule pileux vieillissant, l’accumulation de MeSC dans le bulge en même temps que leur disparition (ou raréfaction) dans le HG diminue leur capacité à se différencier, ce qui cause le grisonnement. Toutefois, le devenir des MeSC du bulge en phase anagène n’a pas été étudié dans les follicules pileux vieillissants, et les auteurs ne montrent pas directement que les follicules pileux dépigmentés correspondent bien à ceux qui ont accumulé des MeSC dans le bulge et perdu celles du HG [8]. Certaines structures associées au follicule pileux ne sont pas représentées (par exemple la glande sébacée), et le nombre de cellules dessinées est volontairement réduit.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




