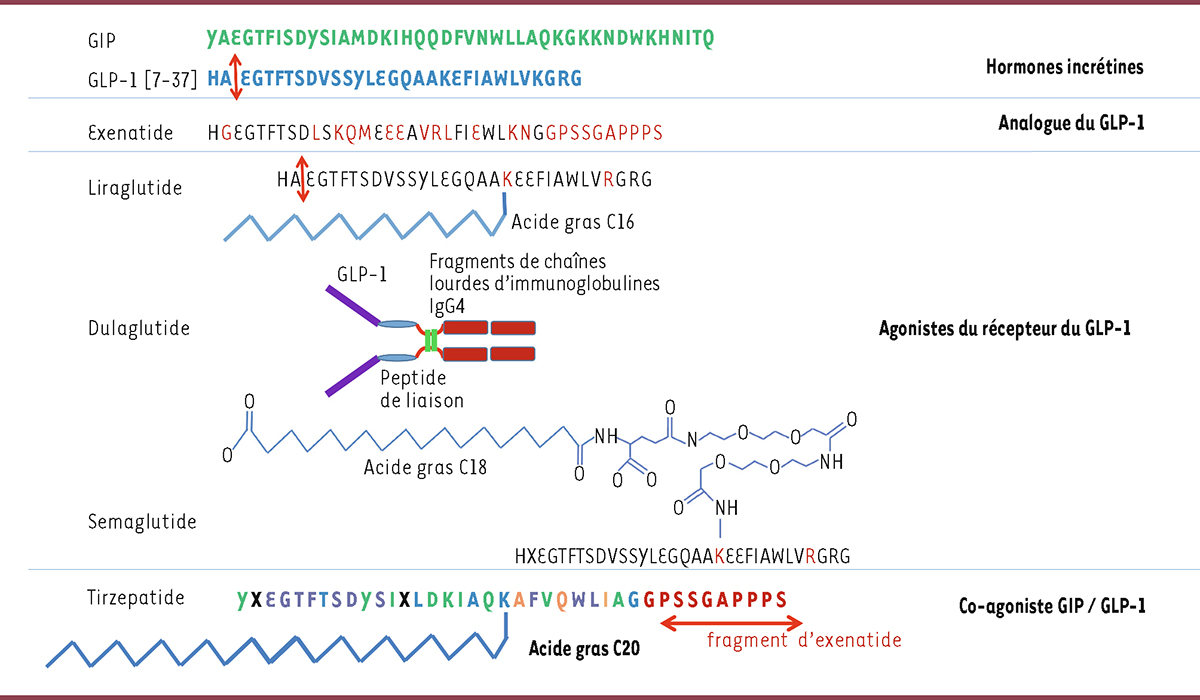
Figure 5.
Télécharger l'image originale
Molécules thérapeutiques analogues du GLP-1 et du GIP disponibles avec une indication thérapeutique pour le diabète de type 2. L’exénatide a une demi-vie plus longue que le GLP-1 actif grâce à une substitution de l’acide aminé en position 2 (alanine remplacée par glycine) conférant une résistance à la dégradation par la dipeptidyl peptidase-4 (DPP-IV), qui reconnaît les motifs histidine-alanine). Le liraglutide résulte d’une part, de l’ajout (par un linker) d’un acide gras à 16 atomes de carbone sur la lysine en position 16 du GLP-1 [7-37] et, d’autre part, du remplacement de la lysine en position 34 par une arginine. Le dulaglutide résulte de la fusion de deux molécules d’un analogue du GLP-1 (identique au GLP-1 natif à 90 %) reliées par un peptide de liaison à deux fragments de chaîne lourde d’immunoglobuline IgG4. Le sémaglutide résulte de deux substitutions d’acides aminés (alanine en position 2 remplacée par l’acide 2-aminoisobutyrique, et lysine en position 34 remplacée par une arginine) par rapport au GLP-1 [7-37]. En position 26, une lysine est liée à un acide gras à 19 atomes de carbone par un linker, ce qui permet une forte liaison à l’albumine, une réduction de la clairance rénale et une augmentation de la demi-vie. Les séquences peptidiques du GIP et du GLP-1 ont des acides aminés en commun. Le tirzépatide, co-agoniste GIP / GLP-1, a une plus forte affinité pour le récepteur du GIP que pour celui du GLP-1 car sa structure est basée sur celle du GIP natif (acides aminés en vert), qui contient des acides aminés communs avec le GLP-1 (en violet). Pour augmenter la demi-vie de la molécule, les acides aminés en position 2 et 13 du GIP et du GLP-1 natifs ont été remplacés par l’acide 2-aminoisobutyrique, ce qui confère au tirzépatide une résistance à la dégradation par la DPP-IV. La demi-vie de la molécule de tirzépatide est également augmentée par l’ajout d’un acide gras à 20 atomes de carbone (par une liaison avec une lysine en position 20 du GLP-1 natif) qui permet sa liaison à l’albumine. Enfin, l’addition d’une partie de l’exénatide à la partie C-terminale du tirzépatide est une troisième modification allongeant la demi-vie de la molécule. La flèche rouge indique le site d’action de l’enzyme DPP-IV sur la séquence d’acides aminés histidine-alanine (HA). Pour le tirzépatide, les acides aminés proviennent du GIP (en vert), du GLP-1 (en bleu), ou de l’exénatide (en rouge), ou sont communs au GIP et au GLP-1 (en violet), ou ne sont présents ni dans le GIP ni dans le GLP-1 (en orange) ; X indique l’acide 2-aminoisobutyrique.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




