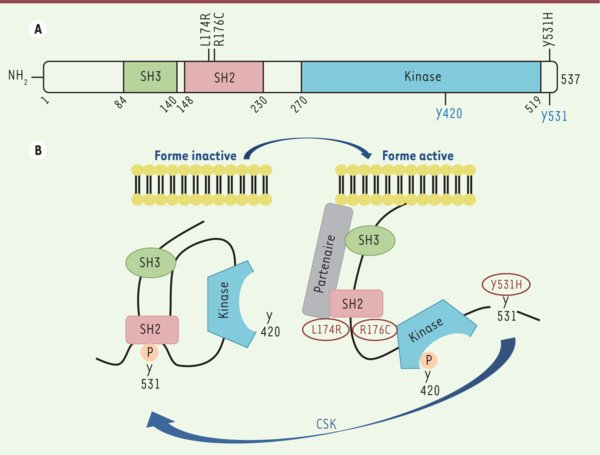
Figure 1.
Télécharger l'image originale
Protéine FYN. A. Structure protéique de FYN montrant les domaines identifiés et la localisation des mutations observées dans les échantillons de PTCL. B. Régulation de l’activité de la SRC kinase FYN. À l’état inactif, la tyrosine 531 située à l’extrémité carboxy-terminale de la protéine est phosphorylée par l’enzyme CSK, et son interaction avec le domaine SH2 maintient la protéine dans une configuration inactive. Dans l’état actif, la tyrosine 531 est déphosphorylée, et la tyrosine 420 située dans la boucle d’activation du domaine kinase est phosphorylée. Les mutants L174R, R176C et Y531H abolissent l’interaction entre le domaine SH2 et la phosphotyrosine 531, permettant une configuration ouverte et active de la protéine, qui résiste à l’action de CSK.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




