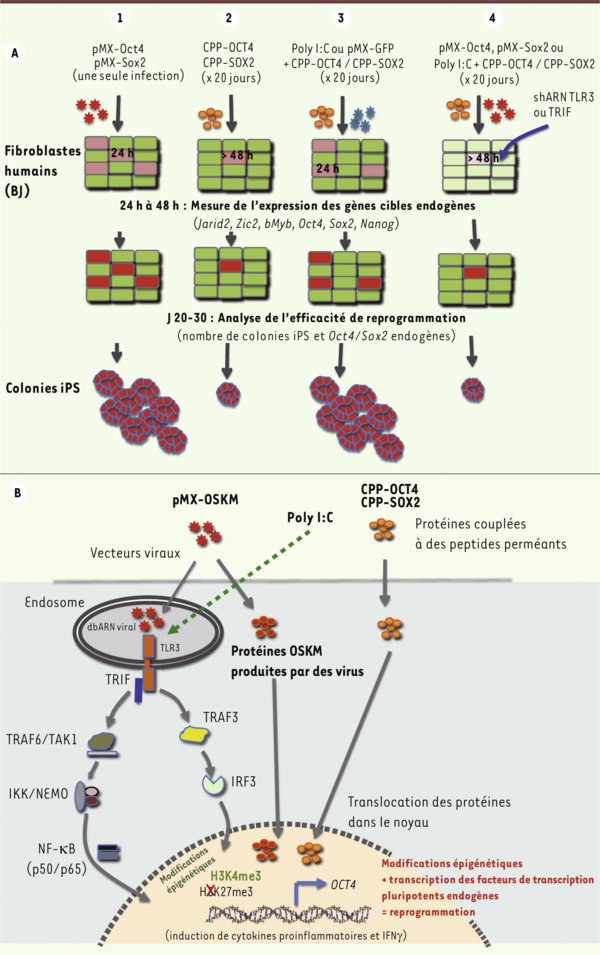
Figure 1.
Télécharger l'image originale
Contribution de l’immunité innée à la reprogrammation de fibroblastes humains en cellules souches pluripotentes iPS. A. Schéma expérimental ayant conduit à l’identification du rôle de TLR3. La transduction de fibroblastes humains par des rétrovirus porteurs des ADNc codant OSKM (1) est 10 à 100 fois plus efficace que la transduction de ces mêmes cellules par des protéines OSKM recombinantes couplées à des peptides perméants (CPP-OSKM) (2) pour (a) induire l’expression précoce des gènes endogènes pluripotents, et (b) assurer une reprogrammation complète en iPS. L’addition aux protéines CPP-OSKM d’un virus non relevant (pMX-GFP) ou de poly I:C, un agoniste de TLR3 non viral, restaure un processus de reprogrammation efficace (3) . L’inhibition de la reprogrammation lorsque TLR-3 ou TRIF sont inhibées (4) confirme l’implication de cette voie de l’immunité innée. B. Mécanisme d’action de TLR3 sur la reprogrammation. L’ARN double brin des rétrovirus (ou les transcrits OSKM modifiés non représentés ici) est reconnu par TLR3. La voie de signalisation TLR3 en aval est activée et agit via IRF3 d’une part et NF-κB d’autre part. En synergie avec les protéines OSKM qui migrent aussi dans le noyau, ces acteurs entraînent des modifications épigénétiques qui contribuent à la dérépression des gènes pluripotents endogènes, une étape décisive de la reprogrammation. Il est probable que l’activation de TLR3 aboutisse aussi à l’expression de gènes codant les cytokines proinflammatoires (non représentées ici).
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




