| Issue |
Med Sci (Paris)
Volume 28, Number 6-7, Juin–Juillet 2012
|
|
|---|---|---|
| Page(s) | 599 - 604 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2012286012 | |
| Published online | 16 juillet 2012 | |
La transmission des infections à Pneumocystis
Transmission of Pneumocystis infection in humans
1
Laboratoire de parasitologie-mycologie, faculté des sciences pharmaceutiques, université Lille-Nord-de-France, 59037 Lille, France
2
EA4547, Inserm U1019, CNRS UMR8204, centre d’infection et d’immunité de Lille (CIIL), France
3
Institut Pasteur de Lille, 1, rue du Pr Calmette, 59019 Lille, France
4
Service de parasitologie-mycologie, faculté de médecine, centre hospitalier régional universitaire (CHRU) de Lille, université Lille-Nord-de-France, 59037 Lille, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
La pneumonie à Pneumocystis (PcP) est-elle une infection fongique transmissible ? Existe-t-il une PcP nosocomiale et/ou une transmission communautaire des infections par Pneumocystis ? Inabordables jusqu’aux années 2000, ces questions peuvent être explorées à l’heure actuelle soit chez l’homme grâce au développement de méthodes de détection non invasives, soit au laboratoire où des modèles de transmission de l’infection ont été développés. Représenté par une seule entité (P. carinii) pendant presqu’un siècle, le genre Pneumocystis contient actuellement plusieurs espèces, P. jirovecii étant la seule identifiée chez l’homme. Les études moléculaires associées à des expériences d’infection croisée ont révélé une forte spécificité d’hôte qui interdit la transmission interespèces. En revanche, la transmission respiratoire entre mammifères d’une même espèce est en général très active, même entre hôtes immunocompétents. D’autres voies de transmission existeraient. Les études montrent que le seul réservoir de P. jirovecii est l’être humain qui constituerait la seule source d’infection aussi bien à l’hôpital que dans la communauté.
Abstract
Is Pneumocystis pneumonia (PcP) a transmissible fungal disease? Does nosocomial PcP occur? Is there Pneumocystis transmission in the community? These questions, which could not be tackled before the 2000s, may at present be approached using either noninvasive detection methods or experimental transmission models. Represented by a unique entity (P. carinii) for almost one century, the Pneumocystis genus was shown to contain several species, being P. jirovecii the sole species identified in humans hitherto. Molecular methods combined with cross infection experiments revealed strong host specificity that precludes Pneumocystis inter-species transmission. In contrast, respiratory transmission between mammals of a same species is usually highly active, even between immunocompetent hosts. Other transmission ways could also exist. New data show that human being is the unique P. jirovecii reservoir; it would constitute the sole infection source in both hospital and community.
© 2012 médecine/sciences – Inserm / SRMS
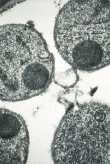
Photo : Pneumocystis jirovecii, ultrastructure (kyste mature) (© Eduardo Dei-Cas).
Pneumocystis : un nouveau défi ?
En 1990, dans cette même revue médecine/sciences, nous évoquions le défi que lançait aux biologistes l’entité pathogénique alors appelée Pneumocystis carinii [1]. À cette époque, les techniques de biologie moléculaire commençaient à lever le voile sur la taxonomie, jusqu’alors incertaine, de ces micro-organismes en révélant leur nature fongique. En l’absence d’un modèle de culture efficace, le recours aux modèles animaux semblait indispensable pour étudier la biologie de ces parasites atypiques, responsables, à cette époque, du décès de 25 % des malades atteints du Sida (syndrome d’immunodéficience acquise).
Cependant, durant les 20 dernières années, le cadre conceptuel appliqué à Pneumocystis et aux infections causées par les membres du genre a subi des changements radicaux. On peut parler d’une sorte de microrévolution des connaissances qui évoque, d’une certaine façon, la notion de révolution scientifique de Kuhn [2], selon laquelle un changement de paradigme entraîne, d’une part, la caducité de conceptions considérées jusqu’alors comme fondamentales et, d’autre part, l’émergence, autour d’un nouveau paradigme, de nouvelles notions qui requièrent la tranformation du langage spécifique associé (Tableau I). Dans cette synthèse, nous tenterons d’examiner ces transitions radicales, notamment les changements taxonomiques dans le genre Pneumocystis, leur impact pratique en clinique, les recherches sur la transmission de ce pathogène suscitées par ces conceptions, et d’autres aspects en relation avec l’émergence d’un nouveau schéma pour penser l’histoire naturelle des infections par Pneumocystis et leurs conséquences en pathologie humaine et animale. Il s’agit aujourd’hui de relever le défi en répondant aux questions suivantes : la pneumonie à Pneumocystis (PcP) est-elle une infection fongique transmissible ? Existe-t-il une PcP nosocomiale et/ou une transmission communautaire des infections par Pneumocystis ?
Pneumocystis et pneumocystoses : changement radical du cadre conceptuel.
Pneumocystis et pneumocystose aujourd’hui
La pneumonie à Pneumocystis, pneumonite interstitielle sévère en général bilatérale et diffuse due à Pneumocystis jirovecii, se présente comme une infection cosmopolite touchant typiquement des sujets en situation de profonde immunodépression. De nos jours, la pneumocystose reste l’infection indicatrice de Sida la plus fréquente en Europe occidentale malgré l’utilisation de la chimioprophylaxie instaurée depuis les années 1980 et des multithérapies antirétrovirales hautement actives [3]. Aujourd’hui, elle est présente également chez des patients non infectés par le VIH (virus de l’immunodéficience humaine) et souffrant d’autres causes d’immunodépression, primaires ou secondaires : cancer, hémopathie maligne, affection inflammatoire chronique, immunosuppression dans le cadre d’une transplantation de moelle osseuse ou d’organes [4]. Chez ces patients immunodéprimés, l’incidence de la PcP varie de 10 à 40 % et le taux de mortalité peut atteindre 50 % [5].
Par ailleurs, depuis les années 1990, les techniques moléculaires de détection, très sensibles et appliquées à des prélèvements non invasifs tels que le liquide de rinçage oropharyngé, ont permis d’identifier l’existence de porteurs de Pneumocystis. Ces patients porteurs colonisés par le micromycète sont habituellement identifiés par la positivité de la PCR (polymerase chain reaction) Pneumocystis pratiquée sur un prélèvement respiratoire, alors que l’examen microscopique est négatif et que les signes cliniques et radiologiques de pneumocystose sont absents [6]. Ainsi, P. jirovecii peut être détecté chez des sujets apparemment sains, adultes et enfants (ces derniers développant dans plus de 90 % des cas une primo-infection par P. jirovecii avant l’âge de 4 ans) [7]. Les femmes enceintes, les patients sous corticoïdes, immunodéprimés, atteints de maladies systémiques ou encore de maladies pulmonaires chroniques comme la bronchopneumopathie chronique obstructive (BPCO) peuvent également être colonisés par le champignon [6]. Il est intéressant de noter que des arguments cliniques et expérimentaux de plus en plus nombreux indiquent que Pneumocystis peut être un facteur de comorbidité chez les patients atteints de BPCO [8, 9]. Ainsi, lorsque l’on parle d’infection par Pneumocystis, on ne peut plus se limiter à la PcP et à son caractère opportuniste. Il est en effet probable que l’impact clinico-épidémiologique réel des infections par Pneumocystis soit à l’heure actuelle sous estimé.
Le genre Pneumocystis : d’une seule entité taxonomique à de nombreuses espèces sténoxènes
Il est difficile, par la seule microscopie optique, de distinguer les microchampignons du genre Pneumocystis (Tableau II) qui se développent dans les poumons des mammifères, ce qui explique qu’ils aient été considérés pendant presqu’un siècle comme une seule entité taxonomique : P. carinii, décrite par P. et M. Delanoë en 1912 [10]. Cependant, les découvertes de ces 20 dernières années ont remis en cause cette perception. L’importance de l’hétérogénéité génétique mais aussi caryotypique, antigénique, ultrastructurale et physiologique des isolats de Pneumocystis, corrélée avec l’espèce des mammifères hôtes, ainsi que les résultats infructueux d’expériences d’infection croisée ont montré l’existence d’une forte spécificité d’hôte [10]. De plus, les études récentes sur la coévolution des Pneumocystis et de leurs hôtes témoignent de l’adaptation très ancienne de ces parasites aux mammifères [11, 12]. Ainsi, le genre Pneumocystis regroupe des populations génétiquement isolées, qui ont subi un long processus d’adaptation à chaque espèce de mammifère, entraînant une spéciation [10]. Le statut des populations naturelles des organismes du genre Pneumocystis conforte ainsi la définition biologique d’espèce [13, 14]. En conséquence, les organismes du genre Pneumocystis doivent actuellement être décrits en tant qu’espèces et nommés comme telles [15]. À l’heure actuelle, cinq espèces ont été décrites : P. jirovecii chez l’homme, P. carinii et P. wakefieldiae chez le rat (Rattus norvegicus), P. murina chez la souris (Mus musculus), et P. oryctolagi chez le lapin (Oryctolagus cuniculus) [10].
Caractérisation des différents stades du cycle biologique des organismes du genre Pneumocystis. Les formes trophiques (2-8 µm), amiboïdes, mononucléées à paroi cellulaire fine, évolueraient en sporocytes arrondis (3-6 µm) et puis en kystes (ou asques) (4-6 µm), à paroi cellulaire épaisse, qui vont générer huit spores (ou ascospores). Ces dernières quitteraient le kyste, très probablement à travers un pore préformé de sa paroi cellulaire, s’attacheraient aux cellules épithéliales alvéolaires de type 1 (pneumocytes 1) et recommenceraient le cycle. Le contenu en ADN des divers stades parasitaires de l’espèce Pneumocystis carinii du rat (Rattus norvegicus) a été déterminé récemment en employant des méthodes cytométriques à haut débit [32]. La plupart des stades sont haploïdes mais, comme pour d’autres ascomycètes, les formes trophiques de P. carinii développent une conjugaison qui conduit à la formation d’un stade diploïde. Une division réductionnelle méiotique survient alors chez le sporocyte précoce, suivie de divisions équationnelles mitotiques dont résulteront les huit noyaux des spores haploïdes.
Cette étroite spécificité parasitaire indique que les êtres humains ne peuvent pas contracter une infection par Pneumocystis à partir d’une source animale : la PcP n’est donc pas une zoonose (Tableau I) mais une anthroponose. Les populations humaines représenteraient donc l’unique réservoir de P. jirovecii.
Les espèces de Pneumocystis sont activement transmises par voie respiratoire
Il a été bien démontré expérimentalement, principalement grâce aux modèles murins, que Pneumocystis se transmet entre hôtes de la même espèce par voie respiratoire, cas unique parmi les champignons pathogènes [6, 16]. Le champignon est de surcroît hautement transmissible, car un seul jour de contact entre une souris porteuse de PcP et une souris susceptible est suffisant pour que la seconde soit infectée [17]. Cependant, le ou les stades parasitaires vecteurs de cette transmission de l’infection sont toujours inconnus. De plus, même si l’ADN de Pneumocystis a été identifié par PCR dans des filtrats d’air en milieu rural et dans l’eau, dans l’air d’animaleries hébergeant des animaux infectés et dans des chambres de patients atteints de PcP, aucun stade parasitaire n’a pu être identifié morphologiquement [6].
Les modèles murins de transmission aérienne naturelle de Pneumocystis, largement utilisés dans notre laboratoire, ont également permis d’étudier le rôle d’animaux porteurs immunocompétents dans la transmission de ces parasites. Ainsi, des mises en contact étroit (souris placées dans la même cage) de souris SCID (severe combined immunodeficient mice) infectées par PcP (P. murina) avec des souris immunocompétentes indemnes de P. murina permettent d’obtenir des souris immunocompétentes porteuses du champignon, mais non malades (Figure 1). Ces souris immunocompétentes, porteuses de Pneumocystis, sont capables de transmettre l’infection à des souris SCID saines qui, elles, développeront la maladie, mais aussi à d’autres souris immunocompétentes, qui, à leur tour, transmettront l’infection à un hôte susceptible (Figure 1) [18, 19]. De plus, des approches moléculaires et histologiques nous ont permis de déterminer que les hôtes immunocompétents porteurs du champignon pouvaient servir de réservoir des Pneumocystis species. En effet, les parasites détectés chez ces hôtes immunocompétents étaient viables et capables de se répliquer [19]. Des résultats comparables ont été obtenus par une équipe américaine ayant utilisé le même modèle expérimental [20].
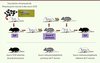 |
Figure 1. Modèle murin de transmission aérienne naturelle de Pneumocystis. Des souris immunodéprimées ou souris SCID (severe combined immunodeficiency) sont inoculées par Pneumocystis murina (P. murina) et développent, environ 6 semaines après, une pneumocystose. Elles sont alors mises en contact dans la même cage avec des souris immunocompétentes (souris Balb/c) qui deviennent porteuses de P. murina. Ces souris Balb/c porteuses de P. murina sont capables d’éliminer radicalement les parasites de leurs poumons en 5 à 6 semaines. Cependant, tant qu’elles sont porteuses, elles sont capables de transmettre l’infection à de nouvelles souris Balb/c, ou alors à de nouvelles souris SCID qui elles développent la maladie. De plus, les souris Balb/c devenues porteuses de P. murina après contact avec des souris Balb/c porteuses du champignon, sont également capables de transmettre l’infection à des souris SCID qui développeront une pneumocystose [19]. IC : immunocompétente. |
Ces chercheurs ont montré que des anticorps IgG anti-Pneumocystis apparaissent chez la souris immunocompétente 3 à 4 semaines après le contact infectant, et que les parasites sont éliminés totalement du poumon au bout de 5 à 6 semaines [20].
Dans leur ensemble, ces résultats suggèrent que le réservoir de Pneumocystis serait un réservoir dynamique constitué par l’ensemble des membres des populations d’hôtes. Chez ces hôtes, plus ou moins susceptibles à Pneumocystis en fonction de leur statut immunitaire, le parasite se développerait (même transitoirement) dans les poumons, assurant la production de formes infectantes et la transmission de l’agent infectieux à de nouveaux hôtes. La succession de génotypes de P. jirovecii décrite récemment chez des patients atteints de mucoviscidose mais sans pneumonie à Pneumocystis, illustre parfaitement ce concept [21].
La transmission de Pneumocystis jirovecii est nosocomiale et communautaire
Tout d’abord, il est aujourd’hui admis que les pneumocystoses ne résultent pas de la réactivation d’une infection latente acquise dans l’enfance, mais d’une contamination de novo [6]. L’idée d’une transmission interindividuelle de P. jirovecii a, quant à elle, été suspectée dès les années 1950, avec la description des premières épidémies survenant chez des enfants prématurés ou malnutris [22, 23]. Plus récemment, des études combinant l’observation de cas groupés de PcP en milieu hospitalier et la mise en évidence de l’identité génotypique des isolats de P. jirovecii trouvés chez ces patients ont renforcé cette idée [6]. Les principaux marqueurs ont été définis dans la séquence des gènes codant pour la grande (mtLSUrARN) ou la petite sous-unité (mtSSUrARN) de l’ARN ribosomal mitochondrial, la dihydroptéroate synthétase (DHPS) et des espaceurs internes transcrits (ITS) de Pneumocystis. Par ailleurs, des cas groupés d’infection à Pneumocystis ont également été rapportés en milieu domestique. Récemment, Rivero et al. ont émis l’hypothèse d’une transmission du champignon entre des grands-parents immunocompétents porteurs de P. jirovecii et leur petite-fille [24]. De l’ADN de Pneumocystis a également été détecté chez des sujets immunocompétents dans l’entourage étroit de patients VIH positifs ou négatifs atteints ou non de PcP [6]. Le rôle potentiel de réservoir de ces populations immunocompétentes porteuses de P. jirovecii a alors été suggéré. A fortiori, le rôle du personnel soignant dans la circulation de P. jirovecii à l’hôpital a été discuté, identifiant un impact nosocomial potentiel de l’infection par Pneumocystis [25, 26].
Ainsi, d’assez nombreuses observations semblent attester d’une circulation active de P. jirovecii dans l’environnement hospitalier comme dans la communauté, où patients et porteurs pourraient constituer en même temps des réservoirs efficaces et des sources potentielles d’infection [3, 25, 27, 28]. Clarifier les mécanismes impliqués dans la transmission aérienne de Pneumocystis est un prérequis important pour définir des stratégies de prévention de cette maladie. Ainsi, pour des raisons scientifiques mais également pratiques (comme prévenir la transmission nosocomiale de la PcP), la communauté scientifique s’est récemment intéressée à l’étude de la dynamique de contamination par Pneumocystis de l’environnement aérien d’hôtes atteints de pneumocystose. Il a ainsi été montré que Pneumocystis était détectable dans l’air exhalé de rats infectés, la charge fongique aérienne étant proportionnelle à la charge fongique pulmonaire [29]. Chez l’homme, la même équipe a montré que P. jirovecii était dispersé dans l’environnement aérien proche des patients développant une PcP et que la charge fongique diminuait quand on s’éloignait du patient jusqu’à devenir indétectable [30]. Des techniques de RT-PCR (reverse transcriptase PCR) ont, quant à elles, permis de montrer que les champignons P. jirovecii détectés dans l’air sont viables, et donc potentiellement infectieux [31].
Compte tenu des résultats obtenus lors des expérimentations animales citées plus haut et de ces observations chez l’homme, la transmission interhumaine à partir de malades immunodéprimés infectés par Pneumocystis mais aussi de patients colonisés et de porteurs sains, semble aujourd’hui plus que probable. Les études récentes renforçant l’hypothèse d’une transmission nosocomiale de la pneumocystose sur le mode interhumain strict ont bien entendu des implications pour l’instauration de mesures de prévention de cette infection (séparation géographique des patients atteints de PcP et/ou des sujets colonisés des patients susceptibles ; mesures d’isolement de type « gouttelettes » ou « respiratoire ») car, à l’heure actuelle, la prévention n’est fondée que sur la seule chimioprophylaxie.
Transmission verticale dans le genre Pneumocystis
La transmission horizontale par voie aérienne ne semble pas être l’unique modalité de transmission inter-hôtes des Pneumocystis species. En effet, des preuves d’une transmission verticale par voie transplacentaire ont été trouvées chez certains mammifères comme le lapin (Oryctolagus cuniculus) et les primates, dont les placentas sont similaires, hémodichorial et hémomonochorial, respectivement [6]. La transmissibilité in utero de Pneumocystis species a également été explorée chez les rats et souris mais elle ne semble pas se produire chez ces rongeurs, qui ont eux un placenta hémotrichorial [6]. L’hypothèse d’une transmission transplacentaire du champignon chez l’homme, longtemps suspectée, vient d’être renforcée par la détection récente d’ADN de P. jirovecii dans les poumons de fœtus et dans le placenta chez des femmes ayant fait des fausses couches [32]. Cette voie de transmission pourrait permettre au champignon une dissémination « protégée » vis-à-vis d’aléas environnementaux. Ces résultats montrent également l’intérêt d’explorer le mode de transmission in utero de Pneumocystis en s’interrogeant sur le rôle potentiel de ce champignon dans certains avortements « spontanés », éventualité qui n’a pas, jusqu’à maintenant, été évoquée chez l’homme à notre connaissance.
Conclusions
Les évolutions techniques et conceptuelles auxquelles ont été confrontés les biologistes et cliniciens s’intéressant aux Pneumocystis species, et que nous venons d’évoquer dans cette revue, ont ébranlé les connaissances initiales sur l’histoire naturelle des infections par Pneumocystis et ont fait émerger une nouvelle conceptualisation de l’épidémiologie de ces infections fongiques. La pneumonie à Pneumocystis ne représenterait en fait qu’une rareté dans le spectre clinicopathologique de ces infections. La colonisation de sujets sans aucun déficit immunitaire par Pneumocystis pourrait poser un problème de santé publique, et de nouvelles études seront nécessaires pour comprendre la signification clinique de ce portage et confirmer si ces sujets porteurs peuvent transmettre Pneumocystis à l’hôpital et dans la communauté.
Liens d’intérêt
E. Dei-Cas déclare participer à des interventions ponctuelles pour la Commission européenne, l'Institut Pasteur de Lille et des universités en France et à l'étranger.
M. Chabé et I. Durand-Joly déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Dei-Cas E, Soulez B, Palluault F, et al. Pneumocystis carinii, un défi pour le biologiste. Med Sci (Paris) 1990 ; 6 : 517–525. [CrossRef] [Google Scholar]
- Kuhn TS. Qué son las revoluciones científicas? y otros ensayos. Barcelona : Paidós ICE UAB, 1996 : 152 p. [Google Scholar]
- Calderon EJ, Gutiérrez-Rivero S, Durand-Joly I, et al. Pneumocystis infection in humans: diagnosis and treatment. Expert Rev Anti Infect Ther 2010 ; 8 : 683–701. [CrossRef] [PubMed] [Google Scholar]
- Catherinot E, Lanternier F, Bougnoux ME, et al. Pneumocystis jirovecii pneumonia. Infect Dis Clin North Am 2010 ; 24 : 107–138. [CrossRef] [PubMed] [Google Scholar]
- Monnet X, Vidal-Petiot E, Osman D et al. Critical care management, outcome of severe Pneumocystis pneumonia in patients with, without HIV infection. Crit Care 2008 ; 12 : R28. [CrossRef] [PubMed] [Google Scholar]
- Chabé M, Nevez G, Totet A, et al. Transmission de Pneumocystis. J Mycol Med 2009 ; 19 : 276–284. [CrossRef] [Google Scholar]
- Peglow SL, Smulian AG, Linke MJ, et al. Serologic responses to Pneumocystis carinii antigens in health and disease. J Infect Dis 1990 ; 161 : 296–306. [CrossRef] [PubMed] [Google Scholar]
- Calderón EJ, Rivero L, Respaldiza N, et al. Systemic inflammation in patients with chronic obstructive pulmonary disease who are colonized with Pneumocystis jiroveci. Clin Infect Dis 2007 ; 45 : e17–e19. [CrossRef] [PubMed] [Google Scholar]
- Norris KA, Morris A. Pneumocystis infection and the pathogenesis of chronic obstructive pulmonary disease. Immunol Res 2011 ; 50 : 175–180. [CrossRef] [PubMed] [Google Scholar]
- Chabé M, Aliouat-Denis CM, Delhaes L, et al. Pneumocystis : from a doubtful unique entity to a group of highly diversified fungal species. FEMS Yeast Res 2011 ; 11 : 2–17. [CrossRef] [PubMed] [Google Scholar]
- Demanche C, Berthelemy M, Petit T, et al. Phylogeny of Pneumocystis carinii from 18 primate species confirms host specificity and suggests coevolution. J Clin Microbiol 2001 ; 39 : 2126–2133. [CrossRef] [PubMed] [Google Scholar]
- Hugot JP, Demanche C, Barriel V, et al. Phylogenetic systematics and evolution of primate-derived Pneumocystis based on mitochondrial or nuclear DNA sequence comparison. Syst Biol 2003 ; 52 : 735–744. [CrossRef] [PubMed] [Google Scholar]
- Mayr E. Animal species and evolution. Cambridge : The Belknap Press of Harvard University Press, 1963 : 798 p. [Google Scholar]
- Stringer JR, Wakefield AE, Cushion MT, et al. Pneumocystis taxonomy and nomenclature: an update. J Eukaryot Microbiol 1997 ; 44 : S5–S6. [CrossRef] [Google Scholar]
- Frenkel JK. Pneumocystis pneumonia, an immunodeficiencydependent disease (IDD): a critical historical overview. J Eukaryot Microbiol 1999 ; 46 : S89–S92. [Google Scholar]
- Aliouat-Denis CM, Chabé M, Demanche C, et al. Pneumocystis species, co-evolution and pathogenic power. Infect Genet Evol 2008 ; 8 : 708–726. [CrossRef] [PubMed] [Google Scholar]
- Soulez B, Palluault F, Cesbron JY, et al. Introduction of Pneumocystis carinii in a colony of SCID mice. J Protozool 1991 ; 38 : S123–S125. [Google Scholar]
- Dumoulin A, Mazars E, Seguy N, et al. Transmission of Pneumocystis carinii disease from immunocompetent contacts of infected hosts to susceptible hosts. Eur J Clin Microbiol Infect Dis 2000 ; 19 : 671–678. [CrossRef] [PubMed] [Google Scholar]
- Chabé M, Dei-Cas E, Creusy C, et al. Immunocompetent hosts as a reservoir of Pneumocystis organisms: histological and RT-PCR data demonstrate active replication. Eur J Clin Microbiol Infect Dis 2004 ; 3 : 89–97. [Google Scholar]
- An CL, Gigliotti F, Harmsen AG. Exposure of immunocompetent adult mice to Pneumocystis carinii f. sp. muris by cohousing: growth of P. carinii f. sp. muris and host immune response. Infect Immun 2003 ; 71 : 2065–70. [CrossRef] [PubMed] [Google Scholar]
- Montes-Cano MA, de la Horra C, Dapena FJ, et al. Dynamic colonisation by different Pneumocystis jirovecii genotypes in cystic fibrosis patients. Clin Microbiol Infect 2007 ; 13 : 1008–1011. [Google Scholar]
- Ammich O. Über die nichtsyphilitische interstitielle Pneumonie des ersten Kindesalters. Virchows Arch A Pathol Anat Histol 1938 ; 302 : 539–554. [CrossRef] [Google Scholar]
- Gajdusek DC. Pneumocystis carinii; etiologic agent of interstitial plasma cell pneumonia of premature and young infants. Pediatrics 1957 ; 19 : 543–565. [PubMed] [Google Scholar]
- Rivero L, de la Horra C, Montes-Cano MA, et al. Pneumocystis jirovecii transmission from immunocompetent carriers to infant. Emerg Infect Dis 2008 ; 14 : 1116–1118. [Google Scholar]
- Durand-Joly I, Soula F, Chabe M, et al. Long-term colonization with Pneumocystis jirovecii in hospital staffs: a challenge to prevent nosocomial pneumocystosis. J Eukaryot Microbiol 2003 ; 50 : 614–615. [CrossRef] [PubMed] [Google Scholar]
- Nevez G, Chabé M, Rabodonirina M, et al. Nosocomial Pneumocystis jirovecii infections. Parasite 2008 ; 15 : 359–365. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Vargas SL, Ponce CA, Gigliotti F, et al. Transmission of Pneumocystis carinii DNA from a patient with P. carinii pneumonia to immunocompetent contact health care workers. J Clin Microbiol 2000 ; 38 : 1536–1538. [PubMed] [Google Scholar]
- Miller RF, Ambrose HE, Wakefield AE. Pneumocystis carinii f. sp. hominis DNA in immunocompetent health care workers in contact with patients with P. carinii pneumonia. J Clin Microbiol 2001 ; 39 : 3877–3882. [CrossRef] [PubMed] [Google Scholar]
- Choukri F, Aliouat EM, Menotti J, et al. Dynamics of Pneumocystis carinii air shedding during experimental pneumocystosis. J Infect Dis 2011 ; 9 : 1333–1336. [CrossRef] [Google Scholar]
- Choukri F, Menotti J, Sarfati C, et al. Quantification and spread of Pneumocystis jirovecii in the surrounding air of patients with Pneumocystis pneumonia. Clin Infect Dis 2010 ; 3 : 259–265. [CrossRef] [Google Scholar]
- Latouche S, Totet A, Lacube P, et al. Development of an RT-PCR on the heat shock protein 70 gene for viability detection of Pneumocystis carinii f. sp. hominis in patients with pneumocystosis and in air sample. J Eukaryot Microbiol 2001 ; suppl : S176–S177. [CrossRef] [Google Scholar]
- Montes-Cano MA, Chabé M, Fontillon-Alberdi M, et al. Vertical transmission of Pneumocystis jirovecii in humans. Emerg Infect Dis 2009 ; 15 : 125–127. [CrossRef] [PubMed] [Google Scholar]
- Martinez A, Aliouat EM, Standaert-Vitse A, et al. Ploidy of cell-sorted trophic and cystic forms of Pneumocystis carinii. PLoS One 2011 ; 6 : e20935. [CrossRef] [PubMed] [Google Scholar]
Liste des tableaux
Caractérisation des différents stades du cycle biologique des organismes du genre Pneumocystis. Les formes trophiques (2-8 µm), amiboïdes, mononucléées à paroi cellulaire fine, évolueraient en sporocytes arrondis (3-6 µm) et puis en kystes (ou asques) (4-6 µm), à paroi cellulaire épaisse, qui vont générer huit spores (ou ascospores). Ces dernières quitteraient le kyste, très probablement à travers un pore préformé de sa paroi cellulaire, s’attacheraient aux cellules épithéliales alvéolaires de type 1 (pneumocytes 1) et recommenceraient le cycle. Le contenu en ADN des divers stades parasitaires de l’espèce Pneumocystis carinii du rat (Rattus norvegicus) a été déterminé récemment en employant des méthodes cytométriques à haut débit [32]. La plupart des stades sont haploïdes mais, comme pour d’autres ascomycètes, les formes trophiques de P. carinii développent une conjugaison qui conduit à la formation d’un stade diploïde. Une division réductionnelle méiotique survient alors chez le sporocyte précoce, suivie de divisions équationnelles mitotiques dont résulteront les huit noyaux des spores haploïdes.
Liste des figures
 |
Figure 1. Modèle murin de transmission aérienne naturelle de Pneumocystis. Des souris immunodéprimées ou souris SCID (severe combined immunodeficiency) sont inoculées par Pneumocystis murina (P. murina) et développent, environ 6 semaines après, une pneumocystose. Elles sont alors mises en contact dans la même cage avec des souris immunocompétentes (souris Balb/c) qui deviennent porteuses de P. murina. Ces souris Balb/c porteuses de P. murina sont capables d’éliminer radicalement les parasites de leurs poumons en 5 à 6 semaines. Cependant, tant qu’elles sont porteuses, elles sont capables de transmettre l’infection à de nouvelles souris Balb/c, ou alors à de nouvelles souris SCID qui elles développent la maladie. De plus, les souris Balb/c devenues porteuses de P. murina après contact avec des souris Balb/c porteuses du champignon, sont également capables de transmettre l’infection à des souris SCID qui développeront une pneumocystose [19]. IC : immunocompétente. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




