| Issue |
Med Sci (Paris)
Volume 27, Number 6-7, Juin–Juillet 2011
|
|
|---|---|---|
| Page(s) | 587 - 589 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2011276009 | |
| Published online | 1 juillet 2011 | |
Des souris humanisées pour l’étude du virus de l’hépatite C
Humanized mice for the study of hepatitis C
Inserm U1016, CNRS UMR 8104, Université Paris Descartes, Institut Cochin 24, rue du Faubourg Saint-Jacques 75014 Paris, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
L’hépatite chronique C, ce sont 170 millions de patients infectés dans le monde dont environ 30 % évolueront vers une cirrhose. Jusqu’à présent, le traitement associait un interféron et un analogue nucléosidique avec un succès relatif dépendant du type de virus et de facteurs intrinsèques aux patients. Le développement récent de nouvelles antiprotéases et antipolymérases ravive le problème du manque criant de modèles cellulaires et animaux adéquats pour étudier leur efficacité et leur mode d’action. Un modèle cellulaire idéal permettrait de reproduire fidèlement l’intégralité du cycle viral, de l’entrée du virus à sa réplication. Un modèle animal permettrait, de plus, d’étudier la physiopathologie de la maladie en y intégrant la réaction immunitaire induite par l’infection et de tester l’efficacité vaccinale ou thérapeutique de nouvelles drogues. Or, le tropisme du virus restreint à l’homme et aux primates non humains limite l’utilisation d’autres espèces. Par ailleurs, la différenciation et la maturation complète des hépatocytes sont requises pour que ceux-ci soient infectés par le virus de l’hépatite C (VHC), caractéristiques qu’il est bien difficile de maintenir en culture primaire, même à moyen terme.
Les modèles de culture du VHC et leurs améliorations ont été récemment présentés dans ces colonnes [9, 10]. La possibilité d’infecter efficacement et de produire des particules virales à partir de tranches de foies humains issues de biopsies, c’est-à-dire dans un contexte cellulaire naturel, semble également très prometteuse (S. Lagaye et S. Pol, communication personnelle).
Premiers modèles murins ayant un foie « humanisé » : les souris uPA et FAH -/-
Qu’en est-il des petits modèles animaux permettant d’aborder les questions relevant de l’immunité et de l’efficacité des combinaisons thérapeutiques à moyen terme ? Avant que ne soient développées des souris au foie humanisé, le seul modèle animal naturel infectable par le VHC humain était une civette arboricole, vivant essentiellement en Asie du Sud-Est et dont le petit nom, tupaia, signifie écureuil en malais. Difficile pourtant d’envisager le développement d’un élevage de cet animal sauvage dans le cadre d’une recherche académique. L’idée d’implanter des hépatocytes humains chez la souris immunodéprimée a alors conduit il y a une dizaine d’années à l’obtention de « trimères ». Les souris subissent à la fois une transplantation de moelle osseuse de souris SCID (severe combined immunodeficient) - ce qui prévient le développement d’une réaction immunitaire - ainsi que l’implantation, sous la capsule rénale, d’une tranche de foie humain préalablement infectée par le VHC. L’ARN du VHC est encore détecté un mois après dans le sérum de la souris greffée [1]. Ce modèle a ainsi servi à valider l’efficacité préclinique d’anticorps dirigés contre la protéine d’enveloppe E2 [2].
Le développement des premiers modèles murins de repeuplement total du foie par des hépatocytes transplantés a permis d’aller un peu plus loin dans l’établissement de souris au foie humanisé. Les deux modèles existants, la souris transgénique uPA (urokinase plasminogen activator) et la souris tyrosinémique (FAH -/- ) fonctionnent sur le même concept : dans les deux cas, les hépatocytes résidents sont continuellement détruits, par un transgène toxique dans le cas du modèle uPA et par un défaut constitutif d’une enzyme du cycle de l’urée, la fumaryl-acide-acéto-hydrolase, dans le cas de la souris FAH -/- . Cette cytolyse induit un stimulus de prolifération, ce qui confère aux hépatocytes transplantés un avantage prolifératif sur les hépatocytes résidents, puisqu’ils ne subissent pas la pression de sélection négative de ces derniers. Successivement, l’équipe de E.P. Sandgren puis celle de M. Grompe, sont donc parvenues à repeupler quasi-entièrement le foie de souris transgéniques uPA et FAH -/- à partir d’un million seulement d’hépatocytes transplantés. Après des croisements successifs avec des animaux de fond génétique immunodéprimé SCID, les souris uPA permirent l’implantation, le maintien et la prolifération d’hépatocytes humains [3]. Il ne restait alors plus qu’à démontrer que ces souris au foie partiellement humanisé étaient infectables par le VHC et, ainsi, à confirmer l’efficacité thérapeutique de différentes drogues comme l’interféron ou les antiprotéases [4]. L’importance de la réponse immunitaire innée dans l’histoire naturelle de l’infection virale C a également pu être démontrée grâce à ce modèle [5]. Il fut beaucoup plus long et laborieux d’obtenir des souris humanisées à partir du modèle FAH -/- , les auteurs ayant dû, pour y parvenir, faire des croisements successifs avec des animaux de fond génétique Rag2γC. Ces souris sont en effet dépourvues de cellules natural killer (NK) et déplétées en macrophages murins résidents. L’infection de cette souris immunodéprimée par le VHC n’a été que récemment démontrée [6]. En revanche, l’absence d’un système immunitaire humain fonctionnel ne permet d’induire une fibrose hépatique dans aucun de ces modèles.
Souris humanisées pour le système immunitaire et le foie : un modèle idéal d’infection par le VHC ?
Quel est, finalement, le cahier des charges pour l’obtention d’un modèle idéal de souris humanisée permettant l’étude du cycle du VHC et celle de ses inhibiteurs potentiels ? Il faut tout d’abord faire de la place au sein du parenchyme hépatique afin que les hépatocytes humains puissent s’y diviser, autrement dit conférer un avantage sélectif négatif aux hépatocytes résidents ; les hépatocytes transplantés doivent d’autre part rester différenciés, ou être capables d’acquérir un niveau de différenciation terminale, faute de quoi ils ne seront pas infectés par le VHC. Ainsi, un tel modèle n’a-t-il pas encore été obtenu avec des cellules souches embryonnaires (ES) ou des cellules souches pluripotentes reprogrammées (iPS), leur niveau de différenciation étant, pour le moment encore, insuffisant pour valider ce paramètre [11]. Enfin, le système immunitaire de la souris doit être, lui aussi, humanisé, pour espérer reproduire toute la physiopathologie de la maladie. Ces différents critères semblent désormais réunis dans un modèle qui vient d’être publié dans la revue Gastroenterology [7].
L’animal receveur est une souris transgénique exprimant dans ses hépatocytes une caspase 8 dimérisable et donc activable par une drogue dépourvue d’autres effets biologiques. Un tel modèle avait déjà été obtenu avec la caspase 3 [8], révélant qu’il était possible d’induire à façon une mort hépatocytaire programmée par apoptose, sans effet bystander sur les cellules avoisinantes ou transplantées, laissant ainsi la possibilité d’y implanter des hépatocytes humains (Figure 1). Des animaux transgéniques nouveau-nés sur fond génétique Rag2γC exprimant cette bombe à retardement ont été irradiés et transplantés à la fois par des cellules souches hématopoïétiques CD34+ et des cellules progénitrices hépatocytaires, ces deux populations étant issues de mêmes foies fœtaux humains de 16 semaines. Environ 15 % des cellules du foie chimérique expriment l’albumine humaine entre 1 à 4 mois après la transplantation. Les animaux présentent également des cellules immunitaires humaines dans tous leurs organes lymphoïdes. Les souris ainsi humanisées pour le système immunitaire et le foie ont alors été inoculées avec le sérum d’un patient porteur d’une hépatite chronique C de génotype 1a (Figure 2). L’ARN du virus est détecté chez la moitié d’entre elles, bien que la virémie ne soit pas détectable dans le sérum des animaux. Ce défaut de détection est probablement dû au niveau encore trop faible d’hépatocytes humains dans le foie des souris. L’infection par le VHC engendre une réponse humaine T spécifique. Cette réaction immunitaire à l’infection permet l’infiltration du foie par des cellules CD45+, des macrophages et des cellules T CD3+ humaines et, de façon remarquable, le développement d’un processus fibrotique semblable à celui qui est observé lors d’une infection VHC chronique chez l’homme. Ce premier modèle de souris humanisées à la fois sur le plan immunitaire et hépatocytaire est donc un outil de choix pour mieux comprendre l’infection virale C, la co-infection VIH-VHC et l’efficacité de nouvelles molécules thérapeutiques, mais aussi pour aborder l’étude de la physiopathologie de la fibrose induite par le virus de l’hépatite C. Si des résultats équivalents pouvaient être obtenus avec des hépatocytes congelés ou des iPS différenciées en hépatocytes, l’utilisation de cette approche en serait grandement facilitée !
 |
Figure 1 Modèle d’apoptose hépatique inductible à façon. Le transgène est composé d’un site de myristoylation (M) suivi de deux séquences FKBP fusionnées à une caspase, en aval d’un promoteur hépatospécifique (non représenté ici). Les séquences FKBP ont été modifiées pour lier un composé non toxique dérivé du FK1012 (AP20187) et inducteur de dimérisation (CID). Le foie des animaux transgéniques correspondants est normal (coloration hémalun-éosine d’une coupe de foie en haut à gauche, grossissement x 200). L’administration intrapéritonéale du CID entraîne la dimérisation et l’activation de la caspase qui induira l’apoptose des cellules qui l’expriment. En quelques heures, le foie des animaux transgéniques présente une apoptose massive (coloration hémalun-éosine d’une coupe de foie en bas à gauche, grossissement x 200), visualisée par une coloration plus rouge des hépatocytes et des corps de Councilman avec condensation nucléaire (astérisque blanche) (d’après [8]). |
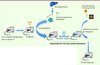 |
Figure 2 Protocole d’infection virale C d’une souris humanisée. Des animaux transgéniques nouveau-nés exprimant la construction illustrée dans la Figure 1 et sur fond immunodéprimé Rag2γC sont irradiés et reçoivent une transplantation de cellules CD34+ et progénitrices hépatiques issues d’un même foie fœtal humain de 15 à 18 semaines. L’administration de l’inducteur de dimérisation de la caspase (CID), en induisant une apoptose des hépatocytes résidents, permet l’expansion des cellules hépatiques humaines au sein du foie receveur. L’inoculation d’un sérum de patient présentant une hépatite chronique C de génotype 1a permet l’infection des hépatocytes humains qui, en association à la réponse immunitaire humaine qu’elle provoque, induit une fibrose hépatique. CSH : cellules souches hématopoïétiques. |
Conflit d’intérêts
L’auteur déclare n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
Références
- Ilan E, Burakova T, Dagan S, et al. The hepatitis B virus-trimera mouse: a model for human HBV infection and evaluation of anti-HBV therapeutic agents. Hepatology 1999 ; 29 : 553-562. [CrossRef] [PubMed] [Google Scholar]
- Eren R, Landstein D, Terkieltaub D, et al. Preclinical evaluation of two neutralizing human monoclonal antibodies against hepatitis C virus (HCV): a potential treatment to prevent HCV reinfection in liver transplant patients. J Virol 2006 ; 80 : 2654-2664. [CrossRef] [PubMed] [Google Scholar]
- Dandri M, Burda MR, Torok E, et al. Repopulation of mouse liver with human hepatocytes and in vivo infection with hepatitis B virus. Hepatology 2001 ; 33 : 981-988. [CrossRef] [PubMed] [Google Scholar]
- Kneteman NM, Weiner AJ, O’Connell J, et al. Anti-HCV therapies in chimeric scid-Alb/uPA mice parallel outcomes in human clinical application. Hepatology 2006 ; 43 : 1346-1353. [CrossRef] [PubMed] [Google Scholar]
- Waters L, Nelson M. New therapeutic options for hepatitis C. Curr Opin Infect Dis 2006 ; 19 : 615-622. [CrossRef] [PubMed] [Google Scholar]
- Bissig KD, Wieland SF, Tran P, et al. Human liver chimeric mice provide a model for hepatitis B and C virus infection and treatment. J Clin Invest 2010 ; 120 : 924-930. [CrossRef] [PubMed] [Google Scholar]
- Washburn ML, Bility MT, Zhang L, et al. A humanized mouse model to study hepatitis C virus infection, immune response, and liver disease. Gastroenterology 2011 ; 140 : 1334-1344. [CrossRef] [PubMed] [Google Scholar]
- Mallet VO, Mitchell C, Guidotti JE, et al. Conditional cell ablation by tight control of caspase-3 dimerization in transgenic mice. Nat Biotechnol 2002 ; 20 : 1234-1239. [CrossRef] [PubMed] [Google Scholar]
- Rosenberg AR, Carpentier A, Podevin P. Enfin un modèle de culture du virus de l’hépatite C adapté aux hépatocytes humains primaires!. Med Sci (Paris) 2010 ; 26 : 1013-1014. [Google Scholar]
- Legrand-Abravanel F, Izopet J. Culture du virus de l’hépatite C. enfin Med Sci (Paris) 23 : 588-589. [Google Scholar]
- Touboul T, Vallier L, Weber A. Cellules souches embryonnaires humaines et iPS - Une source fiable d’hépatocytes fœtaux. Med Sci (Paris) 2010 ; 26 : 1061-1066. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
© 2011 médecine/sciences – Inserm / SRMS
Liste des figures
 |
Figure 1 Modèle d’apoptose hépatique inductible à façon. Le transgène est composé d’un site de myristoylation (M) suivi de deux séquences FKBP fusionnées à une caspase, en aval d’un promoteur hépatospécifique (non représenté ici). Les séquences FKBP ont été modifiées pour lier un composé non toxique dérivé du FK1012 (AP20187) et inducteur de dimérisation (CID). Le foie des animaux transgéniques correspondants est normal (coloration hémalun-éosine d’une coupe de foie en haut à gauche, grossissement x 200). L’administration intrapéritonéale du CID entraîne la dimérisation et l’activation de la caspase qui induira l’apoptose des cellules qui l’expriment. En quelques heures, le foie des animaux transgéniques présente une apoptose massive (coloration hémalun-éosine d’une coupe de foie en bas à gauche, grossissement x 200), visualisée par une coloration plus rouge des hépatocytes et des corps de Councilman avec condensation nucléaire (astérisque blanche) (d’après [8]). |
| Dans le texte | |
 |
Figure 2 Protocole d’infection virale C d’une souris humanisée. Des animaux transgéniques nouveau-nés exprimant la construction illustrée dans la Figure 1 et sur fond immunodéprimé Rag2γC sont irradiés et reçoivent une transplantation de cellules CD34+ et progénitrices hépatiques issues d’un même foie fœtal humain de 15 à 18 semaines. L’administration de l’inducteur de dimérisation de la caspase (CID), en induisant une apoptose des hépatocytes résidents, permet l’expansion des cellules hépatiques humaines au sein du foie receveur. L’inoculation d’un sérum de patient présentant une hépatite chronique C de génotype 1a permet l’infection des hépatocytes humains qui, en association à la réponse immunitaire humaine qu’elle provoque, induit une fibrose hépatique. CSH : cellules souches hématopoïétiques. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




