| Numéro |
Med Sci (Paris)
Volume 27, Numéro 5, Mai 2011
|
|
|---|---|---|
| Page(s) | 527 - 534 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2011275019 | |
| Publié en ligne | 25 mai 2011 | |
Administration de molécules actives dans les cellules
Le potentiel des peptides de pénétration cellulaire
Potential of cell penetrating peptides for cell drug delivery
Équipe canaux calciques, fonctions et pathologies, Institut des neurosciences de Grenoble, Inserm U836; Université Joseph Fourier, site Santé de La Tronche, BP 170, 38042 Grenoble Cedex 9, France
*
cathy.poillot@ujf-grenoble.fr
**
michel.dewaard@ujf-grenoble.fr
L’intérêt de la communauté scientifique pour les peptides de pénétration cellulaire (CPP) s’accroît depuis quelques années et leur nombre ne cesse d’augmenter. Ces peptides sont des outils puissants pour l’acheminement des molécules actives jusqu’à leur site d’action. En effet, de nombreuses drogues qui ne peuvent franchir les membranes cellulaires ont, en revanche, pu être efficacement transportées dans les cellules lorsqu’elles étaient couplées à un peptide de pénétration cellulaire. De nombreux cargos ont ainsi pu être fixés sur des peptides de pénétration cellulaire : oligonucléotides, molécules aux activités pharmacologiques connues, agents de contraste pour l’imagerie, nanoparticules agissant comme des plates-formes aux fonctionnalités multimodales, etc. Cette revue montre le formidable potentiel des peptides de pénétration cellulaire et leur large diversité d’usage, mais surtout, elle envisage leur future destinée dans les applications cliniques et le traitement des maladies.
Abstract
The interest of the scientific community for cell penetrating peptides (CPP) has been growing exponentially for these last years, and the list of novel CPP is increasing. These peptides are powerful tools for the delivery of cargoes to their site of action. Indeed, several drugs that cannot translocate through the cell plasma membrane have been successfully delivered into cells when grafted to a CPP. Various cargoes have been linked to CPP, such as oligonucleotides, pharmacologically active drugs, contrast agents for imaging, or nanoparticles as platforms for multigrafting purposes… This review illustrates the fabulous potential of CPP and the diversity of their use, but their most interesting application appears their future clinical use for the treatment of various pathological conditions.
© 2011 médecine/sciences – Inserm / SRMS
Les premiers peptides de pénétration cellulaire : historique et définition
Le principal obstacle à l’administration de molécules actives dans l’organisme vient du blocage qu’oppose la membrane plasmique à l’entrée dans les cellules des molécules hydrophiles. Un accès intracellulaire pour ces composés s’effectue donc au prix de leur administration répétée et massive ou par le biais de stratégies de formulation adéquates. Une méthode permettant de pallier ce problème se développe à vitesse exponentielle. Il s’agit de l’utilisation de peptides de pénétration cellulaire (CPP pour cell penetrating peptide). Ce sont de petits peptides d’une taille variant de 10 à 30 acides aminés, et qui ont une charge nette positive, essentiellement apportée par des résidus lysines et arginines. Ils peuvent être internalisés dans les cellules par un ou plusieurs mécanismes, dont certains ne nécessitent pas d’apport énergétique cellulaire. En règle générale, les CPP n’ont pas de récepteurs cellulaires connus, à l’exception notable de certains d’entre eux issus de protéines fonctionnelles plus larges.
Ce sont Frankel et Pabo qui les premiers en 1988, en étudiant l’activité de la protéine Tat du virus de l’immunodéficience humaine (VIH), se sont aperçus que cette protéine purifiée était capable de pénétrer dans les cellules [1]. Par la suite, Joliot et al. ont montré en 1991 que la protéine Drosophila antennapedia homeodomain pénètre dans les cellules neuronales et qu’elle a la capacité de s’accumuler dans les noyaux cellulaires [2]. À l’issue de ces travaux, le tout premier CPP à être décrit, la pénétratine, encore appelée Antp, d’une longueur de 16 acides aminés, fut dérivé de la troisième hélice de Drosophila antennapedia homeodomain [3]. Cette étude démontrait pour la première fois que les propriétés de pénétration cellulaire d’une protéine sont dues à des séquences minimales au sein de ces protéines également appelées protein transduction domain (PTD). En 1998, Vives et al. [4] ont adopté la même approche d’étude pour les domaines tronqués de la protéine Tat et identifié une séquence minimale de la protéine capable d’entrer dans les cellules. Ce peptide a été appelé Tat également en référence à la protéine et ses utilisations ont connu un succès grandissant. Ces deux peptides, pénétratine et Tat, sont devenus les premiers CPP d’une longue liste de peptides capables de se distribuer au sein des cellules. Parmi ces nouveaux peptides, la maurocalcine est un CPP original [5] car issu du venin d’un scorpion tunisien Scorpio maurus palmatus. Ce peptide de 33 acides aminés fut identifié grâce à son activité pharmacologique en tant qu’activateur du récepteur à la ryanodine (RyR1) des muscles squelettiques. La cible est particulièrement originale puisqu’il s’agit d’un canal calcique intracellulaire impliqué dans le couplage excitation-contraction [6]. Ces observations avaient laissé entrevoir la possibilité que la maurocalcine devait traverser la bicouche lipidique des cellules afin d’exercer sa fonction d’activateur de canal calcique. Cette hypothèse était largement renforcée par le fait que le site d’interaction de la maurocalcine sur RyR1 est localisé dans une zone du cytoplasme [7]. La démonstration que la maurocalcine était effectivement un CPP est venue des observations suivantes : (1) l’application extracellulaire du peptide à des myotubes induit une libération calcique quasi instantanée [8]; et (2) la greffe d’une protéine streptavidine fluorescente sur la maurocalcine biotinylée permet sa translocation intracellulaire [5]. Par ailleurs, la maurocalcine partage en commun avec les autres CPP la propriété d’être un peptide basique dont de nombreux acides aminés sont chargés positivement (11 sur 33). De plus, la plupart des acides aminés basiques sont localisés sur une même face de la molécule en accord avec la distribution asymétrique observée sur des molécules telles que Tat et pénétratine [9].
Le Tableau I recense des exemples de divers peptides de pénétration cellulaire, et la Figure 1 illustre l’origine de quelques-uns d’entre eux. Ces peptides peuvent être a priori séparés en quatre classes distinctes. À la classe des PTD découverts à l’origine (Tat et pénétratine) s’ajoutent donc trois classes supplémentaires : (1) la classe des peptides chimères, comprenant CADY [10], MPG [11], Pep-1 [12] et transportan [13]; (2) la classe des peptides modèles, dont les plus connus sont les peptides polyarginine [14]; et (3) la classe des CPP naturels comme les toxines de venins dont font partie la maurocalcine et la crotamine [15]. Les peptides chimères sont souvent issus d’une protéine plus large (transportan et CADY). Les peptides comme les polyarginines ou MAP (model amphipathic peptide) sont, eux, totalement artificiels et leur conception de novo a été inspirée des propriétés de certains acides aminés (basiques et hydrophobes) nécessaires à la pénétration cellulaire des peptides.
 |
Figure 1. Origine de quelques CPP. Exemple de l’origine de quatre CPP : la maurocalcine, la pénétratine, Tat et la polyarginine. La maurocalcine, la pénétratine et Tat sont dérivés de séquences naturelles, alors que la polyarginine a été produite par conception de novo pour avoir une bonne pénétration cellulaire. |
Exemples de quatre classes de peptides de pénétration cellulaires et exemples de cargos transportés. La liste des cargos utilisés n’est pas exhaustive et est simplement donnée à titre d’illustration. x = 7, 8 ou 9 résidus arginine.
Peptides de pénétration cellulaire et mécanisme d’entrée cellulaire
Le mécanisme d’accumulation des CPP dans le cytoplasme des cellules n’est pas encore clairement identifié. Il semble acquis que deux types d’internalisation cellulaire coexistent mais diffèrent drastiquement en termes d’efficacité d’accumulation cytoplasmique des CPP et donc d’applications possibles : d’une part, la translocation directe au travers de la bicouche lipidique, qui présente l’avantage d’un accès direct et rapide des CPP au cytoplasme des cellules; d’autre part l’endocytose qui, en revanche, présente l’inconvénient d’une accumulation cytoplasmique lente et limitée des CPP (Figure 2). La translocation peut suivre plusieurs schémas, les modèles de Barrel-Stave et Carpet étant les plus connus [16, 17]. Ces deux modèles ont été empruntés à l’étude des interactions des peptides antimicrobiens avec les bicouches lipidiques et la translocation des peptides est basée sur le concept de perturbation locale de la bicouche lipidique par des agrégats peptidiques. Il est utile de mentionner l’existence de trois modèles supplémentaires : (1) le modèle de pore transitoire, dans lequel les CPP intégrés dans la bicouche lipidique génèrent un courant ionique par formation de pore transmembranaire [18]; (2) le modèle de fusion membranaire, dans lequel les CPP, en s’insérant dans le feuillet externe de la bicouche lipidique, promeuvent une fusion locale et transitoire de deux régions membranaires, rapprochant ainsi les surfaces cationiques des CPP du feuillet interne anionique de la membrane et facilitant le transfert intracellulaire du CPP [19]; et (3) un modèle d’électroporation, dans lequel la fixation de CPP cationiques aux lipides anioniques de surface de la membrane plasmique crée un champ électrique transmembranaire. Ceci altère les tensions latérales et de courbure de la membrane et crée les conditions favorables à une électroporation membranaire permettant l’internalisation des peptides par la formation de structures membranaires atypiques et transitoires [20]. Le terme endocytose représente la phagocytose pour les grosses particules et la pinocytose pour les solutés. Quatre types de pinocytose existent : la macropinocytose, l’endocytose dépendante de la cavéoline ou de la clathrine et l’endocytose indépendante de la clathrine et de la cavéoline [21]. Selon le type de CPP et de cargo utilisé, chacun de ces mécanismes d’endocytose a été impliqué dans l’internalisation des CPP. La contribution respective des mécanismes d’entrée des CPP (translocation versus endocytose) varie selon la nature du CPP utilisé, sa concentration ainsi qu’en fonction du cargo transporté.
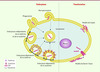 |
Figure 2. Mécanismes d’entrée dans la cellule. Deux modes d’entrée des molécules dans la cellule existent : l’endocytose et la translocation. L’endocytose regroupe la macropinocytose, la phagocytose, l’endocytose dépendante de la clathrine, l’endocytose dépendante de la cavéoline et l’endocytose indépendante de la clathrine et de la cavéoline. La translocation se décline en deux modèles : le modèle de Carpet et le modèle de Barrel-Stave. |
Peptides de pénétration cellulaire et fonction de transport des cargos
L’atout majeur des CPP consiste à pouvoir transporter des cargos qui, sans eux, ne pourraient pas accéder aux compartiments intracellulaires de la cellule (endosomes, noyau et cytoplasme). Les CPP peuvent être couplés à des cargos de natures très diverses. À titre d’exemple, les CPP ont permis avec succès un transport intracellulaire efficace de : peptides, protéines, acides nucléiques (oligonucléotides, ADNc, ARN, siARN, PNA [peptide nucléique acide]), fluorochromes, nanoparticules, agents de contraste pour l’imagerie à résonance magnétique, et drogues [22]. Le couplage des CPP avec les cargos peut se faire de manière covalente ou non afin de permettre une distribution des molécules d’intérêt dans les cellules. La Figure 3 illustre différentes méthodes de couplage de ces peptides aux cargos. Nous illustrons ci-dessous quelques applications à visée thérapeutique ayant un potentiel de développement clinique.
 |
Figure 3. Les différents types de couplage des CPP aux cargos à internaliser. Les cargos peuvent être fixés aux CPP de façon non covalente ou par réaction chimique via un linker, sauf dans le cas du pont disulfure. |
Peptides de pénétration cellulaire : objectifs thérapeutiques
Délivrer des peptides thérapeutiques
Nombreux sont les peptides et protéines exogènes qui possèdent des activités biologiques importantes et qui pourraient être utilisés en thérapeutique humaine pour le traitement de diverses pathologies. Ce qui peut limiter l’utilisation thérapeutique des peptides, ce sont leur faible biodisponibilité en raison des difficultés d’absorption, et les faibles perméabilités au travers de la muqueuse intestinale. Des solutions satisfaisantes ont pu être établies en couplant des peptides bioactifs à des CPP. Ainsi, le groupe de Takayama a établi récemment que le glucagon-like peptide-1 (GLP-1) et l’exendin-4, deux peptides utilisés pour le traitement du diabète de type 2, peuvent être transportés efficacement au travers de la muqueuse nasale s’ils sont couplés à la pénétratine [23]. Cette augmentation du transport favorise très largement la biodisponibilité de ces peptides thérapeutiques.
Délivrer des siARN
Les siARN (short interfering RNA), découverts par Fire et Mello [55], sont des petits ARN double-brin d’environ 19-21 nucléotides qui, après une prise en charge par le système RISC (RNA-inducing silencing complex), et hybridation spécifique à un ARNm cible, induisent une coupure au sein de l’ARNm, rendant celui-ci indisponible pour sa traduction en protéine [24]. Bien que le potentiel thérapeutique des siARN soit immense, leur utilisation en clinique est limitée par leur mauvaise pénétration cellulaire. C’est pourquoi de nombreuses études portent sur le couplage des siARN à des CPP [10, 25–28]. La plupart des stratégies impliquent la formation de liaisons non covalentes entre CPP et siARN, liaisons rendues possibles grâce à la complémentarité de charges électrostatiques entre ces deux ligands (charges positives pour le CPP et charges négatives pour le siARN). Ce couplage s’est avéré approprié dans le cas du CPP MPG pour délivrer des siARN, en raison d’une très bonne affinité avec les acides nucléiques et la formation de complexes stables avec les siARN par liaisons électrostatiques [11, 28]. Ainsi complexés, les siARN ont pu être délivrés dans des cellules en suspension, adhérentes, ou en cultures primaires, ou dans les cellules souches embryonnaires [25]. L’autre alternative à cette méthodologie repose sur un couplage par pont disulfure entre un brin du siARN et le CPP [29]. Des variantes de cette technique sont possibles, elles reposent sur l’utilisation de siARN fluorescents. Cette méthode a été appliquée avec succès in vitro, en utilisant la pénétratine, pour la répression de l’expression de SOD1 (superoxide dismutase) et caspase-3 dans les neurones sympathiques et d’hippocampes [30]. Dans des modèles animaux de cancer établis par xénogreffe avec des cellules de carcinome, le CPP dérivé de la protamine couplé aux siARN adéquats supprime la croissance tumorale en inhibant l’expression du VEGF (vascular endothelial growth factor) [31]. La même stratégie s’avère efficace après injection intratumorale (cellules tumorales PC3 ou SCK3-Her2) de CPP MPG-8 ciblant les ARN de la cycline B1 grâce à un siARN dirigé contre cette cycline [32]. Ces résultats très prometteurs obtenus dans des modèles animaux laissent entrevoir une utilisation possible des CPP couplés aux siARN en clinique.
Délivrer des nanoparticules
Les nanoparticules sont de plus en plus étudiées comme plateformes multimodales, à la fois parce qu’elles permettent de greffer des molécules bioactives et comme outil diagnostique (fluorescence, magnétisme) ou thérapeutique (production d’énergie) [56]. Leur incapacité à traverser les membranes lipidiques des cellules peut limiter cependant grandement leur utilisation in vitro et in vivo. De ce fait, les nanoparticules sont souvent utilisées en complexe avec des CPP afin de contourner cet écueil de pénétration cellulaire. Plusieurs ligands ont pu être fixés sur une même nanoparticule. Ainsi, des nanoparticules de fer superparamagnétiques, conjuguées à Tat, ont ainsi pu être internalisées dans des lymphocytes avec une efficacité 100 fois supérieure à celle des nanoparticules seules. Ce complexe est localisé dans le noyau et le cytoplasme des cellules [33]. Les cellules sont magnétiques et deviennent détectables par IRM. Cette technique permet le suivi cellulaire in vivo par IRM et l’extraction des cellules des organes en raison de leurs propriétés magnétiques. D’autres applications reposent sur l’utilisation de nanocristaux semi-conducteurs luminescents (encore appelés quantum dots), une classe de sondes fluorescentes ayant des propriétés optiques qui les rendent supérieures aux colorants organiques pour les applications biologiques. Selon la nature des nanocristaux ou leurs diamètres, les longueurs d’onde d’émission diffèrent, ce qui permet de créer toute une série de couleurs. Cette propriété a été utilisée avec des quantum dots fonctionnalisés avec la maurocalcine pour marquer avec des codes couleurs différents des monocytes/macrophages et des lymphocytes T [34]. La réinjection in vivo des cellules ainsi marquées dans un modèle d’athérosclérose (souris ApoE−/−) permet de marquer des aires de lésion aortique.
Délivrer des agents antitumoraux
Une des applications prometteuses des CPP semble être la délivrance efficace d’agents antitumoraux in vivo. La doxorubicine est un agent intercalant fréquemment utilisé en chimiothérapie des cancers solides. Après une période d’administration de cet agent, les cellules tumorales développent généralement un mécanisme de résistance à la doxorubicine appelé multidrug resistance (MDR) [35] qui conduit à l’expulsion par les cellules des molécules administrées. Aroui et al. ont démontré en 2009 que l’exposition de cellules chimiorésistantes MDA-MB-231 à un complexe moléculaire formé par une liaison chimique entre un analogue de la maurocalcine (CPP sans activité pharmacologique) et la doxorubicine [36] permettait de contrer ce phénomène de résistance. Il semblerait que le complexe moléculaire soit moins susceptible à l’expulsion cellulaire par le MDR que la doxorubicine. Inversement, si l’on utilise des cellules chimiosensibles MCF-7, l’efficacité de la doxorubine est diminuée par le couplage à la maurocalcine, probablement en raison d’une différence de distribution subcellulaire du complexe (localisation essentiellement cytoplasmique pour la maurocalcine-doxorubicine versus une distribution nucléaire prédominante pour la doxorubicine). Il apparaît que le couplage de la doxorubicine à un CPP favoriserait en réalité plutôt des mécanismes d’apoptose, différant en ce point du mécanisme traditionnel de mort induite par la doxorubicine seule. Ces résultats obtenus avec la maurocalcine ont pu être généralisés à d’autres CPP [37, 38], voire à d’autres agents antitumoraux comme le méthotrexate [39]. D’autres stratégies ont été utilisées avec succès. Citons à titre d’exemple l’encapsulation du paclitaxel, un agent antitumoral inhibiteur de la mitose, au sein de liposomes fonctionnalisés avec des CPP. Ce type de complexe s’est avéré prometteur dans un modèle animal établi par xénogreffe de cellules cancéreuses KB (lignée cellulaire humaine issue d’un carcinome du nasopharynx) [40].
Peptides de pénétration cellulaire et imagerie cellulaire in vivo
Pouvoir visualiser in vivo des molécules, des cellules, des organes ou des tumeurs et coupler à ces agents de détection des fonctions thérapeutiques serait un atout considérable pour la médecine moderne. Les méthodes d’imagerie intracellulaire se sont jusqu’à présent heurtées à un écueil considérable, celui du passage des agents d’imagerie au travers de la membrane plasmique. De nombreuses applications d’imagerie in vivo utilisant les CPP pour ce passage membranaire fleurissent aujourd’hui, que ce soit pour la délivrance de molécules fluorescentes ou d’agents de contraste pour l’imagerie par résonance magnétique [27, 41, 42]. L’Institut de veille sanitaire estime à plus de 347 000 les nouveaux cas de cancer diagnostiqués en 2009 en France. Le principal moyen de traitement des tumeurs solides est la chirurgie. Or, la réussite d’une telle opération dépend de l’aptitude du chirurgien à différencier la tumeur du tissu sain. Le groupe de Tsien de l’Institut médical Howard Hughes de San Diego a développé une méthode qui permet de visualiser la tumeur durant la chirurgie grâce à un CPP couplé à un fluorochrome : la Cy5. Ce peptide de pénétration cellulaire est couplé à un peptide neutralisant la pénétration (peptide chargé négativement) via un agent de liaison (linker) sensible aux protéases. Ce complexe ne pénètre pas efficacement dans les cellules non tumorales, mais le clivage du linker par des protéases spécifiques de la tumeur libère le CPP-Cy5 qui pénètre dans les cellules tumorales, marquant ainsi très efficacement la tumeur in vivo. L’équipe a ainsi pu montrer que quand la chirurgie est effectuée en présence de ce complexe de pénétration cellulaire, il y a dix fois moins de cellules tumorales résiduelles que lors d’une chirurgie classique [43]. Tsien a obtenu le prix Nobel de chimie en 2008 pour l’ensemble de ses travaux sur la conception de molécules fluorescentes et photolabiles [57]. Cette même approche a été généralisée à l’utilisation de nanoparticules de gadolinium, ce qui permet, outre une détection de la fluorescence, une imagerie de la tumeur par IRM [41]. D’autres efforts sont en cours de réalisation pour la détection d’ARNm cellulaires par la délivrance de PNA aux séquences complémentaires à ces ARNm, grâce à des CPP couplés à des agents de contraste IRM, tel le DOTA [44]. Cette stratégie se heurte cependant encore à l’absence de spécificité cellulaire quant à la pénétration des CPP, mais elle présage de manière ambitieuse de l’avenir de l’imagerie moléculaire in vivo.
Les différents exemples d’applications décrits ici prouvent tout le potentiel clinique des CPP et prédisent un brillant avenir à ces peptides pour l’amélioration de l’internalisation de drogues d’intérêt clinique. Cette stratégie d’administration possède plusieurs avantages, comme par exemple une délivrance rapide des cargos dans les cellules, une bonne stabilité et une absence de toxicité avérée [45].
Conflit d’intérêts
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
Références
- Frankel AD, Pabo CO. Cellular uptake of the tat protein from human immunodeficiency virus. Cell 1988 ; 55 : 1189-1193. [CrossRef] [PubMed] [Google Scholar]
- Joliot A, Pernelle C, Deagostini-Bazin H, Prochiantz A. Antennapedia homeobox peptide regulates neural morphogenesis. Proc Natl Acad Sci USA 1991 ; 88 : 1864-1868. [CrossRef] [Google Scholar]
- Derossi D, Joliot AH, Chassaing G, Prochiantz A. The third helix of the antennapedia homeodomain translocates through biological membranes. J Biol Chem 1994 ; 269 : 10444-10450. [PubMed] [Google Scholar]
- Vives E, Brodin P, Lebleu B. A truncated HIV-1 Tat protein basic domain rapidly translocates through the plasma membrane and accumulates in the cell nucleus. J Biol Chem 1997 ; 272 : 16010-16017. [CrossRef] [PubMed] [Google Scholar]
- Esteve E, Mabrouk K, Dupuis A, et al.Transduction of the scorpion toxin maurocalcine into cells. Evidence that the toxin crosses the plasma membrane. J Biol Chem 2005 ; 280 : 12833-12839. [CrossRef] [PubMed] [Google Scholar]
- Fajloun Z, Kharrat R, Chen L, et al.Chemical synthesis and characterization of maurocalcine, a scorpion toxin that activates Ca2+ release channel/ryanodine receptors. FEBS Lett 2000 ; 469 : 179-185. [CrossRef] [PubMed] [Google Scholar]
- Altafaj X, Cheng W, Esteve E, et al. Maurocalcine and domain A of the II-III loop of the dihydropyridine receptor Cav 1.1 subunit share common binding sites on the skeletal ryanodine receptor. J Biol Chem 2005 ; 280 : 4013-4016. [CrossRef] [PubMed] [Google Scholar]
- Esteve E, Smida-Rezgui S, Sarkozi S, et al. Critical amino acid residues determine the binding affinity and the Ca2+ release efficacy of maurocalcine in skeletal muscle cells. J Biol Chem 2003 ; 278 : 37822-37831. [CrossRef] [PubMed] [Google Scholar]
- Ram N, Weiss N, Texier-Nogues I, et al. Design of a disulfide-less, pharmacologically inert, and chemically competent analog of maurocalcine for the efficient transport of impermeant compounds into cells. J Biol Chem 2008 ; 283 : 27048-27056. [CrossRef] [PubMed] [Google Scholar]
- Konate K, Crombez L, Deshayes S, et al. Insight into the cellular uptake mechanism of a secondary amphipathic cell-penetrating peptide for siRNA delivery. Biochemistry 2010 ; 49 : 3393-3402. [CrossRef] [PubMed] [Google Scholar]
- Crombez L, Charnet A, Morris MC, et al. A non-covalent peptide-based strategy for siRNA delivery. Biochem Soc Trans 2007 ; 35 : 44-46. [CrossRef] [PubMed] [Google Scholar]
- Morris MC, Depollier J, Mery J, et al. A peptide carrier for the delivery of biologically active proteins into mammalian cells. Nat Biotechnol 2001 ; 19 : 1173-1176. [CrossRef] [PubMed] [Google Scholar]
- Pooga M, Hallbrink M, Zorko M, Langel U. Cell penetration by transportan. FASEB J 1998 ; 12 : 67-77. [PubMed] [Google Scholar]
- Zhang C, Tang N, Liu X, et al.siRNA-containing liposomes modified with polyarginine effectively silence the targeted gene. J Control Release 2006 ; 112 : 229-239. [CrossRef] [PubMed] [Google Scholar]
- Radis-Baptista G, de la Torre BG, Andreu D. A novel cell-penetrating peptide sequence derived by structural minimization of a snake toxin exhibits preferential nucleolar localization. J Med Chem 2008 ; 51 : 7041-7044. [CrossRef] [PubMed] [Google Scholar]
- Herbig ME, Weller K, Krauss U, et al. Membrane surface-associated helices promote lipid interactions and cellular uptake of human calcitonin-derived cell penetrating peptides. Biophys J 2005 ; 89 : 4056-4066. [CrossRef] [PubMed] [Google Scholar]
- Yeaman MR, Yount NY. Mechanisms of antimicrobial peptide action and resistance. Pharmacol Rev 2003 ; 55 : 27-55. [CrossRef] [PubMed] [Google Scholar]
- Deshayes S, Plenat T, Charnet P, et al. Formation of transmembrane ionic channels of primary amphipathic cell-penetrating peptides. Consequences on the mechanism of cell penetration. Biochim Biophys Acta 2006 ; 1758 : 1846-1851. [CrossRef] [PubMed] [Google Scholar]
- Henriques ST, Castanho MA. Consequences of nonlytic membrane perturbation to the translocation of the cell penetrating peptide pep-1 in lipidic vesicles. Biochemistry 2004 ; 43 : 9716-9724. [CrossRef] [PubMed] [Google Scholar]
- Binder H, Lindblom G. Charge-dependent translocation of the Trojan peptide penetratin across lipid membranes. Biophys J 2003 ; 85 : 982-995. [CrossRef] [PubMed] [Google Scholar]
- Conner SD, Schmid SLRegulated portals of entry into the cell. Nature 2003 ; 422 : 37-44. [CrossRef] [PubMed] [Google Scholar]
- Brasseur R, Divita G. Happy birthday cell penetrating peptides: already 20 years. Biochim Biophys Acta 2010 ; 1798 : 2177-2178. [CrossRef] [PubMed] [Google Scholar]
- Khafagy el S, Morishita M, Kamei N, et al. Efficiency of cell-penetrating peptides on the nasal and intestinal absorption of therapeutic peptides and proteins. Int J Pharm 2009 ; 381 : 49-55. [CrossRef] [PubMed] [Google Scholar]
- Elbashir SM, Harborth J, Lendeckel W, et al. Duplexes of 21-nucleotide RNAs mediate RNA interference in cultured mammalian cells. Nature 2001 ; 411 : 494-498. [CrossRef] [PubMed] [Google Scholar]
- Simeoni F, Morris MC, Heitz F, Divita G. Peptide-based strategy for siRNA delivery into mammalian cells. Methods Mol Biol 2005 ; 309 : 251-260. [PubMed] [Google Scholar]
- Lundberg P, El-Andaloussi S, Sutlu T, et al. Delivery of short interfering RNA using endosomolytic cell-penetrating peptides. FASEB J 2007 ; 21 : 2664-2671. [CrossRef] [PubMed] [Google Scholar]
- Medarova Z, Pham W, Farrar C, et al. In vivo imaging of siRNA delivery and silencing in tumors. Nat Med 2007 ; 13 : 372-377. [CrossRef] [PubMed] [Google Scholar]
- Choi YS, Lee JY, Suh JS, et al. The systemic delivery of siRNAs by a cell penetrating peptide, low molecular weight protamine. Biomaterials 2011(sous presse). [Google Scholar]
- Muratovska A, Eccles MR. Conjugate for efficient delivery of short interfering RNA (siRNA) into mammalian cells. FEBS Lett 2004 ; 558 : 63-68. [CrossRef] [PubMed] [Google Scholar]
- Davidson TJ, Harel S, Arboleda VA, et al.. Highly efficient small interfering RNA delivery to primary mammalian neurons induces MicroRNA-like effects before mRNA degradation. J Neurosci 2004 ; 24 : 10040-10046. [CrossRef] [PubMed] [Google Scholar]
- Choi Y-S, Lee JY, Suh JS, et al. The systemic delivery of siRNAs by a cell penetrating peptide, low molecular weight protamine. Biomaterials 2010 ; 31 : 1429-1443. [CrossRef] [PubMed] [Google Scholar]
- Crombez L, Morris MC, Dufort S, et al. Targeting cyclin B1 through peptide-based delivery of siRNA prevents tumour growth. Nucleic Acids Res 2009 ; 37 : 4559-4569. [CrossRef] [PubMed] [Google Scholar]
- Josephson L, Tung CH, Moore A, Weissleder R. High-efficiency intracellular magnetic labeling with novel superparamagnetic-Tat peptide conjugates. Bioconjug Chem 1999 ; 10 : 186-191. [CrossRef] [PubMed] [Google Scholar]
- Jayagopal A, Su YR, Blakemore JL, et al.Quantum dot mediated imaging of atherosclerosis. Nanotechnology 2009 ; 20 : 165102. [CrossRef] [PubMed] [Google Scholar]
- Sawicka M, Kalinowska M, Skierski J, Lewandowski W. A review of selected anti-tumour therapeutic agents and reasons for multidrug resistance occurrence. J Pharm Pharmacol 2004 ; 56 : 1067-1081. [CrossRef] [PubMed] [Google Scholar]
- Aroui S, Ram N, Appaix F, et al. Maurocalcine as a non toxic drug carrier overcomes doxorubicin resistance in the cancer cell line MDA-MB 231. Pharm Res 2009 ; 26 : 836-845. [CrossRef] [PubMed] [Google Scholar]
- Aroui S. Maurocalcine as a non toxic drug carrier overcomes doxorubicin resistance in the cancer cell line MDA-MB 231. Pharm Res 2009 ; 26 : 836-845. [CrossRef] [PubMed] [Google Scholar]
- Liang JF, Yang VC. Synthesis of doxorubicin-peptide conjugate with multidrug resistant tumor cell killing activity. Bioorg Med Chem Lett 2005 ; 15 : 5071-5075. [CrossRef] [PubMed] [Google Scholar]
- Lindgren M, Rosenthal-Aizman K, Saar K, et al. Overcoming methotrexate resistance in breast cancer tumour cells by the use of a new cell-penetrating peptide. Biochem Pharmacol 2006 ; 71 : 416-425. [CrossRef] [PubMed] [Google Scholar]
- Niu R, Zhao P, Wang Het al.Preparation, characterization, and antitumor activity of paclitaxel-loaded folic acid modified and TAT peptide conjugated PEGylated polymeric liposomes. J Drug Target 2011(sous presse) [Google Scholar]
- Olson ES, Jiang T, Aguilera TA, et al.Activatable cell penetrating peptides linked to nanoparticles as dual probes for in vivo fluorescence and MR imaging of proteases. Proc Natl Acad Sci USA 107 : 4311-4316. [Google Scholar]
- Kersemans V, Kersemans K, Cornelissen B. Cell penetrating peptides for in vivo molecular imaging applications. Curr Pharm Des 2008 ; 14 : 2415-2447. [CrossRef] [PubMed] [Google Scholar]
- Nguyen QT, Olson ES, Aguilera TA, et al. Surgery with molecular fluorescence imaging using activatable cell-penetrating peptides decreases residual cancer and improves survival. Proc Natl Acad Sci USA 107 : 4317-4322. [Google Scholar]
- Su W, Mishra R, Pfeuffer J, et al.Synthesis and cellular uptake of a MR contrast agent coupled to an antisense peptide nucleic acid: cell-penetrating peptide conjugate. Contrast Media Mol Imaging 2007 ; 2 : 42-49. [Google Scholar]
- Heitz F, Morris MC, Divita GTwenty years of cell-penetrating peptides: from molecular mechanisms to therapeutics. Br J Pharmacol 2009 ; 157 : 195-206. [CrossRef] [PubMed] [Google Scholar]
- Johnson JL, Lowell BC, Ryabinina OP, et al.TAT-mediated delivery of a DNA repair enzyme to skin cells rapidly initiates repair of UV-induced DNA damage. J Invest Dermatol 2011 ; 131 : 753-761. [CrossRef] [PubMed] [Google Scholar]
- Perea SE, Reyes O, Puchades Y, et al. Antitumor effect of a novel proapoptotic peptide that impairs the phosphorylation by the protein kinase 2 (casein kinase 2). Cancer Res 2004 ; 64 : 7127-7129. [CrossRef] [PubMed] [Google Scholar]
- Khafagy el S, Morishita M, Takayama KThe role of intermolecular interactions with penetratin and its analogue on the enhancement of absorption of nasal therapeutic peptides. Int J Pharm 2010 ; 388 : 209-212. [CrossRef] [PubMed] [Google Scholar]
- Pooga M, Kut C, Kihlmark M, et al. Cellular translocation of proteins by transportan. FASEB J 2001 ; 15 : 1451-1453. [PubMed] [Google Scholar]
- Chaubey B, Tripathi S, Ganguly S, et al. A PNA-transportan conjugate targeted to the TAR region of the HIV-1 genome exhibits both antiviral and virucidal properties. Virology 2005 ; 331 : 418-428. [CrossRef] [PubMed] [Google Scholar]
- Kim DW, Jeong HJ, Kang HW, et al. Transduced human PEP-1-catalase fusion protein attenuates ischemic neuronal damage. Free Radic Biol Med 2009 ; 47 : 941-952. [CrossRef] [PubMed] [Google Scholar]
- Morris MC, Vidal P, Chaloin L, et al. A new peptide vector for efficient delivery of oligonucleotides into mammalian cells. Nucleic Acids Res 1997 ; 25 : 2730-2736. [CrossRef] [PubMed] [Google Scholar]
- Crombez L, Aldrian-Herrada G, Konate K, et al. A new potent secondary amphipathic cell-penetrating peptide for siRNA delivery into mammalian cells. Mol Ther 2009 ; 17 : 95-103. [CrossRef] [PubMed] [Google Scholar]
- Hallbrink M, Floren A, Elmquist A, et al. Cargo delivery kinetics of cell-penetrating peptides. Biochim Biophys Acta 2001 ; 1515 : 101-109. [CrossRef] [PubMed] [Google Scholar]
- Harel-Bellan A. Prix Nobel de médecine 2006. Andrew Z. Fire et Craig C. Mello : silence, on désactive les gènes. Med Sci (Paris) 2006 ; 22 : 993-994. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Horcajada P, Serre C, Férey G, et al. Des nanovecteurs hybrides pour la restitution retard de médicaments antitumoraux et antiviraux. Med Sci (Paris) 2010 ; 26 : 761-767. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Nicolas MR, Moreau M. Prix Nobel de chimie 2008 (Osumo Shimomura, Martin Chalfie et Roger Y. Tsien). Med Sci (Paris) 2008 ; 24 : 983-984. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des tableaux
Exemples de quatre classes de peptides de pénétration cellulaires et exemples de cargos transportés. La liste des cargos utilisés n’est pas exhaustive et est simplement donnée à titre d’illustration. x = 7, 8 ou 9 résidus arginine.
Liste des figures
 |
Figure 1. Origine de quelques CPP. Exemple de l’origine de quatre CPP : la maurocalcine, la pénétratine, Tat et la polyarginine. La maurocalcine, la pénétratine et Tat sont dérivés de séquences naturelles, alors que la polyarginine a été produite par conception de novo pour avoir une bonne pénétration cellulaire. |
| Dans le texte | |
 |
Figure 2. Mécanismes d’entrée dans la cellule. Deux modes d’entrée des molécules dans la cellule existent : l’endocytose et la translocation. L’endocytose regroupe la macropinocytose, la phagocytose, l’endocytose dépendante de la clathrine, l’endocytose dépendante de la cavéoline et l’endocytose indépendante de la clathrine et de la cavéoline. La translocation se décline en deux modèles : le modèle de Carpet et le modèle de Barrel-Stave. |
| Dans le texte | |
 |
Figure 3. Les différents types de couplage des CPP aux cargos à internaliser. Les cargos peuvent être fixés aux CPP de façon non covalente ou par réaction chimique via un linker, sauf dans le cas du pont disulfure. |
| Dans le texte | |
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.




