| Issue |
Med Sci (Paris)
Volume 27, Number 3, Mars 2011
|
|
|---|---|---|
| Page(s) | 234 - 236 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2011273234 | |
| Published online | 30 mars 2011 | |
Cellules stromales mésenchymateuses
Vecteurs cellulaires de nanoparticules au sein de tumeurs cérébrales
Mesenchymal stromal cells as cellular vehicles for delivery of nanoparticles to brain tumors
1
Inserm U646, Ingénierie de la vectorisation particulaire, Université d’Angers, Institut de recherche et d’innovation scientifique (IRIS)/CHU, 4, rue Larrey, 49100 Angers, France
2
Département de neurochirurgie, Centre hospitalier universitaire d’Angers, 4, rue Larrey, 49100 Angers, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
**
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
***
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Les gliomes malins
Les gliomes malins sont les tumeurs primitives du système nerveux central (SNC) les plus communes. Avec une incidence de 5 nouveaux cas pour 100 000 personnes en France chaque année, elles représentent plus de 60 % des tumeurs primitives du SNC chez l’adulte. La forme la plus commune mais aussi la plus agressive est l’astrocytome de grade IV, aussi appelé glioblastome. Le traitement standard des glioblastomes consiste en une exérèse chirurgicale suivie d’une radiothérapie et d’une chimiothérapie concomitante et adjuvante par Témozolomide. Cependant, le pronostic des patients est particulièrement sombre avec une médiane de survie de 15 mois [1]. Ce sombre pronostic est en partie dû au caractère extrêmement infiltrant du glioblastome. La résection chirurgicale est macroscopiquement complète, mais laisse des cellules tumorales infiltrées dans les parois de la cavité d’exérèse, qui sont souvent à l’origine de la récidive. Il est donc nécessaire de mettre en place de nouveaux outils thérapeutiques capables de cibler spécifiquement les cellules tumorales et les cellules ayant infiltré le parenchyme cérébral sain.
Les cellules stromales mésenchymateuses dans la thérapie du gliome
Depuis une dizaine d’années, il a été montré que des cellules souches, dont les cellules stromales mésenchymateuses (CSM), pouvaient migrer et se distribuer spécifiquement au sein de tumeurs cérébrales [2]. Les CSM constituent, avec les cellules souches hématopoïétiques, les deux principaux types de cellules souches dans la moelle osseuse. les CSM, qui représentent approximativement 0,001-0,01 % du nombre total de cellules de la moelle osseuse, peuvent être isolées par adhérence différentielle au plastique et multipliées en grand nombre in vitro. Ces cellules sont les précurseurs multipotents des cellules osseuses, cartilagineuses, stromales et adipocytaires [9] (→).
(→) Voir l’article de P. Charbord et L. Casteilla, page 261 de ce numéro
Des études récentes indiquent également que les CSM peuvent se différencier en d’autres types cellulaires : myoblastes cardiaques, cellules endothéliales, hépatocytes, neurones et cellules gliales. Outre leur potentiel important pour les techniques thérapeutiques d’ingénierie tissulaire [3, 10] (→), la découverte du tropisme des CSM vers les tumeurs a fait émerger une nouvelle utilisation de ces cellules comme véhicules d’agents thérapeutiques dans les foyers tumoraux [11] (→→).
(→) Voir l’article de C. Vinatier et al., page 289 ce numéro.
(→→) Voir l’article de G. Lazennec, page 285 de ce numéro
Cette migration des CSM vers les cellules tumorales a été montrée aussi bien pour les tumeurs périphériques que pour les tumeurs du système nerveux central. Concernant les tumeurs cérébrales, il a été démontré, à partir de modèles animaux de gliomes, que les CSM étaient capables de se disperser parfaitement dans la tumeur, s’arrêtant à l’interface tissu sain-tumeur, après leur injection soit dans la tumeur, soit à distance de la tumeur dans l’hémisphère controlatéral ou par voie intraveineuse. Pour pouvoir être utilisées en tant que véhicules d’agents thérapeutiques dans le gliome, les CSM ont généralement été modifiées génétiquement par des virus porteurs de gènes toxiques ou de gènes immunostimulateurs, ou chargées avec des virus oncolytiques [4]. Cependant, l’utilisation chez l’homme de ces vecteurs d’origine virale n’est pas sans risque et soulève de nombreux problèmes : risques de toxicité, d’immunogénicité, de mutation et fort coût de production.
Les cellules stromales mésenchymateuses en tant que véhicules cellulaires de nanoparticules au sein des tumeurs cérébrales
Le développement de vecteurs non viraux comme les nanoparticules (NP) représente une autre stratégie pour délivrer des agents thérapeutiques. Les NP, de taille comprise entre 10 et 1 000 nm, sont principalement constituées de lipides ou de polymères et ne sont pas toxiques pour l’organisme. Elles peuvent contenir différents agents thérapeutiques qui sont alors protégés d’une dégradation prématurée et libérés de façon contrôlée et prolongée [5]. Bien que ces NP aient montré leur efficacité dans le traitement des tumeurs cérébrales [6], des stratégies doivent être trouvées pour permettre leur ciblage et leur distribution intratumorale.
Notre équipe a utilisé la capacité de migration des CSM pour véhiculer spécifiquement des NP chargées en agent thérapeutique dans une tumeur cérébrale [7]. Pour faire la preuve de ce concept, un fluorochrome, la 6-coumarine, a été encapsulé dans les NP pour permettre leur suivi. Nous avons ainsi montré que les CSM étaient capables d’incorporer et de conserver au moins sept jours les NP in vitro (Figure 1). Nous avons également observé que cette internalisation ne modifiait pas la viabilité ni les propriétés souches des CSM. Enfin, les CSM chargées en NP migraient et se distribuaient de façon péritumorale après leur injection in vivo dans la masse tumorale d’une souris porteuse d’un gliome (Figure 1).
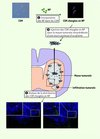 |
Figure 1 Preuve de concept d’un nouvel outil thérapeutique dans les tumeurs cérébrales combinant les CSM et les NP. (1) Internalisation de NP fluorescentes (marquage vert) par les CSM (marquages rouge et bleu) in vitro. (2) Injection des CSM chargées en NP chez une souris porteuse d’un gliome. (3) Migration et distribution des CSM (marquage rouge) et des NP (marquage vert) à la périphérie de la tumeur, à la jonction cerveau normal/masse tumorale 7 jours après l’injection. |
Conclusion
Nous avons ainsi produit un nouvel outil thérapeutique des tumeurs cérébrales en combinant les CSM et les NP. Cet outil permet, via la capacité de migration des CSM, à la fois un ciblage des cellules tumorales et une distribution dans la tumeur. De plus, les NP permettent d’apporter l’agent thérapeutique en grande quantité, de le protéger ainsi que de le libérer de façon contrôlée [8]. Cette stratégie doit maintenant être confirmée en internalisant dans les NP un agent thérapeutique. Plusieurs molécules anticancéreuses peuvent être envisagées. Des résultats prometteurs ont déjà été obtenus au sein du laboratoire avec des NP de ferrociphénol, une molécule toxique pour les cellules tumorales mais pas pour les CSM.
Conflit d’intérêts
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
Remerciements
Nous remercions Dr Claudia Montero-Menei, Pr Paul Schiller, Pr Marie-Claire Venier, Pr Catherine Passirani et Laurence Sindji pour leur contribution à ce travail. Cette étude a été réalisée avec le financement de l’Association « En avant la vie » et de VKF Krebsforschung gGmbH (Berlin, Allemagne).
Références
- StuppR, HegiME, MasonWP, et al. Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial. Lancet Oncol 2009 ; 10 : 459-466. [CrossRef] [PubMed] [Google Scholar]
- KosztowskiT, ZaidiHA, Quinones-HinojosaA. Applications of neural and mesenchymal stem cells in the treatment of gliomas. Expert Rev Anticancer Ther 2009 ; 9 : 597-612. [CrossRef] [PubMed] [Google Scholar]
- DelcroixGJ, CurtisKM, SchillerPC, et al. EGF and bFGF pre-treatment enhances neural specification and the response to neuronal commitment of MIAMI cells. Differentiation 2010 ; 80 : 213-227. [CrossRef] [PubMed] [Google Scholar]
- BexellD, SchedingS, BengzonJ. Toward brain tumor gene therapy using multipotent mesenchymal stromal cell vectors. Mol Ther 2010 ; 18 : 1067-1075. [CrossRef] [PubMed] [Google Scholar]
- HorcajadaP, SerreC, FéreyG, et al. Des nanovecteurs hybrides pour la restitution retard de médicaments antitumoraux et antiviraux. Med Sci (Paris) 2010 ; 26 : 761-767. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- JainKK. Use of nanoparticles for drug delivery in glioblastoma multiforme. Expert Rev Neurother 2007 ; 7 : 363-372. [CrossRef] [PubMed] [Google Scholar]
- RogerM, ClavreulA, Venier-JulienneMC, et al. Mesenchymal stem cells as cellular vehicles for delivery of nanoparticles to brain tumors. Biomaterials 2010 ; 31 : 8393-8401. [CrossRef] [PubMed] [Google Scholar]
- RogerM, ClavreulA, Venier-JulienneMC, et al. The potential of combinations of drug-loaded nanoparticle systems and adult stem cells for glioma therapy. Biomaterials 2011 ; 32 : 2106-2116. [CrossRef] [PubMed] [Google Scholar]
- CharbordP, CasteillaL.. La biologie des cellules souches mésenchymateuses d’origine humaine. Med Sci (Paris) 2011; 27 : 261-268. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- VinatierC, BordenaveL, GuicheuxJ, AmédéeJ. Les cellules souches en ingénierie des tissus ostéoarticulaires et vasculaires. Med Sci (Paris) 2011 ; 27 : 289-296. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- LazennecG. Les cellules souches mésenchymateuses : armes ou dangers pour le traitement des cancers ?Med Sci (Paris) 2011 ; 27 : 285-288. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
© 2011 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1 Preuve de concept d’un nouvel outil thérapeutique dans les tumeurs cérébrales combinant les CSM et les NP. (1) Internalisation de NP fluorescentes (marquage vert) par les CSM (marquages rouge et bleu) in vitro. (2) Injection des CSM chargées en NP chez une souris porteuse d’un gliome. (3) Migration et distribution des CSM (marquage rouge) et des NP (marquage vert) à la périphérie de la tumeur, à la jonction cerveau normal/masse tumorale 7 jours après l’injection. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




