| Issue |
Med Sci (Paris)
Volume 27, Number 1, Janvier 2011
|
|
|---|---|---|
| Page(s) | 14 - 16 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/201127114 | |
| Published online | 10 février 2011 | |
Vers une cartographie des tensions mécaniques intracellulaires ?
Towards mapping mechanical tensions inside cells?
ESPCI ParisTech, CNRS UMR 7083 et MBI, National University of Singapore, 10, rue Vauquelin, 75005 Paris, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Importance des contraintes mécaniques sur le comportement cellulaire
Les stimulus biochimiques étaient considérés jusqu’à la fin des années 1970 comme seuls acteurs de la régulation de l’activité cellulaire, de la morphogenèse ou de la différenciation cellulaire. Il est progressivement apparu que les contraintes mécaniques pouvaient elles aussi jouer un rôle de stimulus externe lors de ces processus [1, 2]. Les cellules sont en effet capables de sonder et de réagir aux sollicitations mécaniques exercées soit par les autres cellules, soit par leur environnement (ex. : matrice extracellulaire). L’intégration de ces stimulus et leur transduction en voies d’activation biochimiques sont actuellement un domaine d’étude en pleine expansion [3, 11, 12] (→).
(→) Voir les Nouvelles de B. Bénazéraf, B. Coste et S.A. Bencherif et al., pages 12, 17 et 19 de ce numéro
Par exemple, certaines voies de régulation peuvent être activées lors de l’ouverture de pores membranaires mécanosensibles consécutive à l’augmentation de la tension de membrane ou bien encore par l’enrichissement local de récepteurs et d’effecteurs au niveau de la déformation du cortex. Enfin l’application de contraintes locales dans le cytoplasme conduisant à la déformation de protéines révélant des sites catalytiques ou de recrutement constitue une autre voie possible de transduction mécanochimique [13]. La capacité d’une cellule à répondre efficacement à une sollicitation mécanique est largement liée à la mise en tension permanente de son cytosquelette via les réseaux dynamiques de filaments interconnectés. L’existence de cette précontrainte permet une transmission physique (donc extrêmement rapide) des sollicitations mécaniques externes qui pourraient potentiellement être intégrées au niveau de la membrane cellulaire ou du nucléosquelette afin d’activer le programme de transcription génétique approprié.
Mesure des forces exercées par les cellules sur leur environnement
La sollicitation mécanique peut être elle-même exercée par la cellule afin de sonder les propriétés microrhéologiques de son environnement. Les cellules souches mésenchymateuses (MSC) peuvent par exemple se différencier en neurones, myoblastes ou ostéoblastes selon la rigidité de leur substrat de culture [4]. La mesure des déformations locales de substrats élastiques a permis d’évaluer à plusieurs dizaines de nN (nanonewtons) les forces exercées sur la matrice extracellulaire par des cellules lors de leur migration [5]. L’existence de points focaux d’adhésion se renforçant au cours du temps ainsi que celle de fibres de stress constituées de filaments d’actine dictant la forme de la cellule a pu être mise en évidence. De la même façon, les forces d’adhésion intercellulaire (relayées par les cadhérines) ont aussi pu être évaluées à une centaine de nN [6]. L’avènement de techniques de microfabrication ou de micropatterning a permis et permettra des mesures beaucoup plus fines et exhaustives des champs de forces externes appliquées par les cellules sur leur environnement.
Tensions internes et renforcement du recrutement
Pour s’exercer, ces contraintes externes doivent être contrebalancées par un champ de contraintes internes supportées, dans le cas de l’adhésion focale, par le complexe d’adhésion (dont les intégrines) et les fibres de stress associées. Ce complexe d’adhésion exerce une contrainte croissante sur la matrice externe ce qui a pour cause et/ou effet d’y favoriser le recrutement constant de protéines (taline, vinculine, actine, etc.) (Figure 1). Une récente étude in vitro [7] a démontré la possibilité d’un mécanisme de régulation du renforcement de ces contraintes par l’ouverture d’un site cryptique de la taline permettant un recrutement accru de vinculine, la protéine servant de lien entre le cytosquelette et le complexe d’adhésion. Ce mécanisme pourrait ainsi servir de transduction de la contrainte en une réponse chimique.
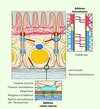 |
Figure 1 Complexes d’adhésion cellulaire. Représentation schématique des complexes d’adhésion intercellulaires CAM (rouge : adherens junctions, bleu : desmosomes) et extracellulaires CMAC (bleu : adhésion focale). Les forces de tension exercées par le complexe d’actomyosine sont représentées en rouge. Adapté avec permission de [3]. |
Un marqueur in vivo de la tension moléculaire
Afin de confirmer in vivo l’existence de tels mécanismes de régulation, une mesure des tensions intracellulaires est nécessaire. Les premières mesures ont récemment été rendu possibles par l’utilisation de marqueurs fluorescents mécanosensibles appliqués à l’α-actinine [8] et au complexe d’actomyosine [9]. Un article récent publié dans Nature [10] présente le plus abouti de ces « dynamomètres moléculaires » appliqués à l’étude de la vinculine. Ce dynamomètre est constitué d’une paire de fluorophores FRET1 (mTFP1 [monomeric teal fluorescent protein 1] et Venus) reliés par une chaîne peptidique dérivée d’une protéine de la soie d’araignée. Cette chaîne non structurée constitue un ressort entropique capable de se déformer sous l’action d’une force de traction de quelques piconewton entraînant une chute du taux de transfert de fluorescence FRET entre les deux fluorophores. En insérant cette construction entre le domaine de la vinculine se liant à l’actine et celui se liant à la taline (Figure 2), le recrutement local et le degré de contrainte exercé sur la vinculine ont pu être déduits de la mesure du taux de transfert FRET à l’échelle d’un complexe d’adhésion unique. Les auteurs ont pu montrer que la vinculine supportait une force de traction dans le complexe d’adhésion plus importante pour les points focaux jeunes que dans les complexes d’adhésion matures en cours de désassemblage. De façon plus surprenante, ce nouveau marqueur moléculaire a permis de montrer que le recrutement et l’activation de la vinculine dépendent, non du niveau de contrainte supporté par la protéine elle-même, mais de la contrainte totale exercée au niveau du complexe d’adhésion. Un mécanisme d’activation et de recrutement lié à la déformation de la protéine (semblable a celui décrit pour la taline) peut donc probablement être exclu.
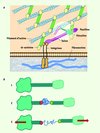 |
Figure 2 Principe du dynamomètre moléculaire. A. Organisation supposée de différentes molécules dans un complexe d’adhésion focale. La vinculine est mise en surbrillance. B. 1. vinculine native; 2. vinculine modifiée avec le dynamomètre moléculaire à faible force. La faible distance entre les fluorophores rouge et vert permet un transfert FRET. 3. Soumis à une force de quelques picoNewton, le dynamomètre moléculaire se déplie, interdisant le transfert de fluorescence (adapté avec permission de [3]). |
Peut-on aller plus loin ?
L’existence de marqueurs moléculaires mécanosensibles ouvre la voie à une possible cartographie dynamique des tensions mécaniques intracellulaires. Le marqueur décrit par l’équipe de M. Schwartz s’applique plus particulièrement aux protéines engagées dans des complexes d’adhésion au niveau des membranes cytoplasmiques ou nucléaires. Pour autant, un principe similaire pourrait permettre de créer des marqueurs s’incorporant dans les filaments d’actine ou les microtubules. La connaissance de la propagation des champs de contrainte externes jusqu’au noyau permettrait par exemple de mieux cerner les procédés d’intégration des signaux mécaniques sur le profil d’expression génétique des cellules.
Conflit d’intérêts
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
FRET : Förster/fluorescence resonance energy transfer.
Références
- Ingber DE, Madri JA, Jamieson JD. Role of basal lamina in neoplastic disorganization of tissue architecture. Proc Natl Acad Sci Biol 1981 ; 78 : 3901-3905. [Google Scholar]
- Farge E. Mechanical induction of twist in the Drosophila foregut/stomodeal primordium. Curr Biol 2003 ; 13 : 1365-1377. [Google Scholar]
- Sheetz M, Gapter L, Hogue CWV(eds). Manual of cellular and molecular function. http://handbook.blueprint.org. [Google Scholar]
- Engler AJ, Sen S, Sweeney HL, Discher DE. Matrix elasticity directs stem cell lineage specification. Cell 2006 ; 126 : 677-689. [CrossRef] [PubMed] [Google Scholar]
- Tan JL, Tien J, Pirone DM, et al. Cells lying on a bed of microneedles : An approach to isolate mechanical force. Proc Natl Acad Sci USA 2003 ; 100 : 1484-1489. [Google Scholar]
- Chu YS, Thomas WA, Eder O, et al. Force measurements in E-cadherin-mediated cell doublets reveal rapid adhesion strengthened by actin cytoskeleton remodeling through Rac and Cdc42. J Cell Biol 2004 ; 167 : 1183-1194. [Google Scholar]
- Del Rio A, Perez-Jimenez R, Liu RC, et al. Stretching single talin rod molecules activates vinculin binding. Science 2009 ; 323 : 638-641. [CrossRef] [PubMed] [Google Scholar]
- Meng F, Suchyna TM, Sachs F. A fluorescence energy transfer-based mechanical stress sensor for specific proteins in situ. FEBS J 2008 ; 275 : 3072-3087. [CrossRef] [PubMed] [Google Scholar]
- Iwai S, Uyeda TQP. Visualizing myosin-actin interaction with a genetically-encoded fluorescent strain sensor. Proc Natl Acad Sci USA 2008 ; 105 : 16882-16887. [CrossRef] [Google Scholar]
- Grashoff C, Hoffman BD, Brenner MD, et al. Measuring mechanical tension across vinculin reveals regulation of focal adhesion dynamics. Nature 2010 ; 466 : 263-266. [CrossRef] [PubMed] [Google Scholar]
- Sidi S, Rosa FM. Mécanotransduction des forces hémodynamiques et organogenèse. Med Sci (Paris) 2004 ; 20 : 557-561. [PubMed] [Google Scholar]
- Albiges-Rizo C, Bouvard D, Bouin AP, et al. La taline : une allure d’haltérophile et la pratique du stretching pour mieux transmettre les forces. Med Sci (Paris) 2009 ; 25 : 909-911. [PubMed] [Google Scholar]
- Desprat N, Farge E. À la recherche des capteurs mécaniques moléculaires de la cellule. Med Sci (Paris) 2007 ; 23 : 583-585. [PubMed] [Google Scholar]
© 2011 médecine/sciences – Inserm / SRMS
Liste des figures
 |
Figure 1 Complexes d’adhésion cellulaire. Représentation schématique des complexes d’adhésion intercellulaires CAM (rouge : adherens junctions, bleu : desmosomes) et extracellulaires CMAC (bleu : adhésion focale). Les forces de tension exercées par le complexe d’actomyosine sont représentées en rouge. Adapté avec permission de [3]. |
| Dans le texte | |
 |
Figure 2 Principe du dynamomètre moléculaire. A. Organisation supposée de différentes molécules dans un complexe d’adhésion focale. La vinculine est mise en surbrillance. B. 1. vinculine native; 2. vinculine modifiée avec le dynamomètre moléculaire à faible force. La faible distance entre les fluorophores rouge et vert permet un transfert FRET. 3. Soumis à une force de quelques picoNewton, le dynamomètre moléculaire se déplie, interdisant le transfert de fluorescence (adapté avec permission de [3]). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




