| Issue |
Med Sci (Paris)
Volume 24, Number 8-9, Août-Septembre 2008
|
|
|---|---|---|
| Page(s) | 673 - 675 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/20082489673 | |
| Published online | 15 août 2008 | |
Tropisme in vivo de l’adénovirus
Rôle inattendu de l’hexon
Adenovirus hexon mediates liver gene transfer
Institut de Génétique Moléculaire de Montpellier (IGMM), CNRS 5535 et Université Montpellier I et II, 1919, route de Mende, 34293 Montpellier, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
L’équipe d’Andrew Baker a montré récemment que la transduction des cellules hépatiques par des adénovirus injectés par voie intraveineuse est due à l’interaction du facteur X de la coagulation avec les trimères d’hexons, composants de la capside [1]. Pourquoi ces observations ont-elles autant d’intérêt ? Pour y répondre, rappelons le principe de Guillaume d’Occam. Le rasoir d’Occam est un principe de raisonnement que l’on attribue au moine franciscain et philosophe Guillaume d’Occam (XIVe siècle). Aussi appelé principe de simplicité, parcimonie ou encore économie. Ce principe est exprimé en latin comme « lex parcimoniae : entia non sunt multiplicanda praeter necessitatem » et souvent paraphrasé comme « si toutes les hypothèses sont possibles, l’explication la plus simple est la meilleure ».
Les adénovirus, agents infectieux et vecteurs de gènes thérapeutiques
Les adénovirus sont des virus non enveloppés à double brin d’ADN dont la structure présente une symétrie icosaédrique. Il en existe plus de 50 sérotypes, tous infectieux pour l’homme. La capside externe virale est constituée majoritairement de trois protéines principales : la fibre, la base du penton et l’hexon (Figure 1). La fibre a une structure homotrimérique qui s’étend en forme de spicule à l’extérieur de la capside. La queue de la fibre est imbriquée dans la base du penton situé sur chaque sommet de l’icosaèdre. L’hexon est la protéine majoritaire avec 240 hexons trimériques qui forment les 20 faces triangulaires. Chez l’homme, les infections à adénovirus causent normalement des symptômes oculaires, du tractus gastro-intestinal et des voies respiratoires. Cependant, chez les patients immunodéprimés et les nouveau-nés, les infections à adénovirus peuvent être graves, voire létales.
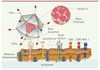 |
Figure 1. Récepteurs jouant un rôle mineur dans la liaison ou l’internalisation. L’adénovirus utilise différents récepteurs tels que CAR, l’acide sialique, le CD86, le CD80, le CMH de classe I ainsi que le récepteur heparan sulfate glycoproteins (HSPG), ce dernier étant le récepteur principal de l’adénovirus après injection par voie intraveineuse en utilisant le facteur X comme pont entre le virus et le récepteur. Les lactoferrines agissent à l’instar du FX pour certains sérotypes sur des tissus spécifiques. |
L’âge d’or des adénovirus date des années 1970, lorsqu’ils ont été utilisés pour comprendre l’épissage de l’ARN et la réplication de l’ADN (ces deux sujets ont été récompensés par un prix Nobel de médecine). Plus récemment, l’engouement pour la thérapie génique a suscité un nouvel intérêt pour les vecteurs adénoviraux. Ces vecteurs sont actuellement les plus utilisés dans les essais cliniques. Les injections de vecteurs adénovirus dans plusieurs modèles animaux ont démontré leur potentiel dans le traitement de maladies hépatiques, musculaires, oculaires, du système nerveux central, de certaines tumeurs ; ils sont également utilisés comme vaccin ainsi que dans la compréhension de diverses questions biologiques [2]. Dans ce contexte, les études des vecteurs adénovirus ont produit des découvertes originales dans divers domaines tels que la virologie, l’immunologie, la biologie structurale et, bien sûr, le transfert de gène.
CAR : le récepteur des adénovirus de type 5
Au début des années 1990, plusieurs laboratoires ont montré qu’une injection par voie intraveineuse de vecteurs adénovirus de type 5 (HAd5) entraînait une excellente transduction des cellules du foie et plus spécifiquement des hépatocytes. Ce fut également le cas de lignées cellulaires dérivées d’hépatocytes. En 1997, Jeff Bergelson, Lennart Philipson et leurs collègues ont identifié le récepteur principal de la plupart des adénovirus, baptisé CAR, le récepteur à coxsackievirus et adénovirus [3, 4]. CAR est exprimé par de nombreux types cellulaires et par les hépatocytes in vivo. Dans le modèle in vitro modélisant l’entrée des HAd5 dans les cellules épithéliales, CAR interagit avec le domaine globulaire terminal de la fibre (appelé tête ou head) [5]. L’ensemble formant une ancre sur la cellule, sans induire l’internalisation du virus. Par la suite, la liaison d’un récepteur auxiliaire (principalement une intégrine) à la base du penton induit l’internalisation. D’autres récepteurs jouant un rôle mineur dans la liaison ou l’internalisation ont également été décrits (Figure 1). Ainsi, si l’on s’appuie sur le principe d’Occam, il paraîtrait normal de déduire que les adénovirus utilisent CAR pour transduire les hépatocytes in vivo.
Oui, mais… CAR n’explique pas tout
L’histoire devient plus complexe quand on sait que lorsque le site de liaison à CAR est muté sur la fibre de HAd5 ce qui, au moins in vitro, empêche la liaison à CAR [6], le vecteur injecté par voie intraveineuse continue à transduire efficacement le foie. Andrew Baker et ses collègues ont tenté de comprendre ce phénomène pendant plusieurs années, et, en combinant de nombreux outils : approche biochimique, génétique, microscopie électronique, utilisation d’inhibiteurs pharmacologiques et de toxines, d’identifier le rôle des composants du sérum dans la transduction du foie par les adénovirus. Travailler avec les adénovirus est un grand plaisir, en raison de leur grande « modularité ». En effet, il est très aisé d’ajouter ou d’éliminer, ou de remplacer, une partie d’un sérotype par un autre sérotype, cette capacité de modulation leur permet d’intervertir soit une partie ou fragment de la fibre, mais également d’échanger les boucles de l’hexon entre différents sérotypes (par exemple voir [7]).
La fibre et le facteur X
Fait intéressant, c’est par une expérience de protéomique effectuée par le groupe d’André Lieber que l’interaction de la fibre avec des protéines du sérum (par exemple C4BP), incluant des facteurs de coagulation (dont le Facteur IX), fut suggérée [8]. Nos connaissances du tropisme de l’adénovirus et de son récepteur suggéraient que la fibre, par son domaine de liaison à CAR, était impliquée. Mais c’était une fausse piste. Des réductions systématiques et finalement une élimination totale de la fibre n’entravaient toujours pas la transduction du foie après injection intraveineuse d’adénovirus. L’équipe d’Andrew Baker a alors testé la liaison des différents facteurs de coagulation avec le virus, et a trouvé que le facteur X1 (FX), qui a une structure similaire à celle du Facteur IX, se liait fortement. De plus, la liaison du FX à HAd5 muté au niveau de la fibre (étude réalisée en utilisant une technique appelée « résonance plasmon de surface » - SPR) reste possible, démontrant ainsi l’intervention d’une autre protéine de capside dans cette liaison. Le FX est bien impliqué, comme le démontre une augmentation de l’infection de différents types cellulaires in vitro par des vecteurs pré incubés avec le FX ou, à l’inverse, une réduction significative du tropisme hépatique du vecteur HAd5 lorsque le sérum est déplété in vivo de FX via l’utilisation de toxines et d’extraits de plantes comme la warfarine2 [9].
Pour éclaircir le mécanisme de la liaison du FX à la capside, Baker et al. sont donc revenus à la technique de SPR (qui suggère l’intervention de l’hexon) puis ont utilisé la cryo-électronmicroscopie. À une résolution de 25 Å, ils ont identifié le domaine de liaison du FX à la capside [1]. En complément, ces chercheurs ont également disséqué le FX afin de déterminer la région d’interaction avec la capside. Le FX présente trois domaines majeurs dont deux, le domaine sérine protéase et le domaine Gla (gamma carboxylated glutamic), ont été impliqués dans cette interaction. La liaison du FX (une molécule de FX par trimère d’hexon - 240 trimères au total) se fait au centre des trimères d’hexon, dans une région composée des boucles hypervariables entre les différents sérotypes. Cette variation dans la boucle d’hexon a mené cette équipe à étudier la liaison du FX aux autres sérotypes. Ils ont alors tiré parti de cette facilité de moduler les boucles des sérotypes d’adénovirus en utilisant différentes boucles de différents sérotypes dans leur vecteur modèle et trouvèrent que seule une, (D), parmi six espèces (A-F) d’adénovirus humains, n’interagissait pas avec le FX.
Conclusion
Ces résultats nous permettront maintenant de modifier plus intelligemment le tropisme in vivo des vecteurs adénoviraux et, à terme, de cibler d’autres organes ou cellules. Que faire à partir de maintenant ? Ces études ont été menées chez le rongeur et de ce fait, l’éternelle problématique de la comparaison souris versus homme persiste. Le rôle du FX est-il identique chez le primate ? Comment devons-nous utiliser ces données pour améliorer les vecteurs de thérapie génique ? Clairement le laboratoire de Baker doit travailler à identifier les acides aminés essentiels de la région hyper variable et essayer de les modifier pour prévenir la liaison du FX dans le but d’éviter la capture rapide par le foie et ainsi pouvoir cibler d’autres organes. Finalement, une chose est sûre, Guillaume d’Occam n’a jamais vraiment travaillé sur le tropisme in vivo de l’adénovirus.
Le facteur X, également connu sous le nom de facteur Stuart, est une sérine endopeptidase de la cascade de coagulation. Il est synthétisé par le foie en présence de vitamine K et est activé par le facteur IV et le facteur VII.
La warfarine est un dérivé synthétique de la coumarine, une substance naturellement présente chez de nombreuses plantes. La warfarine diminue la coagulation du sang en inhibant la vitamine K époxyde réductase, une enzyme qui recycle la vitamine K oxydée en sa forme réduite après qu’elle a participé à la carboxylation de plusieurs protéines de coagulation du sang. La warfarine est efficace dans la prévention de la thrombose et d’embolie.
Références
- Waddington SN, McVey JH, Bhella D, et al. Adenovirus serotype 5 hexon mediates liver gene transfer. Cell 2008; 132 : 397–409. [Google Scholar]
- Keriel A, Billet O, Kremer EJ. L’adénovirus canin : meilleur ami de l’homme ? Med Sci (Paris) 2003; 19 : 1048–9. [Google Scholar]
- Bergelson JM, Cunningham JA, Droguett G, et al. Isolation of a common receptor for Coxsackie B viruses and adenoviruses 2 and 5. Science 1997; 275 : 1320–3. [Google Scholar]
- Tomko R, Xu R, Philipson L. HCAR and MCAR: the human and mouse cellular receptors for subgroup C adenoviruses and group B cocksakieviruses. Proc Natl Acad Sci USA 1997; 94 : 3352–6. [Google Scholar]
- Wu E, Nemerow GR. Virus yoga: the role of flexibility in virus host cell recognition. Trends Microbiol 2004; 12 : 162–9. [Google Scholar]
- Baker AH, McVey JH, Waddington SN, et al. The Influence of blood on in vivo adenovirus bio-distribution and transduction. Mol Ther 2007; 15 : 1410–6. [Google Scholar]
- Hong SS, Magnusson MK, Henning P, et al. Adenovirus stripping: a versatile method to generate adenovirus vectors with new cell target specificity. Mol Ther 2003; 7 : 692–9. [Google Scholar]
- Shayakhmetov DM, Gaggar A, Ni S, et al. Adenovirus binding to blood factors results in liver cell infection and hepatotoxicity. J Virol 2005; 79 : 7478–91. [Google Scholar]
- Le Bonniec B. La cible de la warfarine identifiée. Med Sci (Paris) 2004; 20 : 512–4. [Google Scholar]
© 2008 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Récepteurs jouant un rôle mineur dans la liaison ou l’internalisation. L’adénovirus utilise différents récepteurs tels que CAR, l’acide sialique, le CD86, le CD80, le CMH de classe I ainsi que le récepteur heparan sulfate glycoproteins (HSPG), ce dernier étant le récepteur principal de l’adénovirus après injection par voie intraveineuse en utilisant le facteur X comme pont entre le virus et le récepteur. Les lactoferrines agissent à l’instar du FX pour certains sérotypes sur des tissus spécifiques. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




