| Issue |
Med Sci (Paris)
Volume 24, Number 6-7, Juin-Juillet 2008
|
|
|---|---|---|
| Page(s) | 581 - 583 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/20082467581 | |
| Published online | 15 juin 2008 | |
Des vésicules sécrétées in vivo permettent d’améliorer la réponse immune anti-tumorale
In vivo secreted vesicles allow improvement of anti-tumor immune response
1
Inserm U653, Institut Curie, Section Recherche, 26, rue d’Ulm, 75005 Paris, France
2
Department of Tumor Immunology, NCMLS 278, Radboud University Nijmegen Medical Center, Nijmegen, Pays-Bas
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Le complexe CMH-peptide d’antigène tumoral
Certaines cellules cancéreuses expriment des antigènes tumoraux qui peuvent être reconnus, sous forme de peptides associés aux molécules du complexe majeur d’histocompatibilité (CMH), par des lymphocytes T spécifiques de la tumeur [1]. Cependant, cette reconnaissance ne conduit pas, généralement, à la destruction de la tumeur [2, 3]. Les lymphocytes T naïfs ne reconnaissent pas directement ces complexes CMH-peptide à la surface des tumeurs : ils doivent d’abord être en contact avec une cellule présentatrice d’antigènes professionnelle, la cellule dendritique, portant le complexe CMH-peptide tumoral spécifique (Figure 1). La cellule dendritique n’exprimant pas elle-même l’antigène tumoral, elle doit le capturer à partir des cellules tumorales, pour générer le complexe CMH-peptide. La façon dont les cellules dendritiques capturent les antigènes à partir des tumeurs n’est pas bien comprise [3]. In vitro, diverses études ont montré que des cellules tumorales mortes [4], des protéines de choc thermique isolées à partir de tumeurs [5], des protéines solubles [6], mais aussi des vésicules membranaires appelées « exosomes » sécrétées par les cellules [7, 8], pouvaient être utilisées par les cellules dendritiques comme sources d’antigènes tumoraux. In vivo, dans l’organisme où les cellules cancéreuses se multiplient, les produits sécrétés par les cellules cancéreuses, antigènes solubles ou vésicules membranaires, pourraient donc aussi être capturés par les cellules dendritiques et utilisés pour former les complexes CMH-peptide tumoral et activer les lymphocytes T. Nous avons voulu tester cette hypothèse, et déterminer si la forme de l’antigène tumoral sécrété (soluble ou associé aux membranes) pouvait moduler la nature ou l’efficacité de la réponse immunitaire induite contre la tumeur [9].
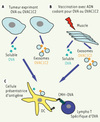 |
Figure 1. Modèle expérimental. L’antigène modèle OVA est sécrété in vivo soit par des cellules tumorales génétiquement modifiées (A), soit par les cellules musculaires après vaccination avec de l’ADN nu (B). L’OVA est normalement sécrétée sous forme soluble (OVA), mais après fusion avec le domaine C1C2 de la lactadhérine, elle est sécrétée associée à des vésicules membranaires, telles que les exosomes (OVAC1C2). Dans les deux cas, l’OVA sécrétée doit être capturée par des cellules présentatrices d’antigènes, qui vont façonner des complexes CMH-peptide (C). Ces complexes seront présentés aux lymphocytes T qui seront alors activés et déclencheront la réponse immunitaire spécifique de l’OVA. |
Efficacité accrue de la réponse T induite par un antigène tumoral porté par des exosomes
Pour cela, nous avons modifié génétiquement une lignée de cellules tumorales de souris, afin qu’elle sécrète un antigène modèle, l’albumine de poulet (ou ovalbumine, OVA), soit sous forme soluble, soit sous une forme associée spécifiquement aux vésicules membranaires de type exosomes (Figure 1A). Pour obtenir une ovalbumine associée aux exosomes, nous l’avons couplée à une séquence protéique dite C1C2, provenant de la lactadhérine, une protéine sécrétée en association avec des vésicules membranaires [10–12]. La séquence C1C2 de la lactadhérine est similaire à des séquences protéiques trouvées dans les facteurs de coagulation sanguine V et VIII, et elle est responsable de l’association aux vésicules membranaires [13]. Nous avons vérifié que, in vitro, les cellules tumorales exprimant l’OVA sécrètent cette protéine en abondance sous forme soluble dans le milieu extracellulaire, alors que les cellules exprimant la protéine de fusion OVAC1C2 sécrètent cette protéine spécifiquement associée à des nanovésicules purifiables par ultracentrifugation, les exosomes.
Nous avons ensuite analysé le comportement des deux types de cellules tumorales in vivo, après leur greffe sous-cutanée dans des souris. Nous avons observé que, dans des souris ayant un système immunitaire fonctionnel, la croissance de la lignée tumorale exprimant OVAC1C2 était plus lente que celle de la lignée exprimant OVA (Figure 2A). Ce retard de croissance est dû à l’activation du système immunitaire, puisque, dans des souris mutantes dépourvues de lymphocytes T et B, la lignée tumorale OVAC1C2 prolifère plus rapidement que la lignée OVA (Figure 2B). Pour augmenter l’efficacité de la réponse immune, nous avons injecté aux souris des lymphocytes T cytotoxiques CD8+ spécifiques d’un complexe CMH-peptide de l’OVA. Nous avons pu montrer que ces lymphocytes T étaient activés de façon plus efficace dans les souris greffées avec les cellules exprimant la protéine de fusion OVAC1C2 portée par les exosomes, et que cette activation des lymphocytes T cytotoxiques permettait la destruction de la tumeur OVAC1C2, alors que la lignée exprimant OVA continuait de croître malgré l’injection des lymphocytes T (Figure 2C). Enfin, si les deux types de lignées sont greffés dans la même souris, les lymphocytes T spécifiques de l’OVA deviennent capables de détruire également la tumeur sécrétant l’OVA soluble. La différence de réponse des deux tumeurs à la présence des lymphocytes spécifiques de l’OVA n’est donc pas due à une différence de sensibilité des tumeurs à leur action destructrice, mais bien à une différence d’efficacité de la réaction initiale d’activation de ces lymphocytes T : l’OVAC1C2 active mieux les lymphocytes T et les rend efficaces pour détruire une tumeur exprimant l’OVA.
 |
Figure 2. Effet de l’expression in vivo de l’OVA soluble ou couplée aux exosomes sur la croissance des tumeurs. A-C. Croissance des tumeurs exprimant l’OVA soluble (OVA), l’OVA associée aux exosomes (OVAC1C2) ou pas d’OVA (Mock) dans des souris hôtes immunocompétentes (A), déficientes en lymphocytes (B), ou immunocompétentes après transfert de lymphocytes T spécifiques de l’OVA (OT-I) (C). D. Survie des souris après greffe de la tumeur exprimant l’OVA soluble dans des souris préalablement vaccinées avec l’ADN codant pour l’OVA soluble (OVA), l’OVA associée aux exosomes (OVAC1C2) ou pas d’OVA (Mock). |
Dans une dernière série d’expériences, nous avons voulu induire l’expression des deux antigènes OVA in vivo par une autre méthode, n’impliquant aucune étape de culture de cellules in vitro : la vaccination avec de l’ADN plasmidique. Quand de l’ADN est injecté dans un tissu (ici le muscle), les cellules au niveau du site d’injection captent l’ADN qui peut alors s’exprimer dans ces cellules. Ainsi, les ADN codant pour les constructions OVA ou OVAC1C2 seront exprimés par les cellules du muscle, qui sécrèteront alors de l’OVA sous forme soit soluble, soit associée aux exosomes (Figure 1B). L’antigène sécrété pourra alors être capturé par des cellules présentatrices d’antigènes puis présenté aux lymphocytes T, et donc déclencher une réponse immunitaire spécifique. Nous avons pu montrer que des souris vaccinées avec l’ADN codant pour OVAC1C2 devenaient résistantes à la croissance d’une tumeur exprimant OVA, et ce de façon plus efficace que des souris vaccinées avec l’ADN codant pour OVA (Figure 2D).
Une nouvelle stratégie d’immunothérapie anticancéreuse
L’ensemble de ces résultats montrent que la sécrétion de l’antigène OVA in vivo sous forme associée à des vésicules membranaires sécrétées, comme les exosomes, permet l’induction de réponses immunitaires T spécifiques de l’OVA efficaces, capables de conduire à la destruction des tumeurs (Figure 1). Nos observations fournissent une des premières preuves expérimentales qu’une sécrétion physiologique in vivo de vésicules membranaires joue un rôle dans les réponses immunitaires. De plus, elles permettent d’envisager une nouvelle stratégie d’immunothérapie contre les tumeurs [14] utilisant la vaccination avec l’ADN plasmidique codant pour un antigène tumoral fusionné au domaine C1C2.
Références
- Van Endert P. Apprêtement des antigènes présentés par les molécules de classe I du CMH. Med Sci (Paris) 2006; 22 : 727–32. [Google Scholar]
- Ochsenbein AF. Principles of tumor immunosurveillance and implications for immunotherapy. Cancer Gene Ther 2002; 9 : 1043–55. [Google Scholar]
- Pardoll D. Does the immune system see tumors as foreign or self ? Annu Rev Immunol 2003; 21 : 807–39. [Google Scholar]
- Albert ML, Pearce SF, Francisco LM, et al. Immature dendritic cells phagocytose apoptotic cells via alphavbeta5 and CD36, and cross-present antigens to cytotoxic T lymphocytes. J Exp Med 1998; 188 : 1359–68. [Google Scholar]
- Basu S, Binder RJ, Ramalingam T, Srivastava PK. CD91 is a common receptor for heat shock proteins gp96, hsp90, hsp70, and calreticulin. Immunity 2001; 14 : 303–13. [Google Scholar]
- Norbury CC, Basta S, Donohue KB, et al. CD8+ T cell cross-priming via transfer of proteasome substrates. Science 2004; 304 : 1318–21. [Google Scholar]
- Wolfers J, Lozier A, Raposo G, et al. Tumor-derived exosomes are a source of shared tumor rejection antigens for CTL cross-priming. Nat Med 2001; 7 : 297–303. [Google Scholar]
- Blanc L, Vidal M. Le signal eat-me des exosomes de réticulocytes. Med Sci (Paris) 2008; 24 : 462–3. [Google Scholar]
- Zeelenberg IS, Ostrowski M, Krumeich S, et al. Targeting tumor antigens to secreted membrane vesicles in vivo induces efficient anti-tumor immune responses. Cancer Res 2008; 68 : 1228–35. [Google Scholar]
- Oshima K, Aoki N, Kato T, et al. Secretion of a peripheral membrane protein, MFG-E8, as a complex with membrane vesicles. Eur J Biochem 2002; 269 : 1209–18. [Google Scholar]
- Veron P, Segura E, Sugano G, Amigorena S, Thery C. Accumulation of MFG-E8/lactadherin on exosomes from immature dendritic cells. Blood Cells Mol Dis 2005; 35 : 81–8. [Google Scholar]
- Silvestre JS, Théry C, Lévy B, et al La lactadhérine, nouvel acteur de l’angiogenèse. Med Sci (Paris) 2005; 21 : 683–5. [Google Scholar]
- Delcayre A, Estelles A, Sperinde J, et al. Exosome display technology : applications to the development of new diagnostics and therapeutics. Blood Cells Mol Dis 2005; 35 : 158–68. [Google Scholar]
- Chouaib S, El Hage F, Benlalam H, Mami-Chouaib F. Immunothérapie du cancer : espoirs et réalités. Med Sci (Paris) 2006; 22 : 755–9. [Google Scholar]
© 2008 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Modèle expérimental. L’antigène modèle OVA est sécrété in vivo soit par des cellules tumorales génétiquement modifiées (A), soit par les cellules musculaires après vaccination avec de l’ADN nu (B). L’OVA est normalement sécrétée sous forme soluble (OVA), mais après fusion avec le domaine C1C2 de la lactadhérine, elle est sécrétée associée à des vésicules membranaires, telles que les exosomes (OVAC1C2). Dans les deux cas, l’OVA sécrétée doit être capturée par des cellules présentatrices d’antigènes, qui vont façonner des complexes CMH-peptide (C). Ces complexes seront présentés aux lymphocytes T qui seront alors activés et déclencheront la réponse immunitaire spécifique de l’OVA. |
| Dans le texte | |
 |
Figure 2. Effet de l’expression in vivo de l’OVA soluble ou couplée aux exosomes sur la croissance des tumeurs. A-C. Croissance des tumeurs exprimant l’OVA soluble (OVA), l’OVA associée aux exosomes (OVAC1C2) ou pas d’OVA (Mock) dans des souris hôtes immunocompétentes (A), déficientes en lymphocytes (B), ou immunocompétentes après transfert de lymphocytes T spécifiques de l’OVA (OT-I) (C). D. Survie des souris après greffe de la tumeur exprimant l’OVA soluble dans des souris préalablement vaccinées avec l’ADN codant pour l’OVA soluble (OVA), l’OVA associée aux exosomes (OVAC1C2) ou pas d’OVA (Mock). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




