| Issue |
Med Sci (Paris)
Volume 23, Number 2, Février 2007
|
|
|---|---|---|
| Page(s) | 173 - 179 | |
| Section | M/S revues | |
| DOI | https://doi.org/10.1051/medsci/2007232173 | |
| Published online | 15 février 2007 | |
Les chimiokines : un réseau sophistiqué de guidage cellulaire
Complexity of the chemokine network
Laboratoire d’immunologie cellulaire, Inserm U543, Université Pierre-et-Marie Curie, Faculté de Médecine Pitié-Salpêtrière, 91 boulevard de l’Hôpital, 75634 Paris Cedex 13, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
L’efficacité du système immunitaire dépend de la mobilité des différents types cellulaires qui le composent et ne cessent de circuler entre le sang, les tissus périphériques et les organes lymphoïdes. Au cours de leur développement ou de leur activation, les capacités migratoires de ces cellules évoluent afin de leur permettre de quitter les organes où elles ont été produites, comme le thymus ou la moelle osseuse, de se positionner dans des sites stratégiques ou encore d’interagir avec d’autres partenaires cellulaires pour éliminer les agents pathogènes. Cette circulation permanente est très organisée et met en jeu de nombreuses protéines, notamment des molécules d’adhérence, des protéases et des facteurs chimiotactiques. Parmi ces derniers, les chimiokines, ou cytokines chimio-attractantes, forment une famille que l’on commence à bien connaître. Nous résumons ici leurs propriétés récemment découvertes, en insistant sur leurs implications physiopathologiques. Nous décrivons ensuite leurs éventuelles utilisations thérapeutiques.
Abstract
The immune system relies on the motility on various cell types that roam the host through the blood, the peripheral tissues and the lymphoid organs, looking for pathogens. Along their maturation and/or activation, the cell migratory capacities change in order to allow them to leave organs where they have been produced such as thymus and bone marrow, to locate in strategic sites to sense surrounding microbes, to meet and interact with other cells, and finally to access peripheral tissues and organs to eradicate the pathogens. This cell traffic is a highly organized process that involves numerous protein families such as adhesion molecules, proteases and chemotactic factors. Among the latter, chemokines are in the front line. We will here summarize the recent findings stressing out their physiopathological relevance and will describe thereafter their possible therapeutic use.
© 2007 médecine/sciences - Inserm / SRMS
Réseau fonctionnel des chimiokines et de leurs récepteurs
Les cytokines chimio-attractantes, ou chimiokines (Ch), sont des polypeptides de 70 à 100 acides aminés, avec des séquences similaires et une structure commune maintenue par deux ponts disulfures conservés [1]. Le nombre et l’espacement des deux premiers résidus cystéine permettent de distinguer quatre sous-familles, dénommées CXC, CC, CX3C et XC (Figure 1). Avec d’autres facteurs chimiotactiques souvent d’origine lipidique, comme le leucotriène BLT1 ou le sphingosine-1-phosphate [2], les Ch forment un ensemble complexe de molécules qui guident et orientent les cellules du système immunitaire.
 |
Figure 1. Les quatre familles de chimiokines, leurs récepteurs et leurs implications dans diverses pathologies. |
Les récepteurs cellulaires des Ch (Rch) sont tous des récepteurs couplés aux protéines G (RCPG), porteurs, donc, de 7 hélices transmembranaires. Ils sont nommés en fonction de la sous-famille de Ch qu’ils reconnaissent (Figure 1). La plupart des Rch reconnaissent plusieurs Ch : cette « polygamie » est la règle, seuls quelques couples « Ch-Rch » y échappant. Cette redondance fonctionnelle constitue le premier niveau de complexité du réseau formé par les Ch et leurs récepteurs, tout à fait comparable ici au réseau des cytokines (Figure 1). La propriété d’un récepteur d’être sensible à plusieurs Ch permet une certaine robustesse du système, puisqu’une même fonction pourrait être prise en charge par plusieurs molécules simultanément [3]. Cela constitue d’ailleurs une difficulté bien connue du physiologiste, qui doit renoncer à la vision simple « un gène → une fonction » abordable par l’inactivation successive des gènes candidats [4].
Circulation des leucocytes et adhérence en 4 étapes : le paradigme
La fonction première des Ch, le chimiotactisme, prend place dans le processus plus large du recrutement des leucocytes depuis le flux circulant jusqu’à leur site d’action, notamment inflammatoire (Figure 2). Il est admis depuis plus de 10 ans que ce processus comporte quatre étapes successives, chacune conditionnant la suivante : l’interaction de faible affinité entre les sélectines leucocytaires ou endothéliales et leurs ligands ralentit la vitesse du leucocyte dans le flux sanguin en permettant son « roulement » ; ce processus est suivi de l’activation des intégrines par divers stimulus provoquant l’arrêt complet du leucocyte et son adhérence forte à l’endothélium ; une perméabilité transitoire (par passage intercellulaire ou pénétration transcellulaire) permet ensuite la diapédèse endothéliale ; enfin, le gradient interstitiel des facteurs chimiotactiques inflammatoires et la protéolyse ciblée par les métalloprotéinases permettent la migration cellulaire par mouvement amiboïde jusqu’au site inflammatoire. Dans ce processus fondamental, les Ch interviennent dans au moins deux des quatre étapes. Avec les intégrines, elles constituent donc des cibles pharmacologiques de choix pour le contrôle thérapeutique de nombreuses situations d’inflammation pathologique. L’utilisation pharmacologique des Ch est déjà bien avancée [5], mais il est clair qu’elle requiert une meilleure connaissance de la complexité du réseau que constituent les Ch et leurs Rch, dans lequel on peut distinguer plusieurs niveaux [6], successivement présentés ci-dessous.
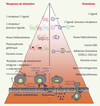 |
Figure 2. Pyramide de complexité des chimiokines et de leurs récepteurs. |
Dimérisation moléculaire
Les Rch, comme beaucoup de RCPG, sont des molécules dimériques [7]. Il existe donc des Rch homo- et hétérodimères. Parmi les nombreuses questions que cette découverte a soulevé [8], celle de savoir si la liaison de la Ch peut induire la dimérisation de son récepteur semble réglée : l’homodimérisation des Rch est constitutive et serait nécessaire à leur expression à la membrane plasmique. L’existence d’hétérodimères constitue un niveau combinatoire supplémentaire (Figure 2) : un hétérodimère de RCPG peut en effet avoir des propriétés différentes de celles de chacun des monomères constituants, comme cela a été bien prouvé pour les récepteurs des opiacés [9]. En ce qui concerne les Rch, l’existence d’hétérodimères CXCR4/CCR2 [10] et CCR5/CCR2b [11] a été clairement montrée grâce aux techniques de transfert de fluorescence (FRET/BRET, fluorescence/bioluminescence resonance energy transfer). Dans le cas du dimère CCR5/CCR2b, la liaison du CCL4 inhiberait la liaison du CCL2 à CCR2b. Il y a donc une coopérativité négative pour la liaison des deux ligands sur l’hétérodimère [11]. Une telle propriété permettrait à la cellule porteuse des deux Rch de mieux distinguer entre les deux ligands correspondants et de mieux « décider » quelle Ch « suivre ». Par ailleurs, des hétérodimères entre Rch et récepteurs d’opioïdes [12] ont été observés, suggérant l’existence d’une interaction entre le réseau des Ch et celui des opiacés.
Liaison aux GAG
Par leur charge globalement basique, les Ch se lient à certains composants glycosylés des surfaces endothéliales et des matrices extracellulaires, les sucres sulfatés des glycosaminoglycanes (GAG). Cette fixation de faible affinité permet très probablement la stabilité du gradient chimiotactique, même soumis au flux sanguin. Pour autant, toutes les Ch ne se fixent pas aux mêmes résidus glycosylés, et pas de la même façon [13], ce qui constitue un niveau supplémentaire de combinatoire possible. De plus, cette liaison permet l’oligomérisation des Ch, sans laquelle leur fonction in vivo est abolie [14], sans que l’on sache s’il y a un lien nécessaire entre la dimérisation des Ch et celle de leur Rch.
Multiplication des Ch par protéolyse
Les Ch subissent d’autres modifications post-traductionnelles, comme le clivage par protéolyse. Ce type de modification peut les inactiver ou modifier leurs spécificités vis-à-vis de leurs récepteurs. Ainsi, le clivage de CCL5 par le CD26 donne lieu à une Ch inactive, réduite de ses deux premiers résidus, tandis que la Ch CCL8 privée de ses quatre premiers résidus après action de MMP-8 (matrix metalloproteinase 8) non seulement n’est plus agoniste, mais devient un antagoniste de CCR2 [15].
La multiplicité des signaux intracellulaires déclenchés par les Ch
Comme tous les ligands de RCPG, les Ch déclenchent en aval de leurs récepteurs des signaux variés aboutissant à différentes fonctions cellulaires, dont la principale est bien sûr la fonction chimiotactique et les fonctions associées d’activation des intégrines et de diapédèse. Ces trois fonctions mettent en jeu la protéine G hétérotrimérique Gi, les protéines G monomériques RhoA et Rap1, telle ou telle isoforme de la PI3K (phosphoinositide-3 kinase), des MAPK (mitogen-activated protein kinase) comme p38 et p42/44 et des protéines liant le cytosquelette comme les FAK (focal adhesion kinase) [16]. Mais, au-delà de ces quelques repères généraux, il est clair qu’il n’y a pas de transduction cellulaire spécifique pour une Ch : non seulement la nature du signal intracellulaire dépend du type cellulaire considéré, mais la plupart des Ch sont capables de déclencher plusieurs voies de transduction parallèles [16]. Ainsi, la diversité du réseau extracellulaire des Ch se double d’une complexité intracellulaire (Figure 2). Notons en particulier que plusieurs Ch sont capables de déclencher des signaux ne passant pas par une protéine G, et éventuellement même des signaux induits directement par la liaison Ch-GAG, et donc ne passant pas par un RCPG [17]. En outre, il est probable que les stimulations extracellulaires simultanées par plusieurs Ch donnent lieu à des interactions entre voies d’activation intracellulaires, ce qui constitue un niveau supplémentaire de complexité.
Polymorphisme génétique
Globalement les Ch et les Rch, à l’instar des RCPG, ne sont pas le siège d’une intense variation génétique, ce qui rend d’autant plus intéressante l’étude des quelques polymorphismes existants. La découverte d’individus dont le gène CCR5 est invalidé (CCR5-Δ32) a permis la confirmation du rôle de ce récepteur dans la pénétration cellulaire du VIH. D’autres variations ponctuelles dans les régions codantes des Rch comme CX3CR1-V249I et T280M, CCR2-V64I et dans les régions régulatrices des gènes des Ch comme CCL2-2518 et CCL5-28 et CCL5-413 ont été décrites et associées à différentes conditions cliniques pathologiques. Cependant, ces associations sont à prendre avec beaucoup de précautions, car leur amplitude et leur pertinence dépendent fortement du recrutement des cohortes concernées et de symptômes observés. Ainsi, les variants CX3CR1-V249I et T280M qui sont associés à une réduction du risque d’accidents cardiovasculaires [18] sont également associés à une augmentation du risque des accidents cérébrovasculaires [19].
Expression différentielle des récepteurs
La combinatoire moléculaire des Ch est naturellement doublée d’une régulation fine de leur expression au cours de la lymphopoïèse et de la différenciation lymphocytaire. Le couple CXCR4/CXCL12 a ainsi un rôle central dans la migration des cellules hématopoïétiques depuis la moelle osseuse jusqu’au sang, tandis que le couple CCR9/CCL25 contribue à la migration des prothymocytes vers le thymus [20]. Par ailleurs, CCR7 et CXCR5 coopèrent dans le développement et l’architecture des organes lymphoïdes secondaires : ils permettent en particulier de cibler les lymphocytes dans ces structures, grâce à l’expression constitutive des chimiokines homéostatiques correspondantes, CCL19 et CCL21 - ligands de CCR7 - dans la zone T, et CXCL13 - ligand de CXCR5 - dans les follicules [21]. En outre, CCR7 est un marqueur des lymphocytes T naïfs et permet de différencier les lymphocytes T dits de « mémoire centrale », qui expriment CCR7, des lymphocytes T « mémoires effecteurs », qui ne l’expriment pas, mais arborent une pléiade d’autres Rch [21]. CXCR5 est un marqueur caractéristique de la population de lymphocytes T appelés follicular B helper [22]. CCR7 et ses ligands CCL19 et CCL21 sont également impliqués dans le guidage des cellules dendritiques (DC) jusqu’aux ganglions lymphatiques [20]. Enfin, les chimiokines participent, comme les cytokines, à la différenciation fonctionnelle des cellules effectrices, comme pour les CD4 Th1/Th2 [23], mais aussi pour les CD8 [24], les NK (natural killer) [25], les monocytes [26] et les DC [27] (Tableau I).
Différenciation leucocytaire et expression différentielle des récepteurs de chimiokines sur les cellules lymphoïdes humaines.
Fonctions physiopathologiques des chimiokines : un « code barre » adapté à chaque situation
Comme souvent, ce recrutement physiologique a son pendant pathologique. Un état donné du réseau des Ch et des cytokines est associé à un type d’inflammation particulier : Th2 comme la dermatite et l’asthme, Th1 comme la maladie de Crohn et la sclérose en plaques. La diapédèse d’une cellule - au cours d’une pathologie particulière, à un stade de différenciation déterminé et à travers un type donné de barrière endothéliale - nécessite un « code barre » précis, dont les éléments identifiants sont constitués des Ch, des Rch, des intégrines et de leurs ligands, afin de pouvoir atteindre un site particulier [6]. Il s’agit donc d’une combinatoire raffinée, qui permet le recrutement des « bonnes » cellules au « bon » endroit et au « bon » moment (Figure 2).
L’importance fonctionnelle des Ch et des Rch est d’ailleurs confirmé par leur détournement par les virus [28]. On sait que le virus d’immunodéficience humaine (VIH) utilise, en plus du CD4, le CCR5 et le CXCR4 comme corécepteurs pour infecter les lymphocytes T4. De son côté, Plasmodium vivax se fixe sur les érythrocytes qu’il infecte en se liant à l’antigène Duffy, qui se révèle être un Rch particulier [29]. Au-delà de cette exploitation de Rch existants, certains virus herpétiques (CMV - cytomégalovirus, HHV6 (human herpes virus), HHV7 et HHV8) sont capables de sécréter des Ch et des Rch, qui agissent comme des leurres pour les Rch et les Ch cellulaires [28].
Utilisation thérapeutique des chimiokines
Ces différentes implications physiopathologiques des Ch et de leurs récepteurs ont motivé leur utilisation à des fins thérapeutiques. Selon que l’on cherche à inhiber, ré-équilibrer ou stimuler un effet des Ch, on peut distinguer trois stratégies d’utilisation pharmacologique des Ch.
Recherche d’antagonistes des chimiokines
C’est dans le cas de l’infection par le VIH que l’application thérapeutique des Ch a été tentée en premier lieu. Connaissant leur rôle dans la reconnaissance du virus par la cellule CD4+, des antagonistes de CCR5 et de CXCR4 ont été testés en études cliniques avec quelques résultats prometteurs [30].
De nombreuses Ch sont exprimées au cours de l’athérogenèse, inflammation des parois vasculaires, qui constitue la première cause des accidents cardiovasculaires. Parmi elles, CCL2 et CX3CL1 semblent avoir un rôle particulièrement important dans la formation de la plaque d’athérome et l’influx initial de monocytes dans la paroi de l’artère [31]. Des analogues de chacune de ces Ch ont donc été recherchés : leurs tests dans des modèles animaux sont encourageants [32].
L’asthme est associé à une accumulation sélective et une activation d’éosinophiles et de mastocytes au niveau de l’épithélium bronchique. Le CCR3 et ses ligands semblent être impliqués dans ce recrutement. Récemment, une étude clinique de phase II utilisant un antagoniste de CCR3 a été mise en place pour le traitement de l’asthme et de la rhinite allergique [33]. Par ailleurs, des antagonistes des Ch sont en essai clinique dans certaines pathologies inflammatoires auto-immunes comme la polyarthrite rhumatoïde ou la sclérose en plaques [34].
De nombreux travaux indiquent que les interactions Ch-Rch ont un rôle dans l’infiltration leucocytaire et la production des médiateurs inflammatoires associés au rejet de greffe. Ainsi, l’inactivation chez la souris des Rch comme CXCR3 [35], et dans une moindre mesure CX3CR1 [36], CCR1 [37] et CCR5 [38], permet une augmentation substantielle de la survie de greffe de cœur. La protection du greffon a également été observée dans d’autres contextes tissulaires comme le rein, le poumon ou la peau. Une amélioration de la survie a aussi été obtenue en traitant des rongeurs avec des anticorps ou des antagonistes bloquant ces Rch. En revanche, l’utilisation d’anticorps neutralisant les ligands correspondants est généralement moins efficace, sauf dans le cas d’IP-10 (interferon-inducible protein-10) [39]. La traduction chez l’homme du rôle de CCR5 dans la transplantation est observée chez les receveurs porteurs homozygotes de la forme inactive du CCR5, pour lesquels la durée de vie des greffes rénales est prolongée [40].
Ré-équilibrer l’environnement en chimiokinique
En fait, l’étude de leurs fonctions physiopathologiques a clairement montré que les Ch n’intervenaient pas seulement dans la migration cellulaire. Ainsi, dans le cancer, elles interviennent aussi dans les phénomènes de transformation cellulaire, de dissémination des métastases, de développement tumoral et de régulation angiogénique. CXCR3 et ses ligands sont angiostatiques [41], tandis que les couples CXCR2/CXCL8 et CXCR4/CXCL12 sont nettement angiogéniques [42]. Enfin, de nombreux autres travaux attestent que certaines Ch et leurs récepteurs orchestrent la destination précise et préférentielle de cellules métastatiques vers un organe donné.
Au vu du rôle important des Ch dans la régulation de l’angiogenèse tumorale et des processus métastatiques, de nombreux travaux tentent d’utiliser des analogues de Ch, agonistes ou antagonistes, pour obtenir une réduction tumorale [43]. Plusieurs études ont en effet démontré qu’un recrutement, par les Ch, de lymphocytes infiltrants dans une tumeur indique un pronostic favorable. L’expression de CCL5 par les cellules tumorales de patients ayant un cancer du poumon a été associée à une réponse lymphocytaire active, et constitue un facteur prédictif de survie [44]. Enfin, l’étude de patients ayant des cancers colorectaux montre une corrélation positive entre la présence de CX3CL1 au niveau des tumeurs, le recrutement des lymphocytes infiltrant les tumeurs et le taux de survie [45].
Afin de rétablir l’équilibre des cellules immunocompétentes en faveur des cellules effectrices T ou NK, des modèles expérimentaux ont été développés afin de changer l’équilibre chimiokinique. En effet, la seule addition des Ch CCL 1, −2, −3, −5, −16, −19, −20, −21, CXCL10 ou XCL1 induit une régression tumorale et une immunité face à un nouveau challenge tumoral [46]. Toutefois, le seul recrutement des cellules ne suffit pas, il faut aussi que ces cellules puissent cibler les cellules tumorales. C’est ce qui a été tenté en utilisant des molécules-chimères, fusion d’une Ch avec un antigène associé aux tumeurs. Ainsi, les protéines chimériques couplant CXCL10 ou CCL7 aux régions variables d’immunoglobulines spécifiques de cellules de lymphomes sont capables de déclencher une réponse inflammatoire et de produire une protection anti-tumorale [47]. D’autres Ch comme CCL19, CCL20 et CCL21 permettent de recruter les DC immatures et induisent un effet antitumoral efficace [48], mais cette migration doit être associée à l’activation des DC [49]. Quoiqu’il en soit, les multiples fonctions des Ch (angiostatique/angiogénique, défensif/trophique, recrutement lymphocytaire/dispersion métastatique) dans un environnement tumoral déjà riche en Ch rendent difficile leur utilisation directe dans la thérapeutique anticancéreuse.
Les chimiokines comme adjuvants de vaccins
On sait que, pour un vaccin, le choix des adjuvants vaccinaux est aussi important que la sélection du ou des antigènes. Ces adjuvants stimulent en effet l’immunité innée par les Toll-like receptors, qui reconnaissent les signaux de danger. Ainsi, le vaccin ADN contenant des motifs CpG imite les effets des virus atténués dans leur capacité à induire les réponses immunitaires T. Pourtant, le niveau d’immunogénicité de ces vaccins ADN est insuffisant pour obtenir des réponses fortes chez l’homme [50]. Cette insuffisance peut être compensée par de l’ADN codant pour des cytokines et des Ch [51]. L’utilisation de CCL5, CCL2 et CCL21 comme adjuvants vaccinaux s’est ainsi montrée bénéfique pour améliorer les réponses induites par la vaccination ADN anti-VIH [52]. À partir de là, des vaccins plus efficaces pourraient être produits, ciblant par exemple telle ou telle sous-population lymphocytaire particulière, ou utilisant tel ou tel site de vaccination plus spécifique.
Conclusions
Les chimiokines ont suscité une recherche passionnante aussi bien sur le plan fondamental que préclinique. Si les nombreuses tentatives d’essais thérapeutiques restent pour l’instant décevantes [5], elles sont toujours instructives, car reposant de nouvelles questions de physiologie fondamentale. La complexité du réseau des chimiokines est, à cet égard, particulièrement typique de celle de cet autre réseau particulièrement intriqué d’études fondamentales et appliquées que constitue l’immunologie moderne.

Article reçu le 7 mars 2006, accepté le 16 juin 2006.
Références
- Foussat A, Galanaud P, Emilie D. Les chimiokines et la longue marche des leucocytes. Med Sci (Paris) 2000; 16 : 757–66. [Google Scholar]
- Cyster JG. Chemokines, sphingosine-1-phosphate, and cell migration in secondary lymphoid organs. Annu Rev Immunol 2005; 23 : 127–59. [Google Scholar]
- Mantovani A. The chemokine system: redundancy for robust outputs. Immunol Today 1999; 20 : 254–7. [Google Scholar]
- Morange M. Déconstruction de la notion de gène. Med Sci (Paris) 2004; 20 : 835–6. [Google Scholar]
- Luster AD, Alon R, von Andrian UH. Immune cell migration in inflammation: present and future therapeutic targets. Nat Immunol 2005; 6 : 1182–90. [Google Scholar]
- Rot A, Von Andrian UH. Chemokines in innate and adaptive host defense: basic chemokinese grammar for immune cells. Ann Rev Imm. 2004; 22 : 891–928. [Google Scholar]
- Springael JY, Urizar E, Parmentier M. Dimerization of chemokine receptors and its functional consequences. Cytokine Growth Factor Rev 2005; 16 : 611–23. [Google Scholar]
- Bulenger S, Marullo S, Bouvier M. Emerging role of homo- and heterodimerization in G-protein-coupled receptor biosynthesis and maturation. Trends Pharmacol Sci 2005; 26 : 131–7. [Google Scholar]
- Jordan BA, Devi LA. G-protein-coupled receptor heterodimerization modulates receptor function. Nature 1999; 399 : 697–700. [Google Scholar]
- Percherancier Y, Berchiche YA, Slight I, et al. Bioluminescence resonance energy transfer reveals ligand-induced conformational changes in CXCR4 homo- and heterodimers. J Biol Chem 2005; 280 : 9895–903. [Google Scholar]
- El-Asmar L, Springael JY, Ballet S, et al. Evidence for negative binding cooperativity within CCR5-CCR2b heterodimers. Mol Pharmacol 2005; 67 : 460–9. [Google Scholar]
- Chen C, Li J, Bot G, et al. Heterodimerization and cross-desensitization between the [mu]-opioid receptor and the chemokine CCR5 receptor. Eur J Pharmacol 2004; 483 : 175–86. [Google Scholar]
- Lortat-Jacob H, Grosdidier A, Imberty A. Structural diversity of heparan sulfate binding domains in chemokines. Proc Natl Acad Sci USA 2002; 99 : 1229–34. [Google Scholar]
- Proudfoot AE, Handel TM, Johnson Z, et al. Glycosaminoglycan binding and oligomerization are essential for the in vivo activity of certain chemokines. Proc Natl Acad Sci USA 2003; 100 : 1885–90. [Google Scholar]
- Van Den Steen PE, Wuyts A, Husson SJ, et al. Gelatinase B/MMP-9 and neutrophil collagenase/MMP-8 process the chemokines human GCP-2/CXCL6, ENA-78/CXCL5 and mouse GCP-2/LIX and modulate their physiological activities. Eur J Biochem 2003; 270 : 3739–49. [Google Scholar]
- Thelen M. Dancing to the tune of chemokines. Nat Immunol 2001; 2 : 129–34. [Google Scholar]
- Roscic-Mrkic B, Fischer M, Leemann C, et al. RANTES (CCL5) utilizes the proteoglycan CD44 as an auxiliary receptor to mediate cellular activation signals and HIV-1 enhancement. Blood 2003; 24 : 24. [Google Scholar]
- Moatti D, Faure S, Fumeron F, et al. Polymorphism in the fractalkine receptor CX3CR1 as a genetic risk factor for coronary artery disease. Blood 2001; 97 : 1925–8. [Google Scholar]
- Lavergne E, Labreuche J, Daoudi M, et al. Adverse associations between CX3CR1 polymorphisms and risk of cardiovascular or cerebrovascular disease. Arterioscler Thromb Vasc Biol 2005; 25 : 847–53. [Google Scholar]
- Campbell DJ, Kim CH, Butcher EC. Chemokines in the systemic organization of immunity. Immunol Rev 2003; 195 : 58–71 [Google Scholar]
- Muller G, Hopken UE, Lipp M. The impact of CCR7 and CXCR5 on lymphoid organ development and systemic immunity. Immunol Rev 2003; 195 : 117–35. [Google Scholar]
- Breitfeld D, Ohl L, Kremmer E, et al. Follicular B helper T cells express CXC chemokine receptor 5, localize to B cell follicles, and support immunoglobulin production. J Exp Med 2000; 192 : 1545–52. [Google Scholar]
- O’Garra A, McEvoy LM, Zlotnik A. T-cell subsets: chemokine receptors guide the way. Curr Biol 1998; 8 : R646–9. [Google Scholar]
- Rabin RL, Park MK, Liao F, et al. Chemokine receptor responses on T cells are achieved through regulation of both receptor expression and signaling. J Immunol 1999; 162 : 3840–50. [Google Scholar]
- Morris MA, Ley K. Trafficking of natural killer cells. Curr Mol Med 2004; 4 : 431–8. [Google Scholar]
- Ancuta P, Moses A, Gabuzda D. Transendothelial migration of CD16+ monocytes in response to fractalkine under constitutive and inflammatory conditions. Immunobiology 2004; 209 : 11–20. [Google Scholar]
- Caux C, Vanbervliet B, Massacrier C, et al. Regulation of dendritic cell recruitment by chemokines. Transplantation 2002; 73 : S7–11. [Google Scholar]
- Murphy PM. Viral exploitation and subversion of the immune system through chemokine mimicry. Nat Immunol 2001; 2 : 116–22. [Google Scholar]
- Hatabu T, Kawazu S, Aikawa M, et al. Binding of Plasmodium falciparum-infected erythrocytes to the membrane-bound form of Fractalkine/CX3CL1. Proc Natl Acad Sci USA 2003; 100 : 15942–6. [Google Scholar]
- Onuffer J, Horuk R. Chemokines, chemokine receptors and small-molecule antagonists : recent developments. Trends Pharmacol Sci 2002; 23 : 459. [Google Scholar]
- Reape TJ, Groot PH. Chemokines and atherosclerosis. Atherosclerosis 1999; 147 : 213–25. [Google Scholar]
- Bursill CA, Channon KM, Greaves DR. The role of chemokines in atherosclerosis: recent evidence from experimental models and population genetics. Curr Opin Lipidol 2004; 15 : 145–9. [Google Scholar]
- Elsner J, Escher SE, Forssmann U. Chemokine receptor antagonists: a novel therapeutic approach in allergic diseases. Allergy 2004; 59 : 1243–58. [Google Scholar]
- Charo IF, Ransohoff RM. The many roles of chemokines and chemokine receptors in inflammation. N Engl J Med 2006; 354 : 610–21. [Google Scholar]
- Hancock WW, Lu B, Gao W, et al. Requirement of the chemokine receptor CXCR3 for acute allograft rejection. J Exp Med 2000; 192 : 1515–20. [Google Scholar]
- Haskell CA, Hancock WW, Salant DJ, et al. Targeted deletion of CX(3)CR1 reveals a role for fractalkine in cardiac allograft rejection. J Clin Invest 2001; 108 : 679–88. [Google Scholar]
- Gao W, Topham PS, King JA, et al. Targeting of the chemokine receptor CCR1 suppresses development of acute and chronic cardiac allograft rejection. J Clin Invest 2000; 105 : 35–44. [Google Scholar]
- Gao W, Faia KL, Csizmadia V, et al. Beneficial effects of targeting CCR5 in allograft recipients. Transplantation 2001; 72 : 1199–205. [Google Scholar]
- Hancock WW, Wang L, Ye Q, et al. Chemokines and their receptors as markers of allograft rejection and targets for immunosuppression. Curr Opin Immunol 2003; 15 : 479–86. [Google Scholar]
- Fischereder M, Luckow B, Hocher B, et al. CC chemokine receptor 5 and renal-transplant survival. Lancet 2001; 357 : 1758–61. [Google Scholar]
- Sgadari C, Angiolillo AL, Tosato G. Inhibition of angiogenesis by interleukin-12 is mediated by the interferon-inducible protein 10. Blood 1996; 87 : 3877–82. [Google Scholar]
- Salcedo R, and Oppenheim JJ. Role of chemokines in angiogenesis: CXCL12/SDF-1 and CXCR4 interaction, a key regulator of endothelial cell responses. Microcirculation 2003; 10 : 359–70. [Google Scholar]
- Balkwill F. Cancer and the chemokine network. Nat Rev Cancer 2004; 4 : 540–50. [Google Scholar]
- Moran CJ, Arenberg DA, Huang CC, et al. RANTES expression is a predictor of survival in stage I lung adenocarcinoma. Clin Cancer Res 2002; 8 : 3803–12. [Google Scholar]
- Ohta M, Tanaka F, Yamaguchi H, et al. The high expression of Fractalkine results in a better prognosis for colorectal cancer patients. Int J Oncol 2005; 26 : 41–7. [Google Scholar]
- Rollins BJ, Sunday ME. Suppression of tumor formation in vivo by expression of the JE gene in malignant cells. Mol Cell Biol 1991; 11 : 3125–31. [Google Scholar]
- Biragyn A, Kwak LW. B-cell malignancies as a model for cancer vaccines: from prototype protein to next generation genetic chemokine fusions. Immunol Rev 1999; 170 : 115–26. [Google Scholar]
- Caux C, Ait-Yahia S, Chemin K, et al. Dendritic cell biology and regulation of dendritic cell trafficking by chemokines. Springer Semin Immunopathol 2000; 22 : 345–69. [Google Scholar]
- Merad M, Fong L, Bogenberger J, et al. Differentiation of myeloid dendritic cells into CD8alpha-positive dendritic cells in vivo. Blood 2000; 96 : 1865–72. [Google Scholar]
- Shedlock DJ, Weiner DB. DNA vaccination: antigen presentation and the induction of immunity. J Leukoc Biol 2000; 68 : 793–806. [Google Scholar]
- Scheerlinck JY. Genetic adjuvants for DNA vaccines. Vaccine 2001; 19 : 2647–56. [Google Scholar]
- Xin KQ, Lu Y, Hamajima K, et al. Immunization of RANTES expression plasmid with a DNA vaccine enhances HIV-1-specific immunity. Clin Immunol 1999; 92 : 90–6. [Google Scholar]
- Sozzani S. Dendritic cell trafficking: more than just chemokines Cytokine Growth Factor Rev 2005; 16 : 581–92. [Google Scholar]
- Moser B, Wolf M, Walz A, et al. Chemokines: multiple levels of leukocyte migration control. Trends Immunol 2004; 25 : 75–84. [Google Scholar]
- O’Garra A, McEvoy LM, Zlotnik A. T-cell subsets: chemokine receptors guide the way Curr Biol 1998; 8 : R646–9. [Google Scholar]
- Geissmann F, Jung S, Littman DR. Blood monocytes consist of two principal subsets with distinct migratory properties. Immunity 2003; 19 : 71–82. [Google Scholar]
- Ancuta P, Rao R, Moses A, et al. Fractalkine preferentially mediates arrest and migration of CD16+ monocytes. J Exp Med 2003; 197 : 1701–7. [Google Scholar]
- Maghazachi AA. Compartmentalization of human natural killer cells. Mol Immunol 2005; 42 : 523–9. [Google Scholar]
Liste des tableaux
Différenciation leucocytaire et expression différentielle des récepteurs de chimiokines sur les cellules lymphoïdes humaines.
Liste des figures
 |
Figure 1. Les quatre familles de chimiokines, leurs récepteurs et leurs implications dans diverses pathologies. |
| Dans le texte | |
 |
Figure 2. Pyramide de complexité des chimiokines et de leurs récepteurs. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




