| Numéro |
Med Sci (Paris)
Volume 22, Numéro 6-7, Juin-Juillet 2006
|
|
|---|---|---|
| Page(s) | 567 - 568 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/20062267567 | |
| Publié en ligne | 15 juin 2006 | |
Une nouvelle cellule dendritique impliquée dans l’immunité anti-tumorale
Interferon-producing killer dendritic cells (IKDC)
1
Inserm U805, Faculté de Médecine Paris Sud, Université Paris XI
2
Inserm U805, CIC Biothérapies, Faculté de Médecine Kremlin Bicêtre, Institut Gustave Roussy, 39, rue Camille Desmoulins, 94805 Villejuif, France
Les cellules natural killer (NK) et les cellules dendritiques (CD) jouent un rôle central dans les réponses immunitaires innées et acquises [1, 2]. De plus, ces cellules sont des acteurs importants de la réponse antitumorale [3, 4]. Enfin, il a été démontré que l’IFNγ a un rôle crucial dans l’immunosuveillance antitumorale [4]. Nous avons démontré récemment, chez des souris, que la principale source d’IFNγ provenait non pas des cellules NK mais d’une nouvelle population de CD dénommées IKDC (interferon-producing killer dendritic cells) [5]. Ces cellules ont un phénotype particulier car elles co-expriment des marqueurs de cellules NK et de CD [5, 6]. En contact avec des lignées tumorales, ces cellules sont capables de sécréter de fortes quantités d’IFNγ et de tuer les lignées tumorales par un mécanisme pro-apoptotique dépendant de TRAIL. De plus, le transfert adoptif de ces IKDC chez des souris Rag2−/−IL2rγ−/− permet le rejet de tumeur. Les IKDC représentent donc une nouvelle population de CD participant à la réponse immunitaire antitumorale.
Caractéristiques phénotypiques et morphologiques de IKDC
Lors d’un travail antérieur, notre équipe a montré que le Glivec® (STI571, imatinib mésylate), un inhibiteur de tyrosine kinase (c-Kit, bcr/abl et PDGFR-α), avait une action antitumorale dépendante des cellules NK1.1+ [7]. Afin d’augmenter ces effets antitumoraux, nous avons combiné le Glivec® avec de l’interleukine-2 (IL-2). Dans un modèle de métastases pulmonaires de mélanome murin (B16F10), l’association Glivec®+IL-2 a permis d’obtenir des effets antitumoraux supérieurs à ceux observés après traitement par Glivec® ou IL-2 seuls. L’étude des cellules infiltrant la tumeur (immuno-histochimie et cytométrie) a révélé des cellules ayant un phénotype jusqu’alors jamais décrit. En effet, ces cellules co-expriment à la fois des marqueurs de cellules NK (NK1.1+/DX5+/NKG2D+) et de CD (CD11c+/B220+/I-Ab). De plus, ces cellules n’expriment pas les marqueurs dendritiques plasmacytoïdes, PDCA1 et Gr1 [5].
Cette nouvelle population cellulaire est retrouvée dans la moelle osseuse, la rate, les ganglions, le foie et les poumons. Une analyse en microscopie électronique montre que ces cellules à l’état de repos sont de très petite taille (5 à 6 µm), plus petites que des cellules NK, elles ont peu d’expansions cytoplasmiques, un rapport nucléocytoplasmique très élevé, un cytoplasme dense contenant peu de mitochondries mais de nombreuses structures multivésiculaires (figure 1). Ainsi, notre thérapie associant le Glivec® et l’IL-2 nous a permis d’identifier une nouvelle population de CD CD11c+B220+ ayant une morphologie unique et qui co-expriment des marqueurs de cellules NK (DX5, NK1.1 et NKG2D) appelées IKDC (interferon-producing killer dendritic cells) [5, 6].
 |
Figure 1. Morphologie des IKDC. A. Photo de microscopie électronique d’une IKDC de rate de souris phagocytant des débris cellulaires après coculture de 24 heures avec des cellules tumorales B16F10 (réalisée par Graça Raposo, Institut Curie, Paris, France). B. Photo d’une coloration en May Grünwald Giemsa d’IKDC (rate de souris sans culture) après cytospin. |
Mécanisme d’action antitumoral des IKDC
Les IKDC sont capables de tuer spontanément des cellules tumorales in vitro. L’étude des mécanismes impliqués dans cette cytotoxicité montre que les effets antitumoraux observés lors de l’administration de notre combinaison dépendent d’un récepteur de mort cellulaire le TNF-related apoptosis-inducing ligand (TRAIL). En effet, l’association Glivec® + IL-2 n’est plus efficace lorsque les animaux reçoivent un anticorps permettant de bloquer TRAIL in vivo. Cette inhibition est confirmée au niveau cellulaire in vitro. De plus, l’expression de TRAIL à la surface des IKDC est confirmée par cytométrie en flux [5]. Parmi les autres mécanismes explorés, les expérimentations faite chez la souris Tnf−/− a permis d’exclure un mécanisme dépendant du TNF [5].
Comme l’expression de TRAIL est, entre autres, contrôlée par l’IFN type II [8, 9] nous avons testé l’efficacité de notre traitement chez des souris IFN de type II R−/−. Chez ces souris, l’efficacité de la combinaison thérapeutique Glivec® + IL-2 est totalement inhibée. L’étude in vitro des IKDC démontre, qu’en présence de cellules tumorales, elles deviennent capables de sécréter des quantités importantes d’IFNγ, et cela de manière beaucoup plus importante que les cellules NK [5]. De plus, le contact avec des cellules tumorales B16F10 est nécessaire mais suffisant pour induire la sécrétion d’IFNγ par les IKDC, alors que les cellules NK, dans ces conditions, n’en produisent pas [5], cette sécrétion étant évidemment augmentée en présence de notre combinaison Glivec® + IL-2. Enfin, le transfert adoptif de cellules IKDC dans des tumeurs B16F10 implantées en sous-cutané chez des souris Rag2−/−IL2rγ−/− permet une inhibition totale de la croissance tumorale lorsque les IKDC proviennent de souris C57BL/6 traitées par Glivec® + IL-2 [5]. Toutes ces observations nous permettent de conclure que les IKDC sont cytotoxiques par un mécanisme dépendant de TRAIL et que la régulation de l’expression de TRAIL sur les IKDC dépend très probablement de l’IFNγ qu’elles sécrètent [5, 10].
L’équipe des « co-découvreurs » de Franck Housseau, a permis de démonter que ces cellules sont aussi capables de sécréter de l’IFNα en présence de séquences ODN CpG [6]. Ils démontrent, in vitro, que les IKDC activées par des séquences CpG sont capables d’être cytotoxiques par un mécanisme dépendant de NKG2D. De plus, cette équipe montre que les IKDC sont capables d’apprêter un antigène et de le présenter au lymphocytes T CD4+ [6].
Du fait de leur capacité à tuer des cibles et à présenter des antigènes, les IKDC peuvent être considérées comme des CD essentielles permettant le lien entre immunité innée et acquise (Figure 2).
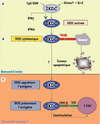 |
Figure 2. Mécanisme d’action des IKDC. Les IKDC peuvent exercer différentes fonctions. En effet, elles sont tueuses et aussi capables de présenter des antigènes aux lymphocytes T. L’activation des IKDC aboutit à la production d’interférons [5, 6]. L’IFNγ permettrait d’augmenter l’expression de TRAIL à la surface des IKDC (A). Les IKDC ainsi activées tuent les cellules tumorales par un mécanisme dépendant de TRAIL (B). Comme les IKDC activées ont également la capacité d’exprimer des molécules du CMH II, elles pourraient être capables d’apprêter les antigènes tumoraux et de les présenter aux lymphocytes T CD4+ initiant ainsi une réponse immunitaire acquise (C). |
Conclusion et perspectives
La pertinence physiologique de cette découverte ne sera pas évidente tant que l’homologue humain ne sera pas identifié. Les tumeurs pressenties sensibles in vitro à la lyse par TRAIL et/ou l’effet anti-angiogénique de l’IFN³ seront prochainement les cibles des essais cliniques combinant Glivec® et IL-2, sous réserve d’un soutien de Novartis. L’Institut Gustave Roussy s’efforcera de lancer ces essais de Phase I/II rapidement. Un des objectifs de ce type d’essai est de mettre en lumière l’homologue humain de l’IKDC murine pour prévoir son expansion ex vivo et sa réinjection à plus long terme. Si les thérapies cellulaires dendritiques se retrouvent en difficulté en 2006, c’est en partie parce que ces cellules migrent mal aux ganglions et qu’elles présentent difficilement les antigènes exogènes tumoraux aux lymphocytes T. Notre IKDC pourrait peut-être faire d’une pierre deux coups. C’est une CD tueuse et présentatrice d’antigènes. L’équipe américaine « co-découvreuse » a pu effectivement démontrer que l’IKDC migrait du sang vers le ganglion dans la zone riche en T pour éduquer les lymphocytes T. Nous devons nous efforcer de démontrer qu’elle tue puis présente les a ntigènes tumoraux à tous les ganglions de l’organisme. Cette démonstration serait vraiment une victoire pour les spécialistes du domaine et le monde de la vaccination.
Références
- Cerwenka A, Lanier LL. Natural killer cells, viruses and cancer. Nat Rev Immunol 2001; 1 : 41–9. [Google Scholar]
- Steinman RM. Some interfaces of dendritic cell biology. Apmis 2003; 111 : 675–97. [Google Scholar]
- Kaplan DH, Shankaran V, Dighe AS, et al. Demonstration of an interferon gamma-dependent tumor surveillance system in immunocompetent mice. Proc Natl Acad Sci USA 1998; 95 : 7556–61. [Google Scholar]
- Shankaran V, Ikeda H, Bruce AT, et al. IFNgamma and lymphocytes prevent primary tumour development and shape tumour immunogenicity. Nature 2001; 410 : 1107–11. [Google Scholar]
- Taieb J, Chaput N, Menard C, et al. A novel dendritic cell subset involved in tumor immunosurveillance. Nat Med 2006; 12 : 214–9. [Google Scholar]
- Chan CW, Crafton E, Fan HN, et al. Interferon-producing killer dendritic cells provide a link between innate and adaptive immunity. Nat Med 2006; 12 : 207–13. [Google Scholar]
- Borg C, Terme M, Taieb J, et al. Novel mode of action of c-kit tyrosine kinase inhibitors leading to NK cell-dependent antitumor effects. J Clin Invest 2004; 114 : 379–88. [Google Scholar]
- Smyth MJ, Takeda K, Hayakawa Y, et al. Nature’s TRAIL : on a path to cancer immunotherapy. Immunity 2003; 18 : 1–6. [Google Scholar]
- Yagita H, Takeda K, Hayakawa Y, et al. TRAIL and itsreceptors as targets for cancer therapy. Cancer Sci 2004; 95 : 777–83. [Google Scholar]
- Shortman K, Villadangos JA. Is it a DC, is it an NK ? No, it’s an IKDC. Nat Med 2006; 12 : 167–8. [Google Scholar]
© 2006 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Morphologie des IKDC. A. Photo de microscopie électronique d’une IKDC de rate de souris phagocytant des débris cellulaires après coculture de 24 heures avec des cellules tumorales B16F10 (réalisée par Graça Raposo, Institut Curie, Paris, France). B. Photo d’une coloration en May Grünwald Giemsa d’IKDC (rate de souris sans culture) après cytospin. |
| Dans le texte | |
 |
Figure 2. Mécanisme d’action des IKDC. Les IKDC peuvent exercer différentes fonctions. En effet, elles sont tueuses et aussi capables de présenter des antigènes aux lymphocytes T. L’activation des IKDC aboutit à la production d’interférons [5, 6]. L’IFNγ permettrait d’augmenter l’expression de TRAIL à la surface des IKDC (A). Les IKDC ainsi activées tuent les cellules tumorales par un mécanisme dépendant de TRAIL (B). Comme les IKDC activées ont également la capacité d’exprimer des molécules du CMH II, elles pourraient être capables d’apprêter les antigènes tumoraux et de les présenter aux lymphocytes T CD4+ initiant ainsi une réponse immunitaire acquise (C). |
| Dans le texte | |
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.




