Figure 2.
Télécharger l'image originale
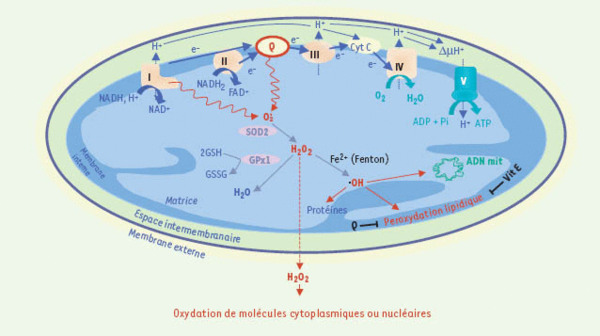
Production mitochondriale et prise en charge de l’anion superoxyde. Au cours du transfert des électrons, dans des conditions physiologiques, il peut y avoir des fuites d’électrons et production d’anion superoxyde (
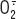 ) par le complexe I et le coenzyme Q.
) par le complexe I et le coenzyme Q. 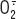 est métabolisé par la superoxyde dismutase (SOD2, ou MnSOD, étant l’isoforme spécifiquement localisée dans la matrice mitochondriale) en peroxyde d’hydrogène (H2O2). Celui-ci peut être décomposé en H2O par la glutathion peroxydase (GPx1), en présence de glutathion réduit (GSH), se transformer en radical hydroxyle (.OH) par la réaction de Fenton, en présence de Fe2+, ou encore diffuser dans le cytoplasme et modifier l’activité de protéines cytoplasmiques ou nucléaires en les oxydant. Le radical hydroxyle peut également oxyder les protéines, ou l’ADN (mitochondrial et nucléaire), et induire la peroxydation lipidique (elle-même limitée par des piégeurs de radicaux libres, de nature lipophile, tels que la vitamine E ou le coenzyme Q). Il est important de souligner ici la dualité d’action du coenzyme Q : piégeur de radicaux libres, sous forme réduite, dans les membranes biologiques, il est la source essentielle d’O-.2 dans la chaîne respiratoire.
est métabolisé par la superoxyde dismutase (SOD2, ou MnSOD, étant l’isoforme spécifiquement localisée dans la matrice mitochondriale) en peroxyde d’hydrogène (H2O2). Celui-ci peut être décomposé en H2O par la glutathion peroxydase (GPx1), en présence de glutathion réduit (GSH), se transformer en radical hydroxyle (.OH) par la réaction de Fenton, en présence de Fe2+, ou encore diffuser dans le cytoplasme et modifier l’activité de protéines cytoplasmiques ou nucléaires en les oxydant. Le radical hydroxyle peut également oxyder les protéines, ou l’ADN (mitochondrial et nucléaire), et induire la peroxydation lipidique (elle-même limitée par des piégeurs de radicaux libres, de nature lipophile, tels que la vitamine E ou le coenzyme Q). Il est important de souligner ici la dualité d’action du coenzyme Q : piégeur de radicaux libres, sous forme réduite, dans les membranes biologiques, il est la source essentielle d’O-.2 dans la chaîne respiratoire.
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.




