| Issue |
Med Sci (Paris)
Volume 21, Number 11, Novembre 2005
|
|
|---|---|---|
| Page(s) | 909 - 910 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/20052111909 | |
| Published online | 15 November 2005 | |
L’endocytose, cheval de Troie pour l’infection virale
Endocytosis: cheval de Troie of viral infection
Département de Biochimie, Université de Genève, 30, quai Ernest Ansermet, 1211 Genève, Suisse
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
L’endocytose est un réseau complexe de compartiments membranaires. Elle est nécessaire à l’internalisation d’éléments nutritifs, à la régulation de l’expression en surface des récepteurs membranaires activés et au maintien de l’équilibre de la membrane plasmique. Les molécules internalisées à partir de la membrane plasmique arrivent tout d’abord dans des compartiments formés de tubules et de corps vésiculaires au pH légèrement acide (pH 6,2), les endosomes précoces. De là, elles sont soit recyclées vers la membrane plasmique via les endosomes de recyclage, soit dirigées vers les endosomes tardifs (pH 5,5) et les lysosomes pour être dégradées. Le trafic entre endosomes précoces et tardifs est assuré par des intermédiaires appelés vésicules endosomiques de transport ou endosomal carrier vesicles (ECV). Les compartiments membranaires de la voie de dégradation, ECV et endosomes tardifs, sont, contrairement aux autres organites de l’appareil vacuolaire, très riches en vésicules internes. Ces dernières se forment au niveau des endosomes précoces où les molécules destinées à être dégradées y sont internalisées [1].
Depuis quelques années, de plus en plus d’exemples montrent que, dans les cellules de mammifère, les molécules incorporées dans les membranes internes ne sont pas forcément toutes dégradées. C’est le cas des récepteurs du mannose-6-phosphate (M6PR) qui transitent entre le réseau trans-golgien et les endosomes tardifs, ou encore des tétraspanines qui s’accumulent dans les vésicules internes. Un autre cas bien connu est celui des molécules du complexe majeur d’histocompatibilité de classe II. Ces protéines sont stockées dans les membranes internes des endosomes tardifs des cellules dendritiques immatures. Une fois les cellules activées, les molécules sont transportées jusqu’à la membrane plasmique via la formation de tubules résultant probablement de la fusion entre membranes internes et limitantes des endosomes [2].
Ainsi, les cellules de mammifères semblent avoir développé un système de tri et de recyclage très efficace au niveau des endosomes tardifs. Les mécanismes impliqués dans la dynamique entre membranes limitantes et internes sont encore mal connus.
Dans un travail récent, nous avons montré qu’un virus, le virus de la stomatite vésiculaire ou vesicular somatitis virus (VSV), a pris avantage des vésicules internes de l’endosome pour infecter les cellules efficacement [3]. VSV est un virus à enveloppe qui entre dans les cellules via la voie de l’endocytose. Une fois internalisé, l’enveloppe du virus fusionne avec la membrane des endosomes. Cette fusion est due au changement de conformation d’une protéine virale de surface sensible au pH acide des endosomes. À la suite de la fusion, VSV libère sa nucléocapside (ARN et nucléoprotéines) dans le cytosol de la cellule où l’ARN est répliqué [4]. Nous avons montré que, contrairement à ce que l’on aurait pu penser, la fusion du virus avec les membranes endosomiques et la libération de la nucléocapside dans le cytoplasme se déroulent en deux temps, à deux étapes différentes de l’endocytose. En effet, la fusion virale se produit déjà dans les ECV tandis que la nucléocapside n’est libérée qu’à partir des endosomes tardifs (Figure 1). Par microscopie électronique, nous avons observé que le virus fusionne majoritairement avec les membranes internes des ECV, ainsi la nucléocapside se cache dans les vésicules internes des ECV – un espace topologiquement équivalent au cytoplasme - mais non continu avec celui-ci (Figure 1). Pour le virus, la fusion entre membranes internes et limitantes lui permet d’éviter d’être dégradé dans les lysosomes. VSV se sert donc des endosomes comme cheval de Troie, ce qui lui permet d’atteindre la région périnucléaire tout en évitant la barrière du cytosquelette d’actine.
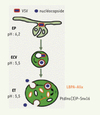 |
Figure 1. Trafic de VSV jusqu’aux endosomes tardifs. Modèle: après internalisation, VSV (vesicular somatitis virus) atteint chronologiquement les endosomes précoces (EP), les ECV (endosomal carrier vesicles) puis les endosomes tardifs (ET). Le pH acide des ECV induit la fusion du virus avec les membranes endosomiques. Après fusion, la nucléocapside se retrouve dans les vésicules internes des ECV. À cette étape, les membranes internes et limitantes ne peuvent encore interagir. Une fois arrivées dans les endosomes tardifs, les vésicules internes contenant les nucléocapsides fusionnent avec la membrane limitante et libèrent ainsi les nucléocapsides dans le cytoplasme où l’ARN viral est répliqué. Dans les endosomes tardifs, la dynamique membranaire est contrôlée par les phospholipides LBPA et PtdIns(3)P et leurs effecteurs respectifs Alix et Snx-16. |
Pour l’instant, deux lipides semblent être impliqués dans la dynamique membranaire des endosomes tardifs: l’acide lysobiphosphatidique (LBPA) et le phosphatidylinositol-3-phosphate (PtdIns(3)P).
Le LBPA est un lipide peu dégradable détecté dans les membranes internes des endosomes tardifs [5]. Lorsque des anticorps se liant au LBPA sont internalisés, le trafic du cholestérol, des M6PR ainsi que l’infection par VSV sont diminués, suggérant que l’interférence avec ce lipide perturbe la dynamique des membranes internes [3, 5, 6]. De plus, des expériences faites sur des liposomes ont montré que le LBPA peut induire l’invagination de membranes, phénomène régulé par la protéine Alix [7]. Le LBPA et Alix pourraient donc être responsable de l’invagination de la membrane limitante.
Le PtdIns(3)P est lui surtout présent dans les endosomes précoces où il a été décrit comme étant nécessaire à la formation des ECV et au tri des molécules dans les membranes internes [1]. Par un essai in vitro mesurant directement la libération d’ARN viral à partir d’endosomes tardifs enrichis en nucléocapsides, nous avons observé que l’ajout du domaine FYVE ou de protéines Snx-16, tous deux se liant au PtdIns(3)P, diminue la libération d’ARN viral, impliquant le PtdIns(3)P dans la dynamique membranaire endosomique [3].
Dans les endosomes tardifs, le LBPA et le PtdIns(3)P semblent se trouver sur deux groupes de vésicules internes distinctes [8]. Les membranes comportant du PtdIns(3)P proviennent certainement des endosomes précoces et contiennent, entre autres, des protéines destinées à être dégradées. En revanche, les protéines présentes dans les vésicules enrichies en LBPA devraient être recyclées en passant par la membrane limitante des endosomes tardifs. Bien que le devenir de ces populations de vésicules internes soit différent, il paraît nécessaire que leur dynamique soit coordonnée afin de maintenir l’équilibre des endosomes.
Nous sommes encore loin de comprendre toutes les subtilités des mécanismes de tri et de recyclage au sein des endosomes tardifs. Néanmoins, grâce à l’étude de l’infection de VSV, deux acteurs sont maintenant identifiés : les phospholipides LBPA et PtdIns(3)P qui jouent un rôle majeur via leur effecteur respectif Alix et Snx-16.
Références
- Gruenberg J, Stenmark H. The biogenesis of multivesicular endosomes. Nat Rev Mol Cell Biol 2004; 5 : 317–23. [Google Scholar]
- Chow A, Toomre D, Garrett W, Mellman I. Dendritic cell maturation triggers retrograde MHC class II transport from lysosomes to the plasma membrane. Nature 2002; 418 : 988–94. [Google Scholar]
- LeBlanc I, Luyet PP, Pons V, et al. Endosome-to-cytosol transport of viral nucleocapsids. Nat Cell Biol 2005; 7 : 653–64. [Google Scholar]
- Marsh M. The entry of enveloped viruses into cells by endocytosis. Biochem J 1984; 218 : 1–10. [Google Scholar]
- Kobayashi T,Stang E, Fang KS, et al. A lipid associated with the antiphospholipid syndrome regulates endosome structure and function. Nature 1998; 392 : 193–7. [Google Scholar]
- Kobayashi T, Beuchat MH, Lindsay M, et al. Late endosomal membranes rich in lysobisphosphatidic acid regulate cholesterol transport. Nat Cell Biol 1999; 1 : 113–8. [Google Scholar]
- Matsuo H, Chevallier J, Mayran, et al. Role of LBPA and Alix in multivesicular liposome formation and endosome organization. Science 2004; 303 : 531–4. [Google Scholar]
- Gillooly DJ, Morrow IC, Lindsay M, et al. Localization of phosphatidylinositol 3-phosphate in yeast and mammalian cells. EMBO J 2000; 19 : 4577–88. [Google Scholar]
© 2005 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Trafic de VSV jusqu’aux endosomes tardifs. Modèle: après internalisation, VSV (vesicular somatitis virus) atteint chronologiquement les endosomes précoces (EP), les ECV (endosomal carrier vesicles) puis les endosomes tardifs (ET). Le pH acide des ECV induit la fusion du virus avec les membranes endosomiques. Après fusion, la nucléocapside se retrouve dans les vésicules internes des ECV. À cette étape, les membranes internes et limitantes ne peuvent encore interagir. Une fois arrivées dans les endosomes tardifs, les vésicules internes contenant les nucléocapsides fusionnent avec la membrane limitante et libèrent ainsi les nucléocapsides dans le cytoplasme où l’ARN viral est répliqué. Dans les endosomes tardifs, la dynamique membranaire est contrôlée par les phospholipides LBPA et PtdIns(3)P et leurs effecteurs respectifs Alix et Snx-16. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




