| Issue |
Med Sci (Paris)
Volume 21, Number 6-7, Juin–Juillet 2005
|
|
|---|---|---|
| Page(s) | 579 - 581 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2005216-7579 | |
| Published online | 15 juin 2005 | |
Fait nouveau : la méthylation des arginines joue un rôle dans la réparation de l’ADN
A new role for arginine methylation in DNA repair
1
Groupe d’oncologie moléculaire Terry Fox, Centre Bloomfield sur le vieillissement et Départements d’oncologie et de médecine, Université McGill, Institut Lady Davis de recherches médicales, 3755, chemin de la Côte Sainte-Catherine, Montréal, Québec, H3T 1E2 Canada
2
Laboratoire de la Stabilité du génome, Centre de recherche en cancérologie de l’Université Laval, Hôtel-Dieu de Québec, CHUQ, Québec, G1R 2J6 Canada
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
L’ajout d’un ou de deux groupements méthylés à l’azote terminal de l’acide aminé arginine (Figure 1) [1] est ce que l’on appelle la méthylation des arginines ; elle a pour propriété de modifier des protéines. Que ce processus joue un rôle dans la régulation du cycle cellulaire liée aux mécanismes de réparation de l’ADN constitue un fait nouveau. Il a été établi que le complexe protéique MRE11/RAD50/NBS11 (MRN) participe à la réparation de l’ADN et nous avons démontré que le domaine riche en glycines et en arginines (GAR) de MRE11 est méthylé en propre par l’enzyme PRMT1 (protein arginine methyltransferase 1). La mutation des arginines méthylées de MRE11 entraîne une sévère diminution de son activité nucléase nécessaire à sa fonction dans la réparation des cassures double-brin de l’ADN. De même, l’absence de méthylation dans MRE11 entraîne une défaillance de la signalisation des bris aux mécanismes de régulation du cycle cellulaire. Ces données révèlent pour la première fois le rôle que joue la méthylation des arginines dans la régulation des mécanismes de réparation de l’ADN et suggèrent que la méthylation de MRE11 est requise pour maintenir la stabilité du génome au fil des nombreuses divisions cellulaires.
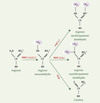 |
Figure 1. Méthylation des arginines. Les arginines peuvent être méthylées sur l’azote par les arginines méthyltransférases de type I ou II pour devenir monométhylées. L’ajout d’un deuxième groupement méthyl sur l’azote opposé se fait par l’intermédiare des enzymes de type II et donne une arginine symétriquement diméthylée. En revanche, l’ajout d’un deuxième groupement méthyl sur le même azote par les enzymes de type I produit une arginine asymétriquement diméthylée. Une arginine monométhylée peut aussi être désimidée par la peptidyl arginine désimidase (PAD4) pour devenir une citrulline. |
Chez les humains, les arginines méthyltransférases (PRMT) font partie d’une famille de huit enzymes qui se servent de la S-adénosyl-méthionine comme donneur de groupement méthyle. Ces enzymes ont été sous-divisées en trois groupes. Les enzymes de type I catalysent la formation d’arginines ω-NG-monométhylées et d’arginines asymétriquement ω-NG, NG-diméthylées (aDMA) et regroupent les enzymes PRMT1, PRMT2, PRMT3, PRMT4 (ou CARM1) et PRMT6. Les enzymes de type II (PRMT5 et PRMT7) catalysent la formation d’arginines ω-NG-monométhylées et d’arginines symétriquement ω-NG, N’G-diméthylées (sDMA). Certaines protéines méthylées par ces enzymes comportent généralement une région riche en glycine et en arginine qu’on retrouve fréquemment dans les protéines se liant à l’ARN [2]. Il n’est donc pas étonnant que la méthylation des arginines participe à la régulation de plusieurs phases du métabolisme de l’ARN : l’import et l’export de protéines et de l’ARN du noyau ; la régulation des liaisons protéines-protéines et protéines-ARN ; la transcription des protéines ; la localisation des protéines ; la biogenèse des ribosomes [3].
Les anticorps ASYM24 et ASYM25, propres aux aDMA, et les anticorps SYM10 et SYM11 reconnaissant les sDMA nous ont permis de répertorier plus de 200 nouvelles protéines potentiellement méthylées sur arginine [4]. L’identification de ces protéines suggère de nouveaux rôles pour la méthylation des protéines dans l’épissage des ARN messagers, la polyadénylation des ARN, la transcription, la signalisation cellulaire et le cytosquelette.
Nul n’avait envisagé jusqu’ici que la méthylation des arginines pouvait jouer un rôle dans la régulation du cycle cellulaire à la suite d’altérations subies par l’ADN, ainsi que dans la régulation des mécanismes de réparation de l’ADN. MRE11 est une protéine conservée aussi bien chez la levure que chez les humains dont l’activité nucléase est relayée par la région aminoterminale [5]. MRE11 interagit avec les protéines RAD50 et NBS1 pour former le complexe MRN (MRE11/RAD50/NBS1). MRN est à la croisée de la réparation des cassures double-brin de l’ADN et de la signalisation des dommages menant à l’arrêt du cycle cellulaire en phase S [6]. Les cassures double-brin peuvent être provoquées naturellement durant la réplication de l’ADN, mais aussi survenir à la suite de l’exposition des cellules à divers agents chimiques ou à des radiations ionisantes. Il nous est donc possible de suggérer que la méthylation des arginines pourrait intervenir dans la régulation du cycle cellulaire ainsi que dans la régulation des mécanismes de réparation de l’ADN.
Nous avons démontré que MRE11 est méthylée à partir des arginines dans un domaine riche en arginines et en glycines [7]. Ce domaine, situé près de la liaison à l’ADN à l’extrémité carboxyterminale de MRE11, est précisément méthylé par PRMT1 in vitro et in vivo. La méthylation des arginines de MRE11 a lieu aussi bien dans les cellules d’insectes que dans les cellules humaines. De plus, la méthylation de MRE11 est absente dans les cellules dérivées de souris mutantes pour la fonction PRMT1. La mutation des arginines en alanines ou en lysines dans le domaine GAR de MRE11 entraîne une diminution de son activité exonucléase in vitro, sans toutefois empêcher la formation du complexe MRN. Ces résultats suggèrent que la méthylation joue un rôle important dans la régulation de -l’activité enzymatique de MRE11 dans les organismes pluricellulaires.
MRE11 prend non seulement une part active dans la réparation des cassures double-brin de l’ADN par son activité nucléase, mais encore exerce une fonction de signalisation de ces dommages aux mécanismes de régulation du cycle cellulaire [6]. Il a été récemment démontré que MRN stimule l’activité kinase d’ATM in vitro envers p53, Chk2 et H2AX [8]. Contrairement aux cellules normales, des cellules traitées avec des inhibiteurs de méthyltransférases poursuivent la réplication de l’ADN malgré la présence de nombreux dommages de l’ADN, ce qui laisse suspecter un défaut dans la signalisation de ces bris d’ADN aux protéines de contrôle du cycle cellulaire. La diminution de PRMT1 par un ARN interférent (ARNi) permet aussi la réplication de l’ADN malgré des altérations ; ce phénotype peut être restauré par la réintroduction du complexe MRN purifié et méthylé, alors qu’un mutant de MRE11 dans la région méthylée en est incapable. Étant donné que l’inhibition de PRMT1 pourrait affecter l’activité de plusieurs protéines, cette expérience de complémentation démontre que le défaut de progression du cycle cellulaire en présence de lésions dans l’ADN est directement relayé par la méthylation sur MRN.
Conclusions
Ces résultats démontrent que la méthylation des arginines joue un rôle dans la régulation des mécanismes de réparation de l’ADN. La régulation de la réplication de l’ADN altéré est certainement un processus essentiel pour une réparation adéquate des cassures double-brin (Figure 2). Puisqu’un défaut de réparation durant la synthèse de l’ADN peut mener à une instabilité génétique, il sera utile d’éclairer davantage les mécanismes d’action de la méthylation de MRE11 liés à la stabilité du génome.
 |
Figure 2. Régulation de MRE11 par la méthylation sur les arginines. La méthylation de MRE11 par PRMT1 est requise pour entraîner une diminution de la réplication de l’ADN endommagé ou pour manifester une signalisation des dommages de l’ADN vers les points de régulation du cycle cellulaire afin de permettre la réparation de l’ADN. |
MRE11 : meiotic recombination mutant 11 ; RAD50: radiation sensitive gene 50 ; NBS1 : Nijmegen breakage syndrome-1.
Références
- Gary JD, Clarke S. RNA and protein interactions modulated by protein arginine methylation. Prog Nucleic Acid Res Mol Biol 1998; 61 : 65–131. [Google Scholar]
- McBride AE, Silver PA. State of the arg : protein methylation at arginine comes of age. Cell 2001; 106 : 5–8. [Google Scholar]
- Boisvert FM, Chénard CA, Richard S. Protein interfaces in signaling regulated by arginine methylation. Sci STKE 2005; 271 : re2. [Google Scholar]
- Boisvert FM, Côté J, Boulanger MC, Richard S. A proteomic analysis of arginine-methylated protein complexes. Mol Cell Proteomics2003; 2 : 1319–30. [Google Scholar]
- Paull TT, Gellert M. The 3’ to 5’ exonuclease activity of MRE11 facilitates repair of DNA double-strand breaks. Mol Cell 1998; 1 : 969–79. [Google Scholar]
- Van den Bosch M, Bree RT, Lowndes NF. The MRN complex : coordinating and mediating the response to broken chromosomes. EMBO Rep 2003; 4 : 844–9. [Google Scholar]
- Boisvert FM, Déry U, Masson JY, Richard S. Arginine methylation of MRE11 by PRMT1 is required for DNA damage checkpoint control. Genes Dev 2005; 19 : 671–6. [Google Scholar]
- Lee JH, Paull TT. Direct activation of the ATM protein kinase by the MRE11/Rad50/Nbs1 complex. Science 2004; 304 : 93–6. [Google Scholar]
© 2005 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Méthylation des arginines. Les arginines peuvent être méthylées sur l’azote par les arginines méthyltransférases de type I ou II pour devenir monométhylées. L’ajout d’un deuxième groupement méthyl sur l’azote opposé se fait par l’intermédiare des enzymes de type II et donne une arginine symétriquement diméthylée. En revanche, l’ajout d’un deuxième groupement méthyl sur le même azote par les enzymes de type I produit une arginine asymétriquement diméthylée. Une arginine monométhylée peut aussi être désimidée par la peptidyl arginine désimidase (PAD4) pour devenir une citrulline. |
| Dans le texte | |
 |
Figure 2. Régulation de MRE11 par la méthylation sur les arginines. La méthylation de MRE11 par PRMT1 est requise pour entraîner une diminution de la réplication de l’ADN endommagé ou pour manifester une signalisation des dommages de l’ADN vers les points de régulation du cycle cellulaire afin de permettre la réparation de l’ADN. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




