Figure 2.
Télécharger l'image originale
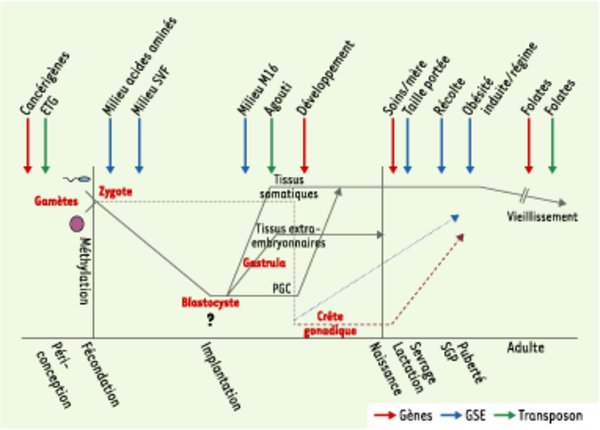
Impact des nutriments ou des interventions nutritionnelles sur la reprogrammation de la méthylation de l’ADN pendant le développement et au cours de la vie. Après la fécondation, les génomes paternel et maternel du zygote subissent une rapide déméthylation au niveau des séquences codantes (gènes) et des séquences répétées (éléments transposables) (ligne pleine), à l’exception des marques épigénétiques des gènes soumis à empreinte et de certaines séquences répétées comme les transposons murins de type IAP (intracisternal A particle), qui semblent aussi réfractaires, dans une certaine mesure, à cette déméthylation. Une méthylation active de novo se met en route après l’implantation, à des degrés variables selon la partie de l’embryon concernée. Après l’implantation, l’ensemble du génome devient hyperméthylé grâce à une intense activité de méthylation de novo, alors que le génome des cellules extra-embryonnaires reste hypométhylé [26]. La méthylation « parent-spécifique » de l’empreinte parentale échappe au processus de déméthylation et de méthylation de novo (ligne brisée). Les empreintes des gènes soumis à empreinte parentale sont effacées avant que les cellules germinales primordiales (PGC) n’atteignent la crête gonadique, remises en place de manière appropriée pendant la gamétogenèse mâle et femelle et achevées pendant la période de croissance lente (SGP), avant la puberté (ligne brisée bleue pour le mâle, ligne pointillée rouge pour la femelle). Chez le mâle, l’acquisition des profils de méthylation commence avant la naissance dans les prospermatogonies et ne s’achève pour de nombreuses séquences qu’après la naissance, avant la fin du stade pachytène de la méiose. Contrairement au mâle, dans les cellules germinales femelles, la plus grande part de la méthylation gamétique se produit après la naissance, pendant la phase de croissance de l’ovocyte après le stade pachytène de la méiose. La SGP est associée à l’apparition du premier pool viable de spermatocytes et à l’initiation de la programmation de la méthylation des empreintes [29, 32]. À chaque stade de cette cascade de fluctuations épigénétiques - aussi bien pendant le développement fœtal qu’au cours de la vie et du vieillissement - l’équilibre nutritionnel doit être « optimal ». L’impact, au niveau de différents types de séquences (gènes et séquences répétées), de régimes alimentaires déséquilibrés ou de certains nutriments chez l’animal - rat, souris, ovins essentiellement - sur les processus de programmation épigénétique au cours de la vie, pendant différentes périodes, avec leur transmission éventuelle d’une génération à l’autre, est aujourd’hui bien mis en évidence [23]. L’impact de différents types de nutriments ou de régimes est indiqué par des flèches, dans la fenêtre au cours de laquelle il a été observé. Ces différents impacts concernent soit des transposons (vert), soit des gènes (rouge), soit des gènes soumis à empreinte parentale (GSE) (bleu). Chaque flèche correspond à une référence citée dans cet article ou dans les références suivantes [14, 23, 33].
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




