| Numéro |
Med Sci (Paris)
Volume 19, Numéro 1, Janvier 2003
|
|
|---|---|---|
| Page(s) | 12 - 14 | |
| Section | Le Magazine : Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/200319112 | |
| Publié en ligne | 15 janvier 2003 | |
Vers de nouvelles cibles thérapeutiques pour les psychoses maniaco-dépressives?
New therapeutic targets in manic-depressive psychosis?
Inserm U.413, Institut Fédératif de Recherches Multidisciplinaires sur les Peptides n° 23, Université de Rouen, 76821 Mont-Saint-Aignan Cedex, France
La psychose maniaco-dépressive encore appelée trouble affectif bipolaire, qui touche 1 % de la population adulte, est caractérisée par une alternance plus ou moins rapide d’épisodes dépressifs et de phases maniaques. Les traitements préconisés visent, d’une part, à diminuer la sévérité des décompensations aiguës par l’administration de neuroleptiques lors des phases maniaques ou d’antidépresseurs lors des épisodes dépressifs, et, d’autre part, à prévenir les récidives par l’administration de thymorégulateurs. Le lithium, l’acide valproïque et la carbamazépine sont les trois principaux thymorégulateurs prescrits lors du traitement prophylactique des psychoses maniaco-dépressives. Bien que l’efficacité clinique de ces psychotropes ne soit plus à démontrer, les mécanismes d’action à l’origine de leurs effets bénéfiques restent controversés. Il est maintenant bien établi que le lithium, en inhibant certaines enzymes impliquées dans le cycle métabolique des phospho-inositides, provoque une déplétion en inositol (Figure 1) [1]. Le lithium est également un inhibiteur de la glycogène synthase kinase-3β, et d’ailleurs la délétion du gène codant pour cette enzyme induit les mêmes effets tératogènes que le lithium, à savoir une dorsalisation de la blastula lors de l’embryogenèse chez le xénope [2]. L’acide valproïque bloque le métabolisme des polyphospho-inositides [3] mais pourrait également agir via l’inhibition de l’histone désacétylase [4] ou la surexpression de Bcl-2 [5]. En menant une étude comparative sur le développement du myxomycète Dictyostelium discoideum et sur la croissance axonale de neurones sensoriels de rats en culture, les équipes d’Adrian Harwood et d’Anne Mudge, de University College à Londres, démontrent que le lithium, l’acide valproïque et la carbamazépine agissent sur une cible commune, le cycle métabolique des phospho-inositides.
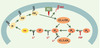 |
Figure 1. Action du lithium et de la prolyl oligopeptidase sur le cycle métabolique des phosphoinositides chez Dictyostelium discoideum. Le lithium [Li+], en inhibant l’activité des inositol polyphosphate phosphatases et de l’inositol monophosphate phosphatase provoque une déplétion en inositol [Ins] qui conduit à une diminution importante de la concentration basale d’inositol (1,4,5)-trisphosphate [I(1,4,5)P3]. La prolyl oligopeptidase (POP) pourrait intervenir dans le métabolisme des phospho-inositides en inhibant la conversion de l’inositol (1,3,4,5,6) pentakisphosphate [IP5] en inositol (1,3,4,5)-tétrakisphosphate [IP4], conduisant à une diminution du taux basal d’I(1,3,4)P3. PI: phosphatidyl inositol; PIP: phosphatidylinositol 4-phosphate; PIP2: phosphatidylinositol (4, 5)-bisphosphate; PLC: phospholipase C; DAG: diacylglycérol. |
Le myxomycète Dictyostelium discoideum est un modèle de choix dans l’étude de l’effet des thymorégulateurs sur le métabolisme de l’inositol dans la mesure où les mécanismes de transduction des signaux chez ce protiste présentent de fortes homologies avec ceux des eucaryotes supérieurs. Lorsque les conditions nutritionnelles sont optimales, Dictyostelium vit sous une forme unicellulaire appelée myxamibe. Lorsque les conditions deviennent défavorables, les myxamibes s’agrègent par chimiotactisme pour former un pseudoplasmode, puis entrent dans une phase de développement marquée par la différenciation d’un appareil fructifère. Les chercheurs londoniens ont montré que le lithium et l’acide valproïque provoquent une diminution de la concentration basale d’inositol trisphosphate (IP3) et bloquent la phase d’agrégation des myxamibes [6, 7]. Le lithium et l’acide valproïque induisent également chez Dictyostelium une surexpression du gène codant pour l’inositol-1-phosphate synthase dont la transcription est réprimée par l’inositol in vivo. Ces données démontrent que le lithium et l’acide valproïque provoquent l’un et l’autre une déplétion en inositol, laquelle engendre une diminution de la concentration basale d’IP3. Ces résultats confortent donc l’hypothèse selon laquelle le cycle des phospho-inositides est situé au coeur du mécanisme d’action des thymorégulateurs. Prenant avantage de l’haploïdie de Dictyostelium, ainsi que de la petite taille de son génome, les chercheurs londoniens ont produit par mutagenèse insertionnelle (technique de restriction enzyme-mediated integration) une lignée cellulaire de Dictyostelium résistante aux effets du lithium et de l’acide valproïque sur la phase d’agrégation cellulaire. L’étude de cette souche a révélé, d’une part, que ces myxamibes présentent des taux d’IP3 supérieurs à ceux des cellules sauvages et, d’autre part, que leur phénotype est dû à l’invalidation du gène codant pour la prolyl oligopeptidase (EC 3.4.21.26, POP), une protéase à sérine qui hydrolyse les peptides du côté C-terminal des résidus proline. De fait, l’inactivation de la POP par invalidation génique ou par l’utilisation d’inhibiteurs sélectifs induit une augmentation des taux d’IP3 consécutive à une déphosphorylation de l’inositol (1,3,4,5,6)-pentakisphosphate (IP5, Figure 1) [7]. Ces résultats démontrent que cette protéase à sérine, de manière tout à fait inattendue, pourrait intervenir dans le cycle des phospho-inositides chez Dictyostelium.
Bien que la fonction physiologique de la POP soit encore mal connue, des études entreprises chez les rongeurs ont montré que cette endopeptidase contribue à l’inactivation des neuropeptides dans le système nerveux central [8]. Parallèlement, divers travaux suggèrent que la POP pourrait être impliquée dans certains troubles de l’humeur. En particulier, il a été montré que l’activité de la POP diminue dans le plasma de patients souffrant de dépression chronique, alors qu’elle augmente chez les patients maniaques [9, 10]. Par ailleurs, les inhibiteurs sélectifs de la POP exercent des actions pro-mnésiques et anti-amnésiques chez les primates et chez l’homme [11, 12]. Or, les patients traités par le lithium se plaignent fréquemment de troubles de la mémoire [13]. L’ensemble de ces données plaide en faveur de l’intervention de la POP dans le mécanisme d’action des thymorégulateurs. De nombreux travaux ont révélé que le lithium et l’acide valproïque provoquent une déplétion en inositol dans les neurones de rat en culture [1, 3]. En revanche, aucune étude n’a permis de montrer que la carbamazépine exerce ce même effet. Afin de vérifier que le cycle métabolique des phospho-inositides constitue effectivement la cible commune des thymorégulateurs, et dans le but de préciser le rôle de la POP dans leur mécanisme d’action, les équipes d’Adrian Harwood et d’Anne Mudge ont étudié les effets du lithium, de l’acide valproïque et de la carbamazépine sur le comportement de neurones sensoriels de rat en culture.
Lors du développement neuritique, les cônes de croissance adoptent un comportement caractéristique marqué par des temps de rétraction totale suivis de phases de développement important, phénomène encore plus prononcé lorsque les neurones sont mis en culture dans un milieu dépourvu en sérum. En enregistrant en temps réel la croissance des neurones sensoriels de rat en culture dans ce type de milieu, les chercheurs britanniques ont observé que l’application de lithium, d’acide valproïque ou de carbamazépine provoque une forte diminution du nombre de cônes de croissance rétractés, ce qui induit une augmentation importante de leur surface moyenne [6]. Ces données constituent la pierre angulaire de leur étude puisqu’elles démontrent qu’en dépit de leurs multiples actions intracellulaires, les trois thymorégulateurs exercent un effet commun sur la croissance neuritique. L’ajout d’inositol au milieu de culture abolit les effets du lithium, de l’acide valproïque et de la carbamazépine sur le nombre et la taille des cônes de croissance, révélant pour la première fois que le cycle des phospho-inositides est la cible commune des thymorégulateurs chez les mammifères [6]. Ces travaux soulignent donc toute la pertinence des stratégies thérapeutiques visant à moduler le métabolisme des phosphatidyl inositols pour le traitement des psychoses maniaco-dépressives. Les chercheurs londoniens ont également observé que l’application d’inhibiteurs sélectifs de la POP abolit l’effet commun du lithium, de l’acide valproïque et de la carbamazépine sur la croissance neuritique des neurones sensoriels de rat, c’est-à-dire sur le nombre de cônes de croissance rétractés, ainsi que sur leur surface moyenne [6]. Ces résultats confortent l’hypothèse selon laquelle la POP est impliquée dans le mécanisme d’action des thymorégulateurs. Compte tenu du rôle important qu’elle semble jouer dans la régulation de la thymie et dans les processus mnésiques, la POP pourrait constituer une nouvelle cible thérapeutique dans le traitement des psychoses maniaco-dépressives.
Références
- Berridge MJ, Downes CP, Hanley MR. Neural and developmental actions of lithium: a unifying hypothesis. Cell 1989; 59: 411–9. [Google Scholar]
- Klein PS, Melton DA. A molecular mechanism for the effect of lithium on development. Proc Natl Acad Sci USA 1996; 93: 8455–9. [Google Scholar]
- O’Donnell T, Rotzinger S, Nakashima TT, Hanstock CC, Ulrich M, Silverstone PH. Chronic lithium and sodium valproate both decrease the concentration of myo-inositol and increase the concentration of inositol monophosphates in rat brain. Brain Res 2000; 880: 84–91. [Google Scholar]
- Phiel CJ, Zhang F, Huang EY, Guenther MG, Lazar MA, Klein PS. Histone deacetylase is a direct target of valproic acid, a potent anticonvulsant, mood stabilizer, and teratogen. J Biol Chem 2001; 276: 36734–41. [Google Scholar]
- Chen G, Zeng WZ, Yuan PX, et al. The mood-stabilizing agents lithium and valproate robustly increase the levels of the neuroprotective protein Bcl-2 in the CNS. J Neurochem 1999; 72: 879–82. [Google Scholar]
- Williams RS, Cheng L, Mudge AW, Harwood AJ. A common mechanism of action for three moodstabilizing drugs. Nature 2002; 417: 292–5. [Google Scholar]
- Williams RS, Eames M, Ryves WJ, Viggars J, Harwood AJ. Loss of a prolyl oligopeptidase confers resistance to lithium by elevation of inositol (1,4,5) trisphosphate. EMBO J 1999; 18: 2734–45. [Google Scholar]
- Toide K, Okamiya K, Iwamoto Y, Kato T. Effect of a novel prolyl endopeptidase inhibitor, JTP-4819, on prolyl endopeptidase activity and substance P- and argininevasopressin- like immunoreactivity in the brains of aged rats. J Neurochem 1995; 65: 234–40. [Google Scholar]
- Maes M, Goossens F, Scharpe S, Meltzer HY, D’Hondt P, Cosyns P. Lower serum prolyl endopeptidase enzyme activity in major depression: further evidence that peptidases play a role in the pathophysiology of depression. Biol Psychiatry 1994; 35: 545–52. [Google Scholar]
- Maes M, Goossens F, Scharpe S, Calabrese J, Desnyder R, Meltzer HY. Alterations in plasma prolyl endopeptidase activity in depression, mania, and schizophrenia: effects of antidepressants, mood stabilizers, and antipsychotic drugs. Psychiatry Res 1995; 58: 217–25. [Google Scholar]
- Schneider JS, Giardiniere M, Morain P. Effects of the prolyl endopeptidase inhibitor S 17092 on cognitive deficits in chronic low dose MPTP-treated monkeys. Neuropsychopharmacology 2002; 26: 176–82. [Google Scholar]
- Morain P, Lestage P, De Nanteuil G, et al. S 17092: a prolyl endopeptidase inhibitor as a potential therapeutic drug for memory impairment. Preclinical and clinical studies. CNS Drug Rev 2002; 8:31–52. [Google Scholar]
- Stip E, Dufresne J, Lussier I, Yatham L. A double-blind, placebo-controlled study of the effects of lithium on cognition in healthy subjects: mild and selective effects on learning. J Affect Disord 2000; 60: 147–57. [Google Scholar]
© 2003 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Action du lithium et de la prolyl oligopeptidase sur le cycle métabolique des phosphoinositides chez Dictyostelium discoideum. Le lithium [Li+], en inhibant l’activité des inositol polyphosphate phosphatases et de l’inositol monophosphate phosphatase provoque une déplétion en inositol [Ins] qui conduit à une diminution importante de la concentration basale d’inositol (1,4,5)-trisphosphate [I(1,4,5)P3]. La prolyl oligopeptidase (POP) pourrait intervenir dans le métabolisme des phospho-inositides en inhibant la conversion de l’inositol (1,3,4,5,6) pentakisphosphate [IP5] en inositol (1,3,4,5)-tétrakisphosphate [IP4], conduisant à une diminution du taux basal d’I(1,3,4)P3. PI: phosphatidyl inositol; PIP: phosphatidylinositol 4-phosphate; PIP2: phosphatidylinositol (4, 5)-bisphosphate; PLC: phospholipase C; DAG: diacylglycérol. |
| Dans le texte | |
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.




