| Issue |
Med Sci (Paris)
Volume 18, Number 12, Décembre 2002
|
|
|---|---|---|
| Page(s) | 1200 - 1201 | |
| Section | Le Magazine : Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/200218121200 | |
| Published online | 15 décembre 2002 | |
Les chaperons de l’évolution
Evolution’ chaperons
Inserm U.490, Toxicologie Moléculaire, Faculté de médecine, 45, rue des Saints-Pères 75270 Paris Cedex 06, France
L’évolution impose aux organismes de concilier deux nécessités apparemment contradictoires. D’une part, ils doivent assurer leur développement et leur adaptation aux conditions habituelles de leur environnement ; d’autre part, ils doivent avoir la capacité de s’adapter à des modifications de cet environnement faute de quoi la survie de l’espèce serait menacée. Cette adaptation s’accompagne de modifications profondes de fonctions essentielles, et d’altérations génétiques. Cependant, l’accumulation de mutations et de modifications fonctionnelles en période de « calme environnemental » a nécessairement un coût qui peut s’avérer trop lourd pour le développement normal et harmonieux de l’organisme. Plusieurs théories ont tenté de résoudre ce paradoxe. Parmi elles, celle de Waddington, se fondant sur la notion de « canalisation », propose que les organismes disposent d’un moyen de « tamponner » les mutations accumulées au cours de l’évolution pour les empêcher de s’exprimer [1]. En cas de stress environnemental, ce « tampon » serait inactivé permettant l’expression rapide de nouveaux phénotypes dont certains seraient à même d’améliorer la survie dans de nouvelles conditions. Ces traits génétiques seraient ensuite assimilés et fixés dans la descendance.
Une fois cette hypothèse posée, encore fallait-il identifier en termes moléculaires ce système tampon. Les travaux récents de l’équipe de Lindquist chez la plante Arabidopsis thaliana, faisant suite à des travaux plus anciens chez la drosophile, proposent que la protéine de choc thermique Hsp90 pourrait constituer un des chaînons de ce système de tampon génétique [2, 3]. Il n’était pas illogique de considérer les nombreuses protéines de choc thermique comme de bons candidats pour cette fonction. Ces protéines exercent avant tout un rôle de chaperon moléculaire [4] ; elles se lient à des protéines en cours de synthèse, ou à des protéines partiellement dénaturées, soit pour catalyser leur maturation conformationnelle, soit pour les empêcher de s’agréger et d’induire une toxicité cellulaire, soit enfin pour les orienter vers la voie de dégradation quand la situation est franchement compromise. La régulation de l’expression de ces protéines chaperons est en accord avec leurs fonctions puisqu’elle est induite par différents stress cellulaires susceptibles de dénaturer les protéines, en particulier le stress thermique. La protéine chaperon Hsp90 exerce aussi une fonction légèrement différente puisqu’elle fait partie de complexes macromoléculaires avec des protéines de signalisation essentielles comme les récepteurs nucléaires et les protéine kinases [5]. Elle confère à ces facteurs de signalisation des fonctions cellulaires particulières, par exemple une affinité élevée pour un ligand ou une inhibition de leur dimérisation.
Les expériences du groupe de Lindquist permettent d’attribuer à la protéine Hsp90 une fonction supplémentaire, une sorte de pouvoir tampon atténuant les conséquences fonctionnelles de l’accumulation de mutations. Que ce soit chez la drosophile ou chez Arabidopsis, l’approche a consisté à inhiber les fonctions de Hsp90 soit par des moyens pharmacologiques, soit par des techniques génétiques, disponibles dans ces espèces. La geldanamycine est l’inhibiteur le plus classique et le plus utilisé. L’approche pharmacologique présente l’avantage d’inhiber l’ensemble des isoformes de la protéine Hsp90, sachant que la plante Arabidopsis comprend sept gènes codant pour cette protéine ; cette approche est en revanche moins spécifique, ce qui a conduit les auteurs à tester les effets de l’invalidation des gènes dans les deux espèces. Chez la drosophile, l’inactivation ou l’invalidation de Hsp90 conduit à l’apparition d’un nombre important de variants différents, chacun présentant un phénotype profondément modifié, en particulier dans les processus de développement et de morphogenèse [3]. Ces altérations, variables selon le fond génétique, étaient finalement « assimilées » par les souches variantes puisqu’elles persistaient après la restauration d’un niveau normal d’Hsp90. Ces résultats avaient conduit les auteurs à proposer un rôle essentiel pour ce chaperon dans les mécanismes de l’évolution.
Le même type d’expériences a été conduit chez Arabidopsis thaliana [2]. Dans ce cas aussi, l’inactivation de Hsp90 a conduit à l’apparition de variants multiples, en particulier des variants morphologiques. En particulier, certaines souches présentent des feuilles de couleur différente ou des cotylédons et des racines aux formes modifiées. Par rapport à ce qui a été observé chez la drosophile, les phénotypes variants chez la plante sont plus modérés et n’empêchent en rien le développement de celle-ci. Il est, bien entendu, difficile de comparer des organismes si différents, mais les observations chez Arabidopsis thaliana semblent plus en accord avec l’hypothèse d’un rôle tampon de Hsp90 au cours de l’évolution, dans la mesure où les variants apparus sont plus compatibles avec la survie globale de l’organisme.
Un autre argument en faveur du rôle des protéines de choc thermique dans les processus d’évolution provient de l’étude des conséquences sur le développement d’un choc thermique. En effet, l’exposition des organismes à un choc thermique provoque l’apparition de variants morphologiques semblables à ceux qu’induit l’inactivation de la protéine Hsp90. Ces observations vont dans le sens d’un rôle éminent de Hsp90 dans ces processus, même si la participation des autres protéines de choc thermique n’est pas à exclure.
Cette série d’expériences conduit à une hypothèse de travail que les travaux futurs devront tester (Figure 1). Les organismes accumulent, selon un rythme qui leur est propre, un nombre croissant de mutations. Certaines de ces mutations, qui auraient pu se traduire fonctionnellement, demeurent néanmoins silencieuses en raison de l’interaction de la protéine variante avec Hsp90, interaction qui permet le maintien de la conformation ou de la fonction d’origine. Des mutations multiples et différentes peuvent ainsi s’accumuler sans conséquences fonctionnelles notables. En cas de stress environnemental, la protéine de choc thermique est déviée de cette fonction pour assurer son rôle protecteur classique à l’égard de l’ensemble des autres protéines. Elle révèle ainsi de nouvelles fonctions jusqu’alors silencieuses des variants préexistants. Elle facilite ainsi l’adaptation de l’organisme à son nouvel environnement. Cela n’empêche pas l’apparition de nouvelles mutations qui permettraient une meilleure adaptation, mais l’originalité de cette proposition est qu’un ensemble de variants est déjà présent au moment du stress. On serait tenté de généraliser ce rôle des protéines chaperons à d’autres espèces, mais les phénomènes d’adaptation peuvent varier selon les espèces et il est beaucoup trop tôt pour aboutir à cette conclusion. Néanmoins, il est assez tentant de considérer que nous avons tous besoin d’un chaperon pour notre propre évolution.
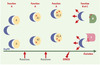 |
Figure 1. Schéma hypothétique de la fonction tampon de Hsp90 au cours de l’évolution. Un certain nombre de protéines (A) interagissent avec les Hsp90. Lorsque des mutations apparaissent au cours de l’évolution, la liaison à la protéine chaperon permet de maintenir la conformation et la fonction A de cette protéine. Ainsi, différents variants (A1; A2; A1,3; A1,4) existent et possèdent la même fonction. À l’occasion d’un stress environnemental, Hsp90 est déviée de ces interactions et libère les variants qui, en retrouvant des conformations différentes, acquièrent de nouvelles fonctions (B ou C) qui pourraient faciliter l’adaptation aux nouvelles conditions. Le modèle est aussi valable si seules les formes variantes de A interagissent avec Hsp90. |
Références
- Waddington CH. Nature 1942; 150: 563. [Google Scholar]
- Queitsch C, Sangster S, Lindquist S. Hsp90 as a capacitor of phenotypic variation. Nature 2002; 417: 618–24. [Google Scholar]
- Rutherford SL, Lindquist S. Hsp90 as a capacitor for morphological evolution. Nature 1998; 396: 336–42. [Google Scholar]
- Morange M. Protéines chaperons. Med Sci 2000; 16: 630–4 [Google Scholar]
- Buschner J. Hsp90 and Co: a holding for folding. Trends Biochem Sci 1999; 24: 136–41. [Google Scholar]
© 2002 médecine/sciences - Inserm / SRMS
Liste des figures
 |
Figure 1. Schéma hypothétique de la fonction tampon de Hsp90 au cours de l’évolution. Un certain nombre de protéines (A) interagissent avec les Hsp90. Lorsque des mutations apparaissent au cours de l’évolution, la liaison à la protéine chaperon permet de maintenir la conformation et la fonction A de cette protéine. Ainsi, différents variants (A1; A2; A1,3; A1,4) existent et possèdent la même fonction. À l’occasion d’un stress environnemental, Hsp90 est déviée de ces interactions et libère les variants qui, en retrouvant des conformations différentes, acquièrent de nouvelles fonctions (B ou C) qui pourraient faciliter l’adaptation aux nouvelles conditions. Le modèle est aussi valable si seules les formes variantes de A interagissent avec Hsp90. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




