| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
|
|
|---|---|---|
| Page(s) | 248 - 250 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026029 | |
| Published online | 20 mars 2026 | |
Les macrophages métallophiles de la zone marginale de la rate
Des sentinelles pour stimuler l’immunité antitumorale impliquant les lymphocytes T CD8+
Metallophilic macrophages of the splenic marginal zone: myeloid sentinels capable of cross-priming CD8+ T cell antitumor immunity
1
Université Paris Cité, Inserm, UMR1141, NeuroDiderot, Paris, France
2
Service de physiologie - explorations fonctionnelles pédiatriques, APHP, Hôpital universitaire Robert-Debré, Paris, France
3
Université Paris Cité, Inserm, CNRS U1151, Institut Necker-Enfants malades, Paris, France
4
Service d’immunologie biologique, APHP, Hôpital universitaire Necker-Enfants malades, Paris, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Les macrophages métallophiles de la zone marginale de la rate occupent une position stratégique unique à l’interface entre la pulpe blanche et les capillaires sinusoïdes. Ces cellules myéloïdes, caractérisées par une forte expression de la molécule CD169, forment une barrière de première ligne capable d’intercepter et de capturer les microorganismes pathogènes ainsi que les débris cellulaires et matériels tumoraux circulant dans le sang [1]. Leur rôle dans l’immunité innée est connu : ils contrôlent la dissémination d’infections généralisées fatales en piégeant virus, bactéries et parasites [2, 3]. Ils participent également à l’immunité adaptative en activant les réponses humorales des lymphocytes B [1], en présentant des antigènes lipidiques aux lymphocytes T natural killer invariants [1], et en activant les réponses des lymphocytes T CD8+ contre les virus qui les infectent directement [4]. Cependant, leur capacité à initier des réponses immunitaires adaptatives contre les tumeurs restait controversée. Les modèles actuels suggèrent que les macrophages CD169+ de la rate transfèrent les antigènes (tumoraux ou autres) aux cellules dendritiques conventionnelles de type 1 (spécialisées dans la présentation croisée des antigènes1) pour activer les lymphocytes T CD8+ [5]. Ce scénario contraste avec celui proposé pour les macrophages CD169+ des sinus sous-capsulaires des ganglions lymphatiques, qui occupent dans ces ganglions une position semblable à celle des macrophages métallophiles de la zone marginale de la rate et qui sont capables d’activer directement les réponses des lymphocytes T CD8+ par l’internalisation de cellules tumorales et la présentation croisée d’antigènes issus de leur dégradation [6]. Or, nous avons récemment montré que les macrophages métallophiles de la zone marginale de la rate ont également la capacité d’activer directement les réponses antitumorales protectrices des lymphocytes T CD8+, indépendamment des cellules dendritiques de type 1 [7].
La difficulté d’isoler les macrophages métallophiles de la rate a représenté un obstacle majeur à leur étude : ces cellules sont rares, fragiles, et intégrées dans un réseau tissulaire complexe incluant des fibroblastes et d’autres cellules immunitaires [8]. Grâce à un protocole innovant combinant digestion enzymatique, gradients de densité et tri par cytométrie en flux, nous sommes parvenus à isoler ces macrophages avec un degré de pureté supérieur à 95 %, confirmé par une analyse transcriptomique sur cellules individuelles. Cette analyse a révélé un profil d’expression génique différent de celui des autres macrophages résidant dans les tissus, enrichi en transcrits codant des protéines impliquées dans la signalisation des interférons de type I et dans l’activation des lymphocytes T. Étonnamment, les macrophages métallophiles de la zone marginale de la rate expriment préférentiellement des gènes associés à la présentation croisée d’antigènes, impliquant le complexe majeur d’histocompatibilité de classe I, plutôt que des gènes associés à la présentation « classique » d’antigènes, impliquant le complexe d’histocompatibilité de classe II. Par des expériences in vitro, nous avons montré que ces macrophages égalent, voire surpassent les cellules dendritiques de type 1 dans leur capacité à présenter une large gamme d’antigènes solubles et particulaires aux lymphocytes T CD8+ naïfs. Contrairement aux cellules dendritiques de type 1, qui utilisent la voie cytosolique dépendante du protéasome pour la présentation croisée des antigènes, ces macrophages utilisent une voie « vacuolaire » distincte impliquant les protéases des endolysosomes, notamment les cathepsines, et indépendante du protéasome (Figure 1). L’utilisation de la microscopie biphotonique in vivo et de la microscopie à feuillets de lumière ex vivo a permis de visualiser directement les interactions physiques entre ces macrophages et les lymphocytes T CD8+ dans la rate. Après ciblage d’antigènes vers ces macrophages, à l’aide d’anticorps permettant l’internalisation des protéines antigéniques par le récepteur CD169, nous avons constaté que des lymphocytes T CD8+ qui se différencient en cellules effectrices capables de tuer des cellules tumorales in situ formaient des contacts prolongés avec ces macrophages de la zone marginale, mais pas avec les cellules dendritiques de type 1.
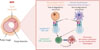 |
Figure 1 La présentation croisée d’antigènes aux lymphocytes T CD8+ par les macrophages métallophiles CD169+ de la zone marginale de la rate contribue à l’immunosurveillance des tumeurs. Les macrophages métallophiles CD169+ de la zone marginale splénique (en orange) capturent les antigènes tumoraux circulant dans le sang ou envahissant la rate et les présentent directement aux lymphocytes T CD8+ naïfs (en bleu) via les molécules du complexe majeur d’histocompatibilité de classe I (CMH-I). Cette présentation croisée des antigènes utilise une voie de traitement « vacuolaire » dépendant des cathepsines et indépendante du protéasome, différente de la voie de dégradation cytosolique classique des cellules dendritiques conventionnelles de type 1. L’activation directe des lymphocytes T CD8+ par ces macrophages ne nécessite pas la coopération des cellules dendritiques conventionnelles de type 1, et conduit à des réponses cytotoxiques protectrices contre les tumeurs. Cette voie alternative de présentation croisée des antigènes ouvre de nouvelles perspectives pour l’immunothérapie antitumorale, en ciblant spécifiquement ces macrophages qui ont une position stratégique pour drainer les antigènes tumoraux présents dans le sang. Figure réalisée avec BioRender. |
Étonnamment, l’efficacité de la présentation croisée des antigènes par ces macrophages dépend de la présence du facteur de transcription BATF3 (basic leucine zipper ATF-like transcription factor 3), qui est également requis pour le développement et l’activité des cellules dendritiques de type 1 [9]. En l’absence de BATF3, les macrophages métallophiles de la zone marginale ont une capacité réduite à induire des réponses antitumorales in vivo, et leur analyse transcriptomique révèle une diminution de l’expression de gènes impliqués dans la présentation croisée d’antigènes et dans l’activation des lymphocytes.
Des expériences utilisant des modèles murins de mélanome métastatique (par transplantation de la lignée cellulaire B16-F10) et de leucémie aigüe myéloblastique (par transplantation de la lignée cellulaire C1498) surexprimant l’ovalbumine comme antigène tumoral modèle ont montré que ces macrophages spléniques peuvent protéger contre les métastases pulmonaires de mélanome ou induire le rejet d’une leucémie envahissant la rate, même en l’absence constitutive de cellules dendritiques de type 1 (Figure 1), ce qui implique, respectivement, la capture d’antigènes tumoraux circulant dans le sang ou l’internalisation directe de cellules tumorales colonisant la rate. L’utilisation de souris Xcr1-DTA, entièrement dépourvues de cellules dendritiques de type 1, a confirmé que l’activation des lymphocytes T CD8+ cytotoxiques antitumoraux par ces macrophages est totalement indépendante des cellules dendritiques de type 1. Cela permet de réfuter définitivement l’hypothèse, jusqu’alors communément acceptée, de la nécessité d’un transfert d’antigènes, ou de complexes moléculaires associant molécules du complexe majeur d’histocompatibilité de classe I et peptides antigéniques (MHC cross-dressing), vers ces cellules [10].
Ces résultats révolutionnent notre compréhension de la fonction immunitaire de la rate en montrant que les macrophages métallophiles de la zone marginale sont des acteurs majeurs de l’immunité antitumorale. Leur position stratégique et leurs capacités uniques de présentation croisée d’antigènes tumoraux (Figure 1) en font des cibles thérapeutiques prometteuses pour le développement de vaccins antitumoraux ou l’immunothérapie. La découverte que ces macrophages utilisent une voie vacuolaire distincte pour la présentation croisée d’antigènes (Figure 1) ouvre également de nouvelles perspectives de recherche concernant la diversité des mécanismes de présentation antigénique, avec de possibles applications pour optimiser les stratégies d’immunisation en médecine préventive. Enfin, la découverte de l’expression du gène codant BATF3 par ces macrophages de la rate s’inscrit dans la grande plasticité fonctionnelle des macrophages tissulaires, et remet en question les frontières traditionnelles entre le rôle des macrophages et celui des cellules dendritiques dans la mise en œuvre des réponses immunitaires adaptatives.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
Références
- Martinez-Pomares L, Gordon S. CD169+ macrophages at the crossroads of antigen presentation. Trends Immunol 2012 ; 33 : 66–70. [Google Scholar]
- Honke N, Shaabani N, Cadeddu G, et al. Enforced viral replication activates adaptive immunity and is essential for the control of a cytopathic virus. Nat Immunol 2011 ; 13 : 51–7. [Google Scholar]
- Perez OA, Yeung ST, Vera-Licona P, et al. CD169+ macrophages orchestrate innate immune responses by regulating bacterial localization in the spleen. Sci Immunol 2017 ; 2 : eaah5520. [Google Scholar]
- Bernhard CA, Ried C, Kochanek S, et al. CD169+ macrophages are sufficient for priming of CTLs with specificities left out by cross-priming dendritic cells. Proc Natl Acad Sci USA 2015 ; 112 : 5461–6. [Google Scholar]
- Grabowska J, Lopez-Venegas MA, Affandi AJ, et al. CD169+ macrophages capture and dendritic cells instruct: the interplay of the gatekeeper and the general of the immune system. Front Immunol 2018 ; 9 : 2472. [Google Scholar]
- Asano K, Nabeyama A, Miyake Y, et al. CD169-positive macrophages dominate antitumor immunity by crosspresenting dead cell-associated antigens. Immunity 2011 ; 34 : 85–95. [Google Scholar]
- Mauvais F-X, Hamel Y, Silvin A, et al. Metallophilic marginal zone macrophages cross-prime CD8+ T cell-mediated protective immunity against blood-borne tumors. Immunity 2025 ; 58 : 843–60.e20. [Google Scholar]
- Gray EE, Friend S, Suzuki K, et al. Subcapsular sinus macrophage fragmentation and CD169+ bleb acquisition by closely associated IL-17-committed innate-like lymphocytes. PLoS One 2012 ; 7 : e38258. [Google Scholar]
- Hildner K, Edelson BT, Purtha WE, et al. Batf3 deficiency reveals a critical role for CD8a+ dendritic cells in cytotoxic T cell immunity. Science 2008 ; 322 : 1097–100. [Google Scholar]
- MacNabb BW, Kline J. MHC cross-dressing in antigen presentation. Adv Immunol 2023 ; 159 : 115–47. [Google Scholar]
Processus par lequel des cellules présentatrices d’antigène internalisent des antigènes exogènes et les présentent aux lymphocytes T CD8+ sur des molécules du complexe majeur d’histocompatibilité de classe I. Ce mécanisme permet l’activation de lymphocytes T CD8+ cytotoxiques contre des antigènes tumoraux, viraux sans infection directe de la cellule présentatrice, ou du soi. Il joue un rôle crucial dans l’immunosurveillance antitumorale et antivirale et dans le maintien de la tolérance au soi.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 La présentation croisée d’antigènes aux lymphocytes T CD8+ par les macrophages métallophiles CD169+ de la zone marginale de la rate contribue à l’immunosurveillance des tumeurs. Les macrophages métallophiles CD169+ de la zone marginale splénique (en orange) capturent les antigènes tumoraux circulant dans le sang ou envahissant la rate et les présentent directement aux lymphocytes T CD8+ naïfs (en bleu) via les molécules du complexe majeur d’histocompatibilité de classe I (CMH-I). Cette présentation croisée des antigènes utilise une voie de traitement « vacuolaire » dépendant des cathepsines et indépendante du protéasome, différente de la voie de dégradation cytosolique classique des cellules dendritiques conventionnelles de type 1. L’activation directe des lymphocytes T CD8+ par ces macrophages ne nécessite pas la coopération des cellules dendritiques conventionnelles de type 1, et conduit à des réponses cytotoxiques protectrices contre les tumeurs. Cette voie alternative de présentation croisée des antigènes ouvre de nouvelles perspectives pour l’immunothérapie antitumorale, en ciblant spécifiquement ces macrophages qui ont une position stratégique pour drainer les antigènes tumoraux présents dans le sang. Figure réalisée avec BioRender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




