Figure 1
Télécharger l'image originale
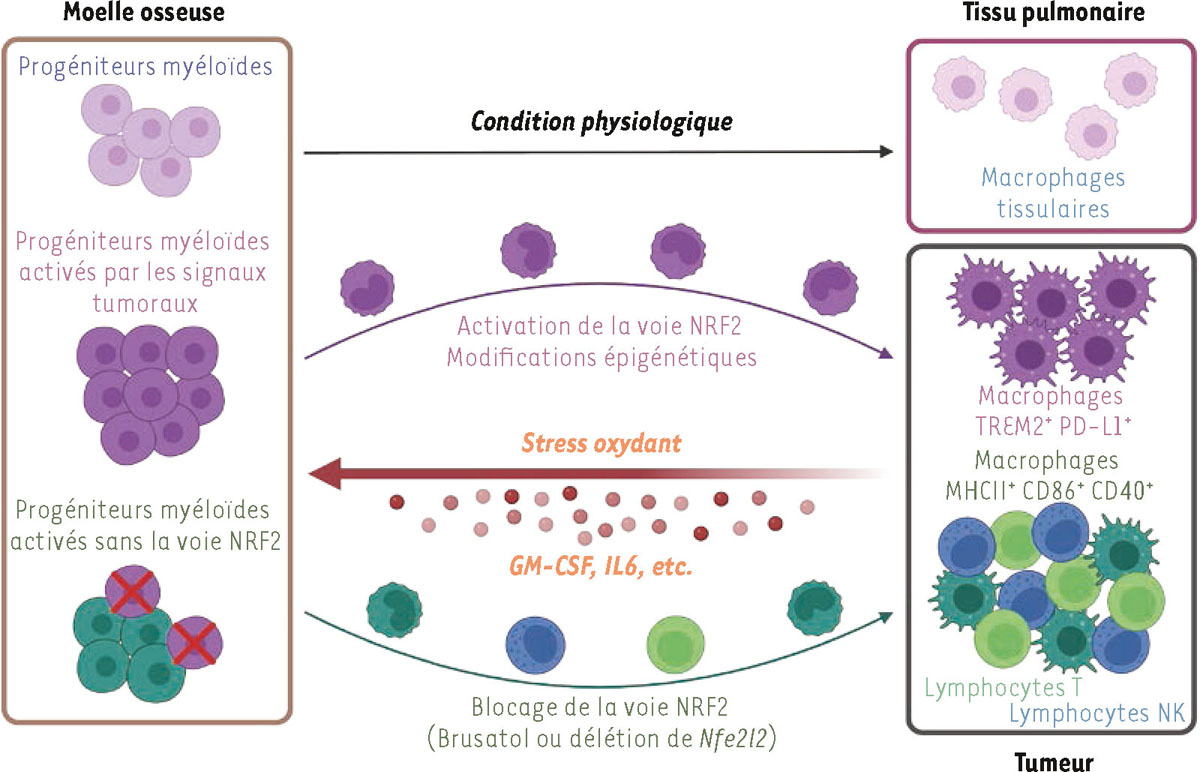
L’activation de NRF2 dans les progéniteurs myéloïdes par des signaux tumoraux conditionne la différenciation des macrophages et module l’immunité antitumorale. Dans des conditions physiologiques (flèche noire, en haut), les progéniteurs myéloïdes contribuent au renouvellement des macrophages tissulaires résidents (en rose). En présence de signaux tumoraux, tels que GM-CSF (granulocyte-macrophage colony stimulating factor) et IL-6 (interleukine-6), et de facteurs de stress oxydant, l’activation des progéniteurs médullaires est profondément modifiée (flèche rouge). En réponse à ces signaux (flèche violette), les progéniteurs activent la voie NRF2 et acquièrent des marques épigénétiques qui orientent leur différenciation vers des macrophages immunosuppresseurs TREM2+ PD-L1+ (en violet), limitant l’infiltration des lymphocytes T et NK cytotoxiques. Le blocage de NRF2, pharmacologique (brusatol) ou génétique (délétion de Nfe2l2), restreint cette polarisation immunosuppressive et favorise l’émergence de macrophages pro-inflammatoires MHCII+ CD86+ CD40+ (en vert foncé), associée à un recrutement accru de lymphocytes T CD8+ et de lymphocytes NK (en vert/bleu). Figure réalisée avec BioRender.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




