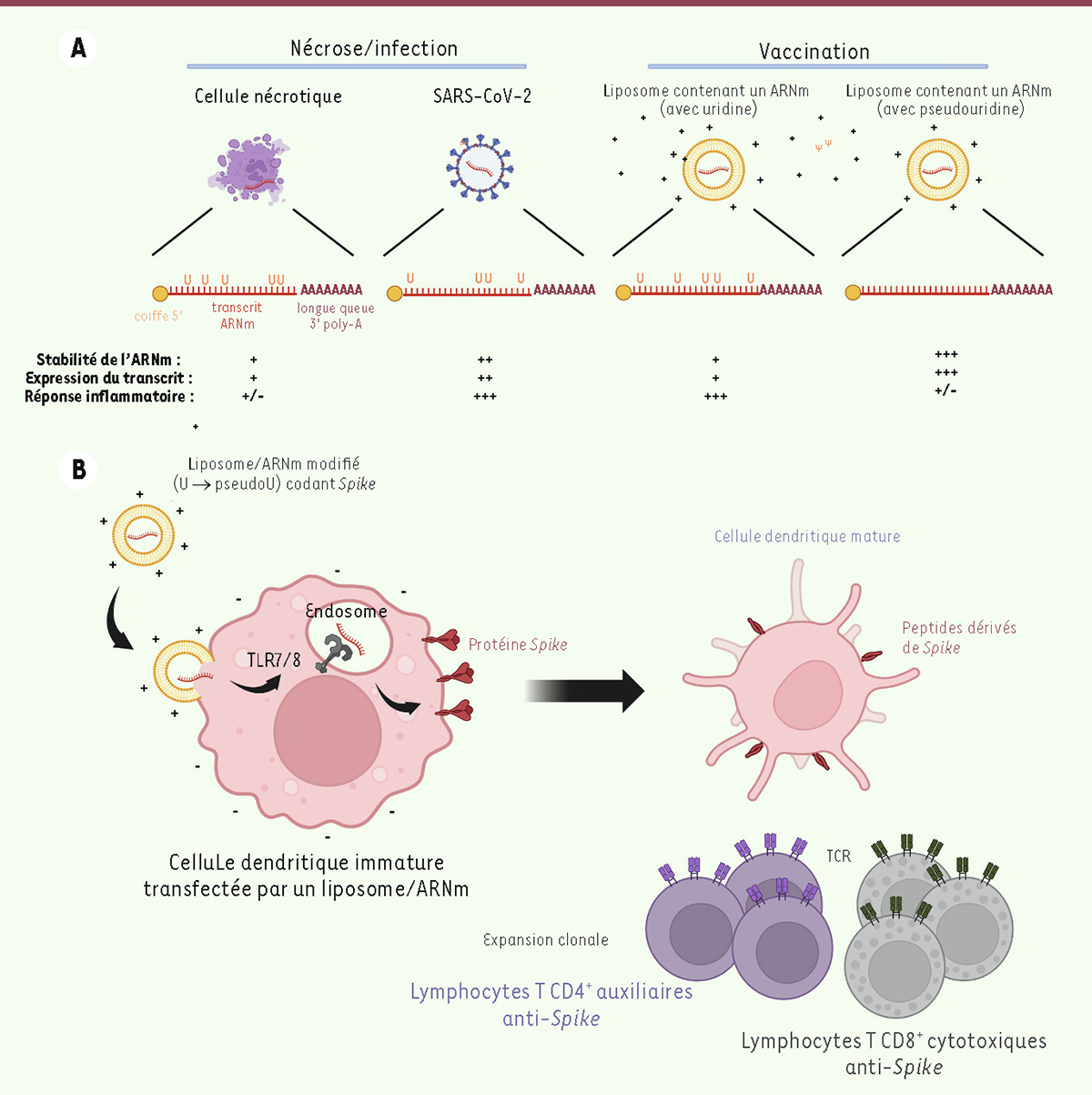
Figure 1.
Télécharger l'image originale
Utilisation d’ARNm modifiés encapsulés dans des liposomes à des fins vaccinales. (A) Les ARNm provenant de cellules eucaryotes nécrotiques sont peu stables, présents en faibles quantités, peu immunogènes et peu inflammatoires, mais capables d’induire la production d’IL-12 et d’IFN-a par les cellules dendritiques [22]. Les ARNm d’origine virale (par exemple des ARNm du SARS-CoV-2) peuvent contenir des pseudouridines (y) à la place d’uridines (u). L’infection par des virus comme le SARS-CoV-2 provoque cependant une réaction inflammatoire qui peut être très sévère chez certains patients. Les travaux de Katalin Karikó et Drew Weissman ont démontré que lorsqu’un ARNm codant une des protéines d’un virus est modifié en introduisant des pseudouridines à la place d’uridines dans sa séquence, puis encapsidé dans un liposome, la production de protéines pro-inflammatoires est diminuée, tandis que sa traduction en protéine est accrue, en raison notamment de sa plus grande stabilité, comparativement au même ARN non modifié contenant seulement des uridines. (B) Des liposomes contenant un ARNm modifié transcrit in vitro, contenant des pseudouridines, codant la protéine Spike du SARS-CoV-2, fusionnent avec la membrane de cellules dendritiques immatures. Ils libèrent dans les endosomes l’ARNm modifié simple brin qui se fixe aux TLR7/8 (des ARNm double brin potentiellement encore présents après purification des ARNm simple brin peuvent se lier au TLR3 et donner un signal d’activation [22]). Cela conduit d’une part à une faible réaction inflammatoire du fait de la présence des pseudouridines et, d’autre part, à la maturation des cellules dendritiques, qui deviennent capables d’apprêter la protéine Spike traduite en quantités importantes à partir de l’ARN modifié transfecté (du fait de la présence des pseudouridines et de la longueur de la queue poly-A de cet ARNm). Cet apprêtement conduit à la présentation de peptides dérivés de spike par des molécules du CMH-I et CMH-II aux lymphocytes T CD8+ et CD4+, respectivement, et à la prolifération et différenciation de ces lymphocytes en cellules effectrices auxiliaires (qui vont notamment aider à la production d’anticorps neutralisant Spike) et cytotoxiques dirigées contre les cellules infectées par le virus. Certaines de ces cellules (lymphocytes T et B) ainsi stimulées vont devenir des cellules mémoires, prêtes à s’activer en cas de nouvelles infections par le virus SARS-CoV-2 ou certains de ses variants. TCR : T cell receptor (récepteur T de l’antigène) ; TLR7/8 : récepteurs Toll-like 7 et 8 (figure créée sur biorender.com).
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




