Figure 2.
Télécharger l'image originale
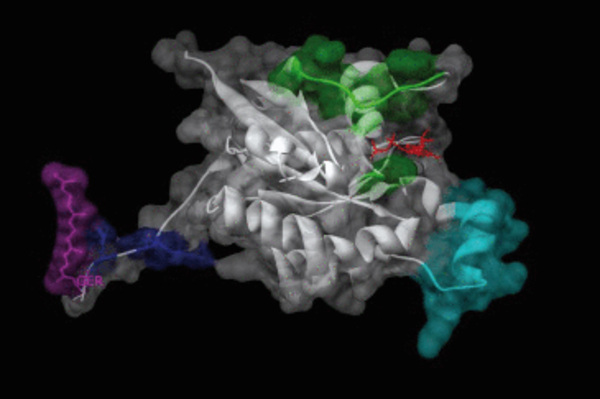
Caractéristiques structurales des GTPases de la famille Rho. Chaque membre de la famille comporte une séquence « insert » de 12 acides aminés située entre le 5e feuillet β et la 4e hélice α du domaine GTPase (cyan). Le positionnement des régions Switch I et Switch II (vert) est dépendant de la nature du guanosine (rouge) lié par la GTPase. La majorité des GTPases Rho sont des commutateurs moléculaires existant sous deux états, liant de façon spécifique leurs partenaires d’interaction selon qu’ils soient associés au guanosine-diphosphate (GDP) ou au guanosine-triphosphate (GTP). Le rythme d’échange du GDP pour un GTP est accéléré par des facteurs d’échange de guanines (GEF) qui rendent les GTPases aptes à lier plus efficacement leurs effecteurs. En contrepartie, les GTPases pallient leur capacité enzymatique réduite à hydrolyser le GTP en GDP par l’assistance entre autre d’une arginine spécifique trouvée dans le site de liaison de protéines activatrices de GTPases (GAP). À l’exception de RhoBTB 1 et 2, le domaine G comporte une modification lipidique à son extrémité carboxylée (magenta) précédée de résidus à chaîne latérale basique (bleu). La modification lipidique ne garantit pas la présence des GTPases dans la membrane. Les GTPases Rho se trouvent généralement séquestrées dans le cytoplasme par des inhibiteurs de la dissociation du GDP (GDI) qui dissimulent notamment la chaîne lipidique des GTPases. Dans le cas présent, Cdc42 lie le GDP et adopte une conformation lui permettant de lier RhoGDI (Protein Data Bank 1DOA) (image réalisée avec UCSF Chimera).
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




