Figure 1.
Télécharger l'image originale
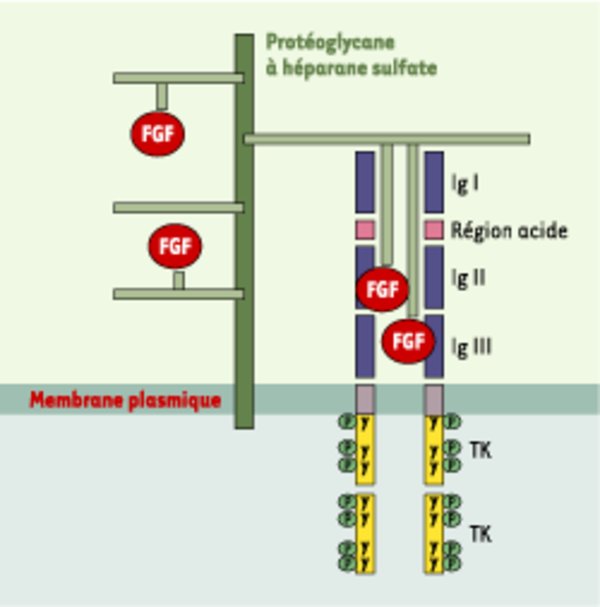
Activation de FGFR1 par ses ligands FGF en présence de protéoglycanes à héparane sulfate. FGFR1 est un récepteur membranaire actif sous forme de dimère, les monomères étant inactifs. La région extracellulaire, qui fixe le ligand FGF, comporte trois domaines de type immunoglobuline (IgI, IgII et IgIII). Entre les deux premiers s’intercale un module très riche en résidus acides (région acide), dont le rôle serait d’empêcher l’activation spontanée du récepteur en l’absence de son ligand [33]. La région intracellulaire comprend deux domaines à activité tyrosine kinase (TK). La formation d’un complexe moléculaire tripartite entre FGF, FGFR et la chaîne héparane sulfate d’un protéoglycanne est nécessaire à la dimérisation du récepteur, qui est suivie de son activation par autophosphorylation (P) de résidus tyrosine (Y) dans la région intracellulaire de la molécule. Les phosphotyrosines stimulent en retour l’activité tyrosine kinase du récepteur ou servent de points d’ancrage à des molécules de la cascade de signalisation.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




