| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
Organoïdes
|
|
|---|---|---|
| Page(s) | 270 - 279 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2026035 | |
| Published online | 20 mars 2026 | |
Organoïdes hépatiques
De la promesse à la complexité fonctionnelle
Liver organoids: from promise to functional complexity
Inserm, Université Paris-Saclay, UMRS1193, Villejuif, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Les progrès récents en biologie des cellules souches et en ingénierie tissulaire ont profondément renouvelé le champ des organoïdes hépatiques. Devenus plus matures et plus complexes, ils intègrent désormais des réseaux canaliculaires fonctionnels, des gradients métaboliques, ainsi que des cocultures associant cholangiocytes, cellules étoilées et macrophages. Les avancées en vascularisation, en bio-impression et en microfluidique améliorent leur stabilité et leur fonctionnalité, renforçant leur utilité pour la modélisation des maladies, la pharmacologie, la médecine personnalisée et de futures applications thérapeutiques.
Abstract
Recent advances in stem cell biology and tissue engineering have profoundly renewed the field of liver organoids. More mature and complex, they now incorporate functional canalicular networks, metabolic gradients, and co-cultures including cholangiocytes, stellate cells, and macrophages. Advances in vascularization, bioprinting, and microfluidics are improving their stability and functionality, thereby enhancing their usefulness for disease modeling, pharmacology, personalized medicine, and future therapeutic applications.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Vignette (© Eléanor Luce).
Le foie est un organe central du métabolisme, impliqué dans l’homéostasie énergétique, la détoxification et la production de bile. Sa complexité repose sur l’agencement des hépatocytes, des cholangiocytes1, des cellules étoilées2, des macrophages résidents et des réseaux vasculaires qui assurent ses multiples fonctions. Reproduire cette organisation in vitro a longtemps représenté un défi majeur, mais les progrès récents de la biologie des cellules souches et de l’ingénierie tissulaire ont ouvert la voie au développement d’organoïdes hépatiques [1] (→).
(→) Voir m/s n° 10, 2021, page 902
Les organoïdes hépatiques, dérivés de cellules souches pluripotentes ou de tissus adultes, constituent aujourd’hui l’une des innovations les plus marquantes de la biologie et de la médecine régénérative, offrant un modèle de plus en plus fidèle pour étudier le développement, la physiopathologie ainsi que pour tester de nouvelles approches thérapeutiques. En quelques années, ces structures tridimensionnelles, capables de reproduire certaines fonctions d’un tissu complexe comme le foie, ont transformé la recherche fondamentale et préclinique. En effet, des stratégies inspirées du développement embryonnaire, telles que l’utilisation de facteurs placentaires, ont permis d’améliorer la croissance et la robustesse des cultures. Parallèlement, la maturation fonctionnelle s’est enrichie grâce à une intégration progressive de voies métaboliques complexes, rapprochant les organoïdes de l’identité d’un foie adulte. La reconstitution d’une zonation lobulaire, l’apport de cocultures multicellulaires et les premiers succès de vascularisation partielle ont contribué à accroître leur pertinence biologique. Ces avancées placent désormais les organoïdes hépatiques à la frontière de la recherche translationnelle, avec des perspectives allant de la modélisation des maladies à la transplantation expérimentale.
Nouvelles avancées dans la croissance et la maturation fonctionnelle des organoïdes hépatiques
Facteurs de croissance et voies métaboliques
La question de la croissance et de la maturation des organoïdes hépatiques a longtemps constitué un obstacle majeur pour leur utilisation en recherche comme en clinique. En effet, la production d’organoïdes à grande échelle demeure un défi dans la perspective d’une utilisation clinique, et de nombreuses études ont montré que les hépatocytes dérivés de cellules souches restaient proches d’un phénotype fœtal [2], caractérisé par une faible expression des cytochromes P450, des transporteurs canaliculaires et des enzymes de phase II3, limitant leur utilité pour la modélisation des maladies, la pharmacologie et la toxicologie. En 2025, T. Sato et ses collaborateurs ont franchi une étape décisive en décrivant la génération d’organoïdes d’hépatocytes adultes humains capables d’autorenouvellement, d’exprimer un ensemble complet de gènes du métabolisme, et de former des réseaux canaliculaires biliaires fonctionnels [3]. L’équipe a en effet mis au point un protocole de différenciation séquentielle guidée, dans lequel ils ont modulé la voie de signalisation du TGF-β (transforming growth factor β) et exposé les cellules à l’acide rétinoïque afin de maintenir la plasticité des hépatoblastes, tout en favorisant l’expression coordonnée des facteurs de maturation HNF4A (hepatocyte nuclear factor 4 alpha), FOXA2 (forkhead box protein A2) et PXR (pregnane X receptor). Parallèlement, les chercheurs ont reconstruit un microenvironnement tridimensionnel biliaire biomimétique, en utilisant une matrice composite de collagène I et de laminine-511,favorisant la polarisation apico-basale des hépatocytes et la formation de jonctions serrées. Cette architecture a permis l’émergence spontanée de réseaux canaliculaires interconnectés exprimant MRP2 (multidrug resistance-associated protein 2) et BSEP (bile salt export pump), deux facteurs capables de transporter activement des substrats biliaires fluorescents. L’introduction de gradients d’oxygène et de signaux mécaniques doux, assurée par l’intermédiaire d’un flux microfluidique, a favorisé une maturation métabolique proche du foie adulte. Ensemble, ces ajustements expliquent le degré inédit de maturation observé, confirmé par la restauration de fonctions métaboliques après transplantation chez la souris.
Dans le même temps, l’équipe de Y. Kuse a mis en évidence un rôle inattendu des signaux d’origine placentaire dans la croissance des organoïdes dérivés de cellules souches pluripotentes induites (iPSC : induced pluripotent stem cells) [4]. Leur étude a montré que l’IL1α (interleukine 1α), sécrétée sous hypoxie par les cellules trophoblastiques, active la voie immunodéveloppementale SAA1 (serum amyloid A1) –TLR2 (Toll-like receptor 2) –CCL20 (C-C motif chemokine ligand 20) –CCR6 (C-C chemokine receptor 6) dans les hépatoblastes. Au cours de celleci, l’IL1α induit la production du facteur SAA1, le ligand endogène du récepteur TLR2, qui déclenche à son tour une signalisation par la voie NF-kB, conduisant à la sécrétion de CCL20. Ce dernier agit sur son récepteur CCR6 selon une boucle autocrine et paracrine, stimulant la prolifération et la survie des cellules hépatiques. Ce circuit reproduit un mécanisme physiologique observé lors du développement hépatique embryonnaire, où des signaux inflammatoires contrôlés participent à l’expansion rapide du tissu hépatique. En culture, sa réactivation a permis d’obtenir une prolifération plus importante et homogène, ouvrant ainsi la voie à une production d’organoïdes plus robuste et standardisée. De plus, l’intégration de voies métaboliques complexes, incluant la gestion des lipides, du glucose et des xénobiotiques via les cytochromes P450, rapproche les organoïdes hépatiques d’un fonctionnement physiologique adulte [5].
Zonation hépatique
Le foie adulte est organisé en zones métaboliques distinctes, définies par des gradients d’oxygène, de nutriments, d’hormones et de signaux morphogénétiques le long de l’axe porto-central. Cette organisation en lobules comprend trois régions principales : la région périportale (zone 1), la région intermédiaire (zone 2) et la région péricentrale (zone 3) [6]. Au sein de ces dernières, les hépatocytes expriment des ensembles de gènes spécifiques, responsables de la spécialisation fonctionnelle du parenchyme, allant de la gluconéogenèse périportale jusqu’à la détoxification centrolobulaire. Reproduire cette architecture était jusque-là hors de portée. En 2025, l’équipe dirigée par Takebe a mis au point des organoïdes « multizonés » mimant cette structuration spatiale (Figure 1) [7]. L’équipe a combiné des signaux moléculaires et des contraintes physiques : la création de gradients de Wnt/β-caténine, d’oxygène et de nutriments dans des cultures tridimensionnelles microfluidiques a permis de générer une organisation lobulaire stable, avec des populations cellulaires différenciées selon leur position au sein de l’organoïde. L’ajout de microcanaux perfusés a permis d’induire des microgradients comparables à ceux du flux portal. Transplantées chez des rongeurs, ces structures ont permis une amélioration significative de la survie après obstruction biliaire, démontrant les impacts physiologiques et fonctionnels de cette organisation spatiale et illustrant leur potentiel thérapeutique. Ce modèle ouvre des perspectives inédites pour l’étude de pathologies zonales telles que les lésions périportales observées dans la fibrose biliaire, certaines étapes de la MASLD (metabolic dysfunction-associated steatotic liver disease, ou maladie stéatosique d’origine métabolique) ou l’ischémie hépatique. Il constitue un jalon dans la compréhension de la physiologie spatiale du foie et un outil de choix pour la pharmacotoxicologie.
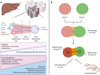 |
Figure 1 Zonation hépatique dans le foie humain (A), mimée par des organoides hépatiques « multizonés » [6]. B. (HLO : human liver organoid). Organisation architecturale (lobules) et métabolique (gradients d’oxygène, de nutriments, d’hormones et de signaux morphogénétiques) du foie humain, réparties en trois régions distinctes périportale (zone 1), intermédiaire (zone 2) et péricentrale (zone 3) et mimée dans les organoides par l’équipe de T. Takebe. Figure réalisée avec BioRender. |
Cocultures
Au-delà de cette organisation multizonée, les organoïdes hépatiques se sont enrichis de cocultures complexes intégrant entre autres des cholangiocytes, des cellules étoilées et des macrophages [8] (Figure 2). Cette diversité cellulaire a permis de reproduire des phénomènes pathologiques jusque-là inaccessibles en rétablissant des interactions paracrines cruciales dans l’homéostasie tissulaire et la réponse au stress. Dans des conditions de culture spécifiques, les organoïdes hépatiques peuvent mimer les premières étapes du développement d’une fibrose hépatique (activation des cellules étoilées, production de collagène I et fibrogenèse progressive), avec des réponses comparables à celles observées in vivo [9], validant ainsi leur pertinence comme modèle d’étude des maladies [10]. D’autres systèmes permettent de reproduire la MASLD [11] (→), la cirrhose ou encore des tumeurs primitives [12, 13] (→), ce qui permet d’explorer les mécanismes métaboliques et inflammatoires de ces maladies. Ces organoïdes « patients-spécifiques », dérivés d’iPSC ou de biopsies, constituent aujourd’hui de véritables plateformes pour la médecine personnalisée et la recherche translationnelle.
(→) Voir m/s n° 3, 2020, page 261
(→) Voir m/s n° 11, 2022, page 888
 |
Figure 2 Formation d’organoïdes hépatiques multicellulaires. En utilisant des protocoles de définis, on peut différencier les iPSC en hépatocytes, cholangiocytes, cellules endothéliales, celles étoilées ou encore macorphages, qui peuvent par la suite être mis en ccoculture pour former des organoides hépatiques complexes multicellulaires. Figure réalisée avec BioRender. |
Vascularisation et micro-environnements
La question de la vascularisation reste un défi central pour l’obtention d’organoïdes pleinement fonctionnels. Les premières tentatives de vascularisation utilisant des cellules dérivées des iPSC reposaient sur la coculture d’un endoderme hépatique, de précurseurs endothéliaux et mésenchymateux dérivés d’iPSC, aboutissant à une connexion partielle avec la circulation après transplantation [14]. Les cellules endothéliales ainsi différenciées peuvent être intégrées aux cultures tridimensionnelles dès la phase d’agrégation, ou combinées à des organoïdes hépatiques préformés dans des approches de fusion avec des organoïdes vasculaires (Figure 3). Les efforts actuels visent à obtenir cette organisation in situ, sans passage in vivo. Des protocoles combinant VEGF-A (vascular endothelial growth factor A) et FGF-2 (fibroblast growth factor 2) permettent désormais d’induire la différenciation endothéliale au sein des organoïdes eux-mêmes, conduisant à la formation de réseaux luminalisés, donc perfusables [15]. Plus récemment, l’utilisation combinée de CRISPR-Cas9 (clustered regularly interspaced short palindromic repeats) et d’outils d’intelligence artificielle a permis d’induire des facteurs de maturation tels que PROX1 (prospero homeobox gene 1), ATF5 (activating transcription factor 5) ou CYP3A4 (cytochrome P450 family 3A4), donnant naissance à des organoïdes hépatiques vascularisés, plus matures et capables de sécrétion biliaire [16].
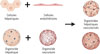 |
Figure 3 Stratégies de vascularisation des organoïdes hépatiques. Plusieurs stratégies peuvent être utilisées pour vasculariser un organoïde hépatique: (i) la coculture de cellules hépatiques avec des cellules endothéliales, ou (ii) la fusion d’organoïdes hépatiques et vasculaires. Figure réalisée avec BioRender. |
Ces avancées, couplées aux progrès de la bioimpression, ouvrent la voie à la fabrication de greffons extracorporels, capables de soutenir temporairement la fonction du foie chez un patient en attente de transplantation. En effet, la bio-impression 3D permet de déposer précisément des agrégats cellulaires hépatiques et vasculaires dans des matrices bioactives, reproduisant la géométrie lobulaire et facilitant la diffusion des nutriments [17]. En intégrant des capillaires préformés et des zones de perfusion contrôlée, les systèmes bio-imprimés constituent aujourd’hui la voie la plus prometteuse pour surmonter la limitation de biomasse et standardiser la production de tissus.
Enfin, une autre avancée technologique est la microfluidique, dont les progrès jouent un rôle majeur dans la survie des organoïdes. En effet, l’absence de perfusion continue peut conduire à une hypoxie centrale et à une nécrose progressive de l’organoïde au-delà de 200 à 300 µm d’épaisseur. Les nouvelles générations de dispositifs microfluidiques (canaux microperfusés, coques d’oxygénation intégrées, systèmes « liver-on-chip », etc.) permettent désormais de maintenir un flux laminaire d’oxygène et de nutriments [18]. Ces dispositifs reproduisent la physiologie du flux sanguin portal et créent des gradients d’oxygène réalistes, réduisant significativement la nécrose et favorisant une maturation plus homogène. Néanmoins, la perfusion continue et fonctionnelle in vitro reste hors de portée, et les organoïdes ne deviennent pleinement vascularisés qu’après transplantation chez l’animal [19].
Applications translationnelles et précliniques
Les progrès récents dans la structuration, la maturation et la vascularisation des organoïdes hépatiques ouvrent désormais des perspectives concrètes d’application en recherche translationnelle et en médecine régénérative (Figure 4). Ces modèles tridimensionnels, initialement développés comme outils de biologie fondamentale, s’imposent aujourd’hui comme des prototypes crédibles de tissus implantables et de plateformes pharmacologiques avancées.
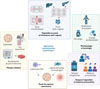 |
Figure 4 Applications translationnelles et précliniques de organoïdes hépatiques. Les oganoïdes hépatiques peuvent être utilisés dans des approches de thérapies cellulaires après transplantation ou utilisés dans des systèmes extracorporels. Ils sont également des précieux outils d’étude et de diagnostique dans des approches microfluidiques sur puces, des études pharmacologiques, toxicologiques et/ou immunitaires, ainsi que pour la création de banques. Figure réalisée avec BioRender. |
Études pharmacologiques et toxicologiques
Grâce à une expression plus fidèle des enzymes impliquées dans la biotransformation, notamment des cytochromes P450, et des transporteurs canaliculaires, ces modèles permettent désormais une évaluation plus fine de la clairance4, de la toxicité et des interactions médicamenteuses. Leur stabilité métabolique surpasse celle des hépatocytes primaires isolés, souvent instables en culture, et des lignages tumoraux, dont les fonctions sont altérées. Plusieurs travaux récents ont montré que ces organoïdes reproduisent les profils de toxicité de médicaments hépatotoxiques, tels que le paracétamol ou le méthotrexate, avec une pertinence proche de celle des données cliniques humaines [20, 21].
L’intégration de cellules étoilées, de cholangiocytes et de macrophages résidents a en outre permis de générer des organoïdes multicellulaires capables de mimer des conditions pathologiques complexes, notamment la fibrose, la cholestase ou la MASLD [22, 23]. Ces systèmes réagissent de manière reproductible à des antifibrotiques ciblant le TGF-β ou le PDGFR-β (platelet-derived growth factor receptor-β), démontrant leur capacité à servir de plateformes de criblage thérapeutique dans des contextes pathologiques reproduits in vitro [24, 25].
Les organoïdes se révèlent également particulièrement adaptés à la modélisation de maladies génétiques du foie. L’utilisation d’iPSC dérivées de patients porteurs de mutations, notamment celle responsable du déficit en facteur IX dans l’hémophilie B [26], permet de reconstituer fidèlement des phénotypes moléculaires et cellulaires [27]. De plus, l’introduction ciblée de mutations, ou leur correction, par la technique CRISPR-Cas9, a permis la génération d’organoïdes isogéniques formant des paires « mutant/corrigé », constituant des outils puissants pour comprendre l’impact direct d’un variant génétique sur la physiopathologie hépatique et sur les réponses aux médicaments [28].
Organoïdes sur puces et interactions multi-organes
Comme évoqué précédemment, l’une des évolutions majeures de la dernière décennie est l’intégration des organoïdes hépatiques dans des dispositifs microfluidiques. Ces plateformes permettent de reproduire les interactions physiologiques entre le foie et d’autres organes métaboliquement couplés, tels que l’intestin ou le pancréas. Des systèmes « multi-organoid-on-a-chip », associant des organoïdes intestinaux et hépatiques dérivés de cellules souches humaines, ont ainsi permis de reproduire les échanges métaboliques du cycle entéro-hépatique et de suivre en temps réel la biotransformation et la recirculation de composés lipophiles [29, 30]. D’autres dispositifs, intégrant des organoïdes pancréatiques, explorent les relations dynamiques entre métabolisme du glucose et sécrétion d’insuline, ouvrant la voie à des modèles physiopathologiques complexes de diabète et de stéatose métabolique [31].
Thérapie cellulaire : greffons, patchs et foies bio-artificiels
Un autre versant translationnel concerne la transplantation. Les organoïdes sont également testés comme greffons partiels ou patchs, destinés à être appliqués à la surface du foie lésé ou injectés dans le parenchyme, notamment pour réparer des lésions biliaires, avec des résultats précliniques prometteurs [32]. Dans des modèles murins de cholestase5 ou de fibrose biliaire, ces greffons se sont intégrés au tissu hôte et ont contribué à restaurer partiellement la fonction hépatique. Pour atteindre une échelle compatible avec l’application clinique, la bio-impression 3D apparaît comme un outil stratégique. En effet, en couplant bio-impression et microfluidique, il devient possible de créer des tissus vascularisés pouvant être assemblés en greffons de grande taille. Cette approche facilite également la standardisation de la production : les paramètres de dépôt, de densité cellulaire et de perfusion peuvent être contrôlés automatiquement, ouvrant la voie à des procédés robotisés conformes aux normes GMP (good manufacturing practices). Ces développements s’accompagnent de la mise en place de protocoles standardisés de contrôle qualité, basés sur l’expression des marqueurs de différenciation, l’activité enzymatique des cytochromes, la production d’albumine, ainsi que l’intégrité des jonctions canaliculaires. Ces résultats ont conduit à l’exploration de stratégies plus ambitieuses : la mise au point de foies bioartificiels extracorporels, combinant des organoïdes vascularisés à des bioréacteurs perfusés [33].
Ces bioréacteurs, inspirés des dispositifs de dialyse hépatique, sont conçus pour accueillir une biomasse cellulaire équivalente à 109 à 1010 hépatocytes, seuil estimé pour assurer une fonction de détoxification minimale [34]. Les organoïdes y sont disposés dans des cartouches traversées par un flux sanguin artificiel. L’utilisation d’organoïdes matures, plutôt que de suspensions d’hépatocytes isolés, améliore la stabilité métabolique et la résistance mécanique des cultures. Des études précliniques montrent déjà que ces systèmes peuvent améliorer la survie d’animaux en insuffisance hépatique aiguë [35].
Vers des organoïdes immunocompétents : étude des réponses immunitaires
Un champ émergeant particulièrement prometteur concerne l’introduction de cellules immunitaires dans les organoïdes hépatiques, afin de mieux comprendre et contrôler les réactions immunologiques associées à la transplantation. En effet, le foie étant un organe hautement immunomodulateur, son microenvironnement cellulaire joue un rôle clé dans la tolérance aux greffes et la réponse aux lésions. Des travaux récents ont montré qu’il était possible d’incorporer des macrophages (cellules de Kupffer) dans des organoïdes dérivés d’iPSC [36]. De la même manière, l’addition de lymphocytes T CD8+ permet d’étudier la reconnaissance allogénique et les mécanismes de rejet in vitro [37]. À terme, ces organoïdes immunocompétents pourraient constituer la base de greffons « humanisés », capables d’interagir harmonieusement avec le système immunitaire du receveur. Leur mise au point implique de relever plusieurs défis : la stabilité des populations immunitaires dans le temps, l’homogénéité de leur distribution et le contrôle de l’inflammation liée à la culture prolongée. Toutefois, les progrès réalisés dans la différenciation d’iPSC vers des lignages myéloïdes et lymphoïdes rendent désormais cette ambition crédible.
Banques d’organoïdes et médecine personnalisée
Enfin, les avancées réalisées en termes de production et de cryopréservation des organoïdes ont permis d’entamer le développement de biobanques dédiées. Ces collections permettent d’étudier la variabilité inter-individuelle dans les réponses métaboliques et les effets indésirables des médicaments. Plusieurs initiatives, en Europe (Hubrecht organoid biobank, Pays Bas) et au Japon (Japan organoid repository), visent à regrouper des organoïdes sains ou issus de patients atteints de maladies génétiques rares, de MASLD ou de cancers hépatiques. Ces biobanques constituent une ressource stratégique pour la médecine personnalisée, mais également pour la sélection de candidats dans des essais cliniques. Combinées à des approches d’intelligence artificielle, elles permettent d’analyser à haut débit les signatures transcriptomiques et métaboliques associées à la réponse au traitement. À terme, chaque organoïde patient-spécifique pourrait devenir un modèle prédictif pour guider la décision thérapeutique.
Enjeux et éthique
Le passage des organoïdes de la paillasse au lit du patient implique de relever plusieurs défis. La standardisation et l’automatisation des protocoles de production sont essentielles pour assurer une reproductibilité entre lots et une production à grande échelle compatible avec les exigences de la recherche clinique. Les biobanques d’iPSC, comme l’« European bank for induced pluripotent stem cells » (EBiSC), constituent un facteur déterminant en fournissant des lignées bien caractérisées, traçables et certifiées pour l’usage pharmaceutique. En parallèle, des acteurs industriels comme SunBioscience (Gri3D®) ou Evotec6 développent des procédés conformes aux normes GMP, ouvrant la voie à une production semi-automatisée d’organoïdes destinés aux essais précliniques ou aux dispositifs bioartificiels.
L’intégration de la robotisation dans les chaînes de culture permet d’envisager une production à haut débit, standardisée et contrôlée en continu, tout en réduisant la variabilité humaine. Cette automatisation s’accompagne de la mise en place de procédures de contrôle qualité harmonisées, incluant la caractérisation morphologique, le profil transcriptomique, la mesure de l’activité enzymatique (par exemple CYP3A4, MRP2 et albumine), ainsi que la vérification de la fonctionnalité biliaire. Ces outils, encore expérimentaux, constituent une condition sine qua non pour toute application clinique future.
Au-delà des aspects techniques, les organoïdes hépatiques contribuent à un changement de paradigme dans la recherche biomédicale : ils participent à la réduction de l’expérimentation animale, en offrant des modèles in vitro de plus en plus prédictifs du comportement in vivo chez l’être humain. Leur complexité structurelle et fonctionnelle, intégrant désormais les cholangiocytes, les cellules endothéliales, les cellules étoilées, les macrophages, et même les cellules immunitaires, permet de reproduire des processus pathologiques et pharmacologiques jusque-là étudiés exclusivement sur des modèles animaux. Les études de toxicité hépatique, d’inflammation ou de fibrose peuvent ainsi être menées sur des tissus humains miniaturisés, tout en respectant les principes des « 3R » (reduce, refine, replace) définis par la directive européenne 2010/63/UE [38]. Cette substitution progressive de l’expérimentation animale par des systèmes organoïdes constitue non seulement une avancée éthique, mais également scientifique, en améliorant la transposabilité des résultats à l’être humain.
L’essor de structures de plus en plus complexes, notamment les organoïdes vascularisés et immunocompétents, soulève de nouvelles questions éthiques et sociétales. Les organoïdes vascularisés, capables d’exercer certaines fonctions physiologiques de l’organe natif, interrogent sur leur statut moral et sur les limites de leur utilisation en transplantation ou en recherche. En effet, si les organoïdes hépatiques ne présentent évidemment aucune conscience ni autonomie fonctionnelle, leur complexification exige une réflexion bioéthique continue sur la finalité et les conditions de leur usage. L’emploi de facteurs d’origine placentaire, bien qu’efficace, soulève des questions sur l’origine, la traçabilité et le consentement lié aux tissus humains utilisés pour leur extraction ou leur modélisation.
Afin d’accompagner ces évolutions, plusieurs initiatives internationales ont émergé. Parmi lesquelles, les recommandations de l’ISSCR (international society for stem cell research), actualisées en 2025, précisent les critères éthiques de l’utilisation des cellules souches dans la recherche ainsi que les applications cliniques qui peuvent en découler, dont la création et l’utilisation des organoïdes humains. Dans la même logique, le projet européen HYBRIDA7 (human-integrated bioethical research on organoid and chimeric technologies, 2020– 2024), financé dans le cadre d’Horizon Europe, a joué un rôle majeur. Ce programme interdisciplinaire associe biologistes, philosophes, juristes et cliniciens pour définir des lignes directrices éthiques et réglementaires relatives à la recherche sur les organoïdes et les chimères humaines. Ces cadres en constante évolution visent à prévenir les dérives, tout en favorisant la collaboration entre chercheurs, cliniciens et institutions. Ainsi, le développement rapide des organoïdes hépatiques ne se résume pas à un progrès technologique : il appelle à une évolution parallèle des normes, des pratiques et des valeurs. L’équilibre entre innovation biomédicale, réduction de l’expérimentation animale et responsabilité éthique conditionnera leur acceptabilité sociale et leur intégration dans la médecine de demain.
Perspectives
En l’espace de quelques années, les organoïdes hépatiques sont passés du statut de modèles expérimentaux prometteurs à celui de micro-tissus métaboliquement actifs, vascularisés, multizonés et partiellement immunocompétents. Les avancées récentes ouvrent la voie à une nouvelle ère pour la recherche biomédicale et la médecine régénérative.
Maturation fonctionnelle et stabilité à long terme
Le premier défi des années à venir concerne la maturation complète et stable des organoïdes en coculture, indispensable pour reproduire durablement la physiologie hépatique adulte. Les efforts se concentrent aujourd’hui sur l’activation de réseaux transcriptionnels matures et sur l’optimisation des milieux de culture à base de nutriments lipidiques complexes et d’hormones stéroïdiennes [39]. L’utilisation de l’intelligence artificielle en biologie devrait permettre de modéliser les boucles métaboliques et d’ajuster dynamiquement les conditions de culture pour maintenir la fonctionnalité à long terme [40].
Perfusion, microfluidique et intégration vasculaire
Le second verrou à lever reste la perfusion continue et la connexion vasculaire fonctionnelle in vitro. Les approches actuelles, basées sur des microcanaux perfusés, des réseaux endothéliaux luminalisés et des matrices à porosité contrôlée, ne reproduisent encore qu’imparfaitement la circulation sinusoïdale du foie. La prochaine étape consistera à combiner les plateformes organoïdes-sur-puce avec des systèmes microfluidiques autonomes, capables de réguler le flux, la pression et la composition du milieu en temps réel. Ces dispositifs viseront à reproduire non seulement la perfusion, mais aussi la mécanotransduction, c’est-à-dire le dialogue entre le flux sanguin, l’oxygène et la différenciation cellulaire, qui structure le foie in vivo. Les progrès de la microfabrication, associés à des capteurs optiques intégrés, permettront de suivre la consommation d’oxygène, le pH et la sécrétion d’albumine en continu, rendant possible une culture physiologiquement augmentée.
Immunotolérance et compatibilité biologique
La question de l’immunotolérance sera cruciale pour toute application clinique. Si les organoïdes autologues, dérivés des propres cellules iPSC du patient, constituent une solution séduisante, leur production reste coûteuse et longue. Une alternative explorée est celle des organoïdes allogéniques « universels », capables d’être greffés à différents receveurs sans réaction immunitaire majeure. Ces tissus sont générés à partir de lignées pluripotentes modifiées pour échapper à la reconnaissance immunitaire, par exemple via la délétion des antigènes HLA de classe I/II et l’expression de molécules inhibitrices telles que HLA-G. De telles stratégies visent à recréer un état de tolérance furtif vis-à-vis du système immunitaire du receveur.
Dans cette perspective globale, l’initiative japonaise du Center for iPS cell research and application (CiRA8), fondée par Shinya Yamanaka, occupe une place centrale. Depuis 2010, cette biobanque nationale a établi une collection de lignées d’iPSC homozygotes pour les loci HLA, soigneusement sélectionnées pour couvrir la majorité de la population japonaise. En combinant typage immunogénétique et compatibilité HLA, le projet vise à constituer un stock de lignées allogéniques « prêtes à l’emploi », utilisables pour des applications thérapeutiques standardisées, dont la bio-ingénierie hépatique. Cette approche illustre une stratégie intermédiaire entre l’autologue et l’universel : réduire le risque de rejet sans recourir à une immunosuppression lourde, tout en garantissant la disponibilité rapide du greffon.
Convergence technologique : intelligence artificielle et bio-impression
Les perspectives les plus ambitieuses résident dans la convergence des technologies émergentes. La bioimpression 3D pourrait s’associer à la robotisation et à l’intelligence artificielle pour automatiser la fabrication de greffons sur mesure. L’intelligence artificielle pourrait optimiser, en temps réel, la densité cellulaire, la distribution des matrices et la perfusion des bioréacteurs, tandis que les algorithmes de conception générative permettraient de reproduire la géométrie lobulaire à différentes échelles.
À terme, ces approches pourraient déboucher sur des foies biofabriqués vascularisés, assemblés à partir de modules organoïdes imprimés et connectés entre eux par des réseaux microfluidiques. Ces « méta-organoïdes » pourraient être utilisés comme greffons extracorporels temporaires pour soutenir les patients en insuffisance hépatique aiguë, ou comme prototypes de tissus implantables chez l’homme.
Vers une « médecine par les organoïdes »
Au-delà des approches expérimentales ou de la perspective du greffon biofabriqué, les organoïdes hépatiques s’inscrivent désormais dans un cadre plus large que l’on pourrait qualifier de « médecine par les organoïdes ». Cette nouvelle approche relie directement la biologie cellulaire et la clinique : les tissus cultivés deviennent à la fois des outils de compréhension, de prédiction et, à terme, d’intervention thérapeutique.
Dans cette vision, chaque organoïde dérivé d’un patient constitue un modèle biologique unique, capable de reproduire fidèlement ses caractéristiques génétiques et métaboliques. Il permet d’évaluer la toxicité de médicaments, de tester des thérapies ciblées ou d’anticiper des complications avant traitement. Couplés à des plateformes de microfluidique et à des algorithmes d’intelligence artificielle, ils pourraient former un écosystème expérimental où la simulation numérique et la biologie vivante interagiraient en continu.
À plus long terme, la convergence des progrès en bio-impression, en robotisation et en culture automatisée ouvre la perspective de tissus personnalisés produits à la demande, avec des niveaux de standardisation et de sécurité compatibles avec un usage clinique. Ces technologies pourraient permettre la fabrication de greffons extracorporels destinés à soutenir temporairement la fonction hépatique, ou de modules tissulaires implantables capables de compléter un foie défaillant.
Cette « médecine par les organoïdes » ne se limite pas à la régénération : elle inaugure une nouvelle manière de penser la médecine expérimentale, fondée sur la modélisation fidèle de la physiologie humaine, la personnalisation des traitements et la réduction de la dépendance à l’expérimentation animale.
Conclusion
En l’espace de quelques années, les organoïdes hépatiques sont passés du statut de modèles prometteurs à celui d’outils biomédicaux complexes, métaboliquement actifs, multizonés et en voie de vascularisation. Ces avancées marquent un tournant : l’organoïde n’est plus seulement un outil de recherche, mais devient un outil fonctionnel en passe d’intégrer la médecine régénérative, annonçant une révolution biomédicale dans le domaine de la transplantation et de la médecine personnalisée. Leur évolution illustre la capacité de la recherche à rapprocher la biologie fondamentale de la thérapeutique, en créant des systèmes capables d’émuler, puis de réparer, la fonction d’un organe humain. À l’horizon 2030, le défi ne sera plus seulement de reproduire le foie, mais de l’exploiter comme modèle dynamique et personnalisable du vivant.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
Références
- Luce E, Messina A, Caillaud A, et al. Les organoïdes hépatiques : quels sont les enjeux ? Med Sci (Paris) 2021 ; 37 : 902–9. [Google Scholar]
- Yu Y, Liu H, Ikeda Y, et al. Hepatocyte-like cells differentiated from human induced pluripotent stem cells: Relevance to cellular therapies. Stem Cell Res 2012 ; 9 : 196–207. [Google Scholar]
- Igarashi R, Oda M, Okada R, et al. Generation of human adult hepatocyte organoids with metabolic functions. Nature 2025 ; 641 : 1248–57. [Google Scholar]
- Kuse Y, Matsumoto S, Tsuzuki S, et al. Placenta-derived factors contribute to human iPSC-liver organoid growth. Nat Commun 2025 ; 16 : 2493. [Google Scholar]
- Osonoi S, Takebe T. Organoid-guided precision hepatology for metabolic liver disease. J Hepatol 2024 ; 80 : 805–21. [Google Scholar]
- Jungermann K, Katz N. Functional specialization of different hepatocyte populations. Physiol Rev 1989 ; 69 : 708–64. [Google Scholar]
- Reza HA, Santangelo C, Iwasawa K, et al. Multi-zonal liver organoids from human pluripotent stem cells. Nature 2025 ; 641 : 1258–67. [Google Scholar]
- Harrison SP, Siller R, Tanaka Y, et al. Scalable production of tissue-like vascularized liver organoids from human PSCs. Exp Mol Med 2023 ; 55 : 2005–24. [Google Scholar]
- Kim HY, Lee W, Liu X, et al. Protocol to generate human liver spheroids to study liver fibrosis induced by metabolic stress. STAR Protocols 2024 ; 5 : 103111. [Google Scholar]
- Guan Y, Enejder A, Wang M, et al. A human multi-lineage hepatic organoid model for liver fibrosis. Nat Commun 2021 ; 12 : 6138. [Google Scholar]
- Collin De l’Hortet A, Gilgenkrantz H. L’émergence des modèles miniatures de foie gras humain en 3D générés en laboratoire. Med Sci (Paris) 2020 ; 36 : 261–3. [Google Scholar]
- Perréard M, Florent R, Thorel L, et al. Les organoïdes dérivés de tumeurs (ou tumoroïdes), des outils de choix pour la médecine de précision en oncologie. Med Sci (Paris) 2022 ; 38 : 888–95. [Google Scholar]
- Giron-Michel J, Padelli M, Oberlin E, et al. State-of-the-art liver cancer organoids: modeling cancer stem cell heterogeneity for personalized treatment. BioDrugs 2025 ; 39 : 237–60. [Google Scholar]
- Takebe T, Sekine K, Kimura M, et al. Massive and reproducible production of liver buds entirely from human pluripotent stem cells. Cell Reports 2017 ; 21 : 2661–70. [Google Scholar]
- Kim HJ, Kim G, Chi KY, et al. Generation of multilineage liver organoids with luminal vasculature and bile ducts from human pluripotent stem cells via modulation of Notch signaling. Stem Cell Res Ther 2023 ; 14 : 19. [Google Scholar]
- Velazquez JJ, LeGraw R, Moghadam F, et al. Gene regulatory network analysis and engineering directs development and vascularization of multilineage human liver organoids. Cell Systems 2021 ; 12 : 41–55.e11. [Google Scholar]
- Yan J, Ye Z, Lu Y, et al. 3D bioprinting lobule-like hepatorganoids with induced vascularization for orthotopic implantation. Materials Today Bio 2025 ; 31 : 101515. [Google Scholar]
- Deguchi S, Takayama K. State-of-the-art liver disease research using liver-on-a-chip. Inflamm Regen 2022 ; 42 : 62. [Google Scholar]
- Kim HJ, Kim G, Chi KY, et al. In Vitro Generation of luminal vasculature in liver organoids: from basic vascular biology to vascularized hepatic organoids. Int J Stem Cells 2023 ; 16 : 1–15. [Google Scholar]
- Shinozawa T, Kimura M, Cai Y, et al. High-fidelity drug-induced liver injury screen using human pluripotent stem cell–derived organoids. Gastroenterology 2021 ; 160 : 831–46.e10. [Google Scholar]
- Wu X, Jiang D, Yang Y, et al. Modeling drug-induced liver injury and screening for anti-hepatofibrotic compounds using human PSC-derived organoids. Cell Regen 2023 ; 12 : 6. [Google Scholar]
- Wu X, Jiang D, Wang Y, et al. Modeling metabolic-associated steatohepatitis with human pluripotent stem cell-derived liver organoids. Hepatol Commun 2024 ; 8 : e0585. [Google Scholar]
- Sgodda M, Gebel E, Dignas L, et al. iPSC-based hepatic organoids reveal a heterozygous MYO5B variant as driver of intrahepatic cholestasis. Hepatol Comm 2025 ; 9 : e0812. [Google Scholar]
- Yoon Y, Gong SC, Kim MY, et al. Generation of fibrotic liver organoids using hepatocytes, primary liver sinusoidal endothelial cells, hepatic stellate cells, and macrophages. Cells 2023 ; 12 : 2514. [Google Scholar]
- Coll M, Perea L, Boon R, et al. Generation of hepatic stellate cells from human pluripotent stem cells enables in vitro modeling of liver fibrosis. Cell Stem Cell 2018 ; 23 : 101–13.e7. [Google Scholar]
- Luce E, Steichen C, Allouche M, et al. In vitro recovery of FIX clotting activity as a marker of highly functional hepatocytes in a hemophilia B iPSC model. Hepatology 2022 ; 75 : 866–80. [Google Scholar]
- Guan Y, Xu D, Garfin PM, et al. Human hepatic organoids for the analysis of human genetic diseases. JCI Insight 2017 ; 2 : e94954. [Google Scholar]
- Hendriks D, Brouwers JF, Hamer K, et al. Engineered human hepatocyte organoids enable CRISPR-based target discovery and drug screening for steatosis. Nat Biotechnol 2023 ; 41 : 1567–81. [Google Scholar]
- Maschmeyer I, Lorenz AK, Schimek K, et al. A four-organ-chip for interconnected long-term co-culture of human intestine, liver, skin and kidney equivalents. Lab Chip 2015 ; 15 : 2688–99. [CrossRef] [PubMed] [Google Scholar]
- Lucchetti M, Aina KO, Grandmougin L, et al. An Organ-on-chip platform for simulating drug metabolism along the gut–liver axis. Adv Healthc Mater 2024 ; 13 : 2303943. [Google Scholar]
- Tao T, Deng P, Wang Y, et al. Microengineered multi-organoid system from hiPSCs to recapitulate human liver-islet axis in normal and type 2 diabetes. Adv Sci (Weinh) 2022 ; 9 : 2103495. [Google Scholar]
- Sampaziotis F, Muraro D, Tysoe OC, et al. Cholangiocyte organoids can repair bile ducts after transplantation in the human liver. Science 2021 ; 371 : 839–46. [CrossRef] [PubMed] [Google Scholar]
- Hussein M, Pasqua M, Pereira U, et al. Microencapsulated hepatocytes differentiated from human induced pluripotent stem cells: optimizing 3d culture for tissue engineering applications. Cells 2023 ; 12 : 865. [Google Scholar]
- Sakiyama R, Blau BJ, Miki T. Clinical translation of bioartificial liver support systems with human pluripotent stem cell-derived hepatic cells. World J Gastroenterol 2017 ; 23 : 1974–9. [Google Scholar]
- Selden C, Bundy J, Erro E, et al. A clinical-scale bioartificial liver, developed for GMP, improved clinical parameters of liver function in porcine liver failure. Sci Rep 2017 ; 7 : 14518. [Google Scholar]
- Li Y, Nie Y, Yang X, et al. Integration of Kupffer cells into human iPSC-derived liver organoids for modeling liver dysfunction in sepsis. Cell Reports 2024 ; 43 : 113918. [Google Scholar]
- Soussi FEA, Brusilovsky M, Buck E, et al. Autologous organoid-t cell co-culture platform for modeling of immune-mediated drug-induced liver injury. Adv Sci (Weinh) 2025 ; 12 : e08584. [Google Scholar]
- Lewis DI. Animal experimentation: implementation and application of the 3Rs. Emerg Top Life Sci 2019 ; 3 : 675–9. [Google Scholar]
- Liu Y, Zhou Y, Ahodantin J, et al. Generation and characterization of mature hepatocyte organoids for liver metabolic studies. J Cell Sci 2024 ; 137 : jcs261961. [Google Scholar]
- Maramraju S, Kowalczewski A, Kaza A, et al. AI-organoid integrated systems for biomedical studies and applications. Bioeng Transl Med 2024 ; 9 : e10641. [Google Scholar]
Les cholangiocytes sont les cellules qui tapissent les voies biliaires. Ils sont responsables d’importantes modifications de la bile sécrétée par les hépatocytes (ndlr).
Les cellules étoilées hépatiques ou cellules stellaires, sont présentes dans le parenchyme du foie. Elles sont localisées plus précisément dans les espaces de Disse, c’est-à-dire les espaces situés entre les hépatocytes et les cellules endothéliales des sinusoïdes veineux (ndlr).
Il s’agit d’enzymes, principalement des transférases, qui métabolisent les médicaments dans le foie (ndlr).
La clairance est la capacité d’un tissu, organe ou organisme à éliminer une substance donnée d’un liquide biologique (ndlr).
La cholestase est une maladie qui se caractérise par une réduction ou un arrêt de l’écoulement de la bile (ndlr).
Liste des figures
 |
Figure 1 Zonation hépatique dans le foie humain (A), mimée par des organoides hépatiques « multizonés » [6]. B. (HLO : human liver organoid). Organisation architecturale (lobules) et métabolique (gradients d’oxygène, de nutriments, d’hormones et de signaux morphogénétiques) du foie humain, réparties en trois régions distinctes périportale (zone 1), intermédiaire (zone 2) et péricentrale (zone 3) et mimée dans les organoides par l’équipe de T. Takebe. Figure réalisée avec BioRender. |
| Dans le texte | |
 |
Figure 2 Formation d’organoïdes hépatiques multicellulaires. En utilisant des protocoles de définis, on peut différencier les iPSC en hépatocytes, cholangiocytes, cellules endothéliales, celles étoilées ou encore macorphages, qui peuvent par la suite être mis en ccoculture pour former des organoides hépatiques complexes multicellulaires. Figure réalisée avec BioRender. |
| Dans le texte | |
 |
Figure 3 Stratégies de vascularisation des organoïdes hépatiques. Plusieurs stratégies peuvent être utilisées pour vasculariser un organoïde hépatique: (i) la coculture de cellules hépatiques avec des cellules endothéliales, ou (ii) la fusion d’organoïdes hépatiques et vasculaires. Figure réalisée avec BioRender. |
| Dans le texte | |
 |
Figure 4 Applications translationnelles et précliniques de organoïdes hépatiques. Les oganoïdes hépatiques peuvent être utilisés dans des approches de thérapies cellulaires après transplantation ou utilisés dans des systèmes extracorporels. Ils sont également des précieux outils d’étude et de diagnostique dans des approches microfluidiques sur puces, des études pharmacologiques, toxicologiques et/ou immunitaires, ainsi que pour la création de banques. Figure réalisée avec BioRender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




