| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
|
|
|---|---|---|
| Page(s) | 245 - 247 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026030 | |
| Published online | 20 mars 2026 | |
Immunosuppression et fièvre de Lassa sévère
Immunosuppression and severe Lassa fever
Unité de Biologie des infections virales émergentes, Institut Pasteur - Centre international de recherche en infectiologie, Université de Lyon, Inserm U1111, CNRS UMR5308, École normale supérieure de Lyon, Lyon, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
**
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
La fièvre de Lassa est une fièvre hémorragique virale endémique en Afrique de l’Ouest. Elle est causée par un arénavirus, le virus Lassa, contre lequel il n’existe ni vaccin autorisé, ni traitement spécifique efficace [1]. Elle est responsable de dizaines de milliers de cas par an et de milliers de morts. Les personnes qui succombent à cette infection sont victimes d’une défaillance multiviscérale, parfois accompagnée de saignements et d’atteintes du système nerveux central. Ce sepsis viral complique considérablement la prise en charge médicale des infections graves [2]. La pathogenèse de la maladie et les réponses immunitaires impliquées dans le contrôle de l’infection sont mal connues. L’obligation de manipuler le virus Lassa en laboratoire de confinement de niveau 4 et le fait que les épidémies surviennent dans des endroits reculés et mal dotés en structures de santé compliquent les études scientifiques sur cette maladie. De plus, le primate non-humain, et plus particulièrement le macaque, est le seul modèle animal permettant de reproduire la pathogenèse et les réponses immunitaires de la maladie humaine, ce qui constitue une difficulté supplémentaire. Nous avons développé un modèle fondé sur le singe cynomolgus (Macaca fascicularis) qui permet de reproduire le continuum des signes cliniques de la fièvre de Lassa chez l’homme, de l’infection quasi asymptomatique à l’infection fatale [3]. Lorsque les animaux sont infectés par la souche AV du virus Lassa, qui appartient au lignage 5 et a été isolée à partir d’un patient ayant succombé à la maladie [4], ils survivent à cette infection, dont la sévérité est modérée. En revanche, lorsqu’ils reçoivent la souche Josiah, qui appartient au lignage 4, ils développent une infection très sévère et toujours mortelle. Nous avons montré que lors de l’infection non fatale par le virus Lassa, la dissémination virale restait limitée aux organes lymphoïdes et était rapidement contrôlée[5]. L’absence d’envahissement de l’organisme par du matériel viral en grande quantité évitait l’induction d’une réponse inflammatoire excessive et délétère. Au contraire, chez les animaux qui ne contrôlent pas la réplication virale, la dissémination du virus Lassa s’étend à tous les organes, ce qui aboutit à la libération de matériel viral en très grande quantité, à l’infiltration de cellules inflammatoires dans les tissus (granulocytes neutrophiles et macrophages), à l’induction d’une tempête cytokinique et chimiokinique, et à un syndrome apparenté au sepsis viral. Enfin, dans ce modèle d’infection mortelle, les stades terminaux sont associés à une défaillance multiviscérale et à des troubles majeurs de l’hémostase [6].
Les mécanismes immunitaires associés à l’issue fatale de la fièvre de Lassa ou, au contraire, à son contrôle et à la guérison sont mal connus. La réponse humorale induite au cours de l’infection est dépourvue d’anticorps neutralisants, ces derniers n’apparaissant que plusieurs mois après la guérison. Les immunoglobulines G (IgG) spécifiques du virus Lassa, quant à elles, apparaissent de manière similaire chez tous les animaux infectés, ce qui indique que d’autres mécanismes immunitaires sont impliqués dans le contrôle de la réplication virale [3]. La réponse immunitaire innée précoce joue vraisemblablement un rôle crucial dans le contrôle de la dissémination virale en dehors des organes lymphoïdes, mais cela reste à montrer. En revanche, les arguments en faveur d’un rôle essentiel de la réponse impliquant les lymphocytes T dans le contrôle de la fièvre de Lassa s’accumulent. Nous avons montré l’existence d’une activation et d’une prolifération des lymphocytes T CD4+ et CD8+ chez les singes qui survivaient à la fièvre de Lassa, mais pas chez ceux qui ont succombé à l’infection [3]. Au contraire, chez ces derniers, une forte proportion des lymphocytes T circulants était apoptotique et exprimait PD1 (programmed cell death protein 1). Nous avons récemment confirmé l’importance de la réponse lymphocytaire T dans le contrôle du virus Lassa, par la détection des lymphocytes T CD4+ et CD8+ spécifiques de la glycoprotéine et de la nucléoprotéine du virus dans le sang, la rate et les ganglions lymphatiques des singes ayant survécu à l’infection, mais pas chez ceux pour lesquels l’infection a été fatale [7]. Afin d’identifier les causes de cette différence, le tropisme du virus Lassa a été analysé au sein des ganglions lymphatiques drainant le site d’inoculation du virus, qui sont les premiers à produire de nouvelles particules virales. Cinq jours après l’infection, le virus était principalement retrouvé dans les cellules dendritiques et dans des macrophages immunorégulateurs au cours de l’infection mortelle, tandis que seuls les macrophages, les cellules endothéliales et les cellules stromales étaient infectés chez les singes qui survivaient à l’infection. L’analyse transcriptomique des organes et du sang des animaux a mis en évidence l’ expression de groupes de gènes associés à l’immunosuppression, incluant ceux codant l’interleukine-10 et l’indoleamine 2,3-dioxygénase (IDO1), au cours de l’infection mortelle. Ces résultats nous ont incités à étudier l’implication des cellules myéloïdes suppressives dans la maladie. En effet, ces cellules sont des cellules myéloïdes immatures qui prolifèrent dans des situations pathologiques et suppriment les réponses impliquant les lymphocytes T. Nous avons constaté une diminution du nombre des monocytes classiques matures dans le sang au cours de l’infection fatale, alors que ce nombre augmentait chez les animaux qui contrôlaient l’infection. Dans les stades terminaux de la maladie, nous avons constaté un enrichissement du sang en cellules myéloïdes suppressives dérivées de monocytes (CD14+ HLA-DR- CD11b+ CD33+), tandis qu’un grand nombre de cellules myéloïdes suppressives dérivées de granulocytes (CD14- HLA-DR- CD11b+ CD66abce+) apparaissaient dès 6 jours après l’infection. Ces cellules exprimaient de plus PD1 et son ligand PD-L1, ce qui confirmait leur phénotype immunosuppresseur. Une analyse histologique fondée sur l’immunofluorescence multiplexée a ensuite permis de mettre en évidence, dès 5 jours après l’infection, la présence dans les ganglions lymphatiques d’un plus grand nombre de cellules myéloïdes suppressives PD-L1+ et de lymphocytes T exprimant PD1, souvent en contact avec les précédentes, chez les animaux ayant succombé à l’infection que chez les survivants. Semblable enrichissement en cellules myéloïdes suppressives a été mis en évidence dans les poumons et l’intestin des animaux qui ont succombé à l’infection. Des concentrations élevées de PD-L1 soluble ont été mesurées dans le sang au cours de l’infection sévère, confirmant l’activation de mécanismes suppresseurs de la réaction immunitaire. On sait l’importance de l’architecture du ganglion lymphatique et de son réseau de cellules stromales, cellules réticulées fibroblastiques, et cellules dendritiques fibroblastiques, pour l’induction des réponses immunitaires. Or le réseau de cellules réticulées fibroblastiques était très altéré dans les stades terminaux de la maladie, avec des cellules en apoptose et un plus grand nombre de cellules exprimant PD-L1 que chez les singes survivants. En particulier, les cellules réticulées fibroblastiques infectées par le virus exprimaient plus fréquemment PD-L1, suggérant que le tropisme du virus pour ces cellules impliquées dans la présentation antigénique induisait un phénotype immunosuppresseur et une destruction du réseau stromal.
Nous avons donc montré qu’au cours de l’infection fatale du singe macaque par le virus Lassa, le virus se réplique rapidement dans des macrophages immunosuppresseurs, ce qui induit un priming défectueux de l’immunité cellulaire spécifique et permet au virus de se disséminer aux organes périphériques non lymphoïdes (Figure 1). Cette dissémination est à l’origine d’une libération considérable de « motifs moléculaires associés aux microorganismes pathogènes », du recrutement de cellules de l’immunité innée (macrophages et granulocytes neutrophiles), et d’une activation immunitaire incontrôlée. Une myélopoïèse d’urgence est alors amorcée pour maintenir le pool de cellules de l’immunité innée, avec pour résultat l’accumulation de cellules myéloïdes immatures dans les organes et la suppression de la réponse cellulaire adaptative. Parallèlement, la destruction du réseau stromal des organes lymphoïdes secondaires altère l’homéostase des lymphocytes T et leur activation, ce qui permet une réplication virale incontrôlée. Les contacts des lymphocytes T avec les cellules réticulées fibroblastiques et les cytokines régulatrices induisent un épuisement et une anergie des lymphocytes T, expliquant l’absence de lymphocytes T spécifiques du virus Lassa chez les singes qui succombent à la maladie.
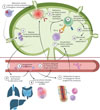 |
Figure 1 Schéma récapitulatif des mécanismes immunitaires et pathologiques associés à l’infection fatale par le virus Lassa chez le singe cynomolgus. Un ganglion lymphatique drainant un site de l’infection est représenté en vert. Un vaisseau sanguin est représenté en rouge. PAMP : pathogen-associated molecular pattern. Figure adaptée de [7]. |
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
Références
- Buchmeier MJ, de la Torre JC, Peters CJ. Arenaviridae. In: Knipe DM, Howley PM, Cohen JI, Griffin DE, Lamb RA, Martin MA, Racaniello VR, Roizman B (eds). Fields virology, 6th ed. Philadelphia: Lippincott Williams and Wilkins, 2013 : 1283–303. [Google Scholar]
- Duvignaud A, Jaspard M, Etafo IC, et al. Lassa fever outcomes and prognostic factors in Nigeria (LASCOPE): a prospective cohort study. Lancet Glob Health 2021 ; 9 : e469–78. [Google Scholar]
- Baillet N, Reynard S, Perthame E, et al. Systemic viral spreading and defective host responses are associated with fatal Lassa fever in macaques. Commun Biol 2021 ; 4 : 27. [Google Scholar]
- Günther S, Emmerich P, Laue T, et al. Imported Lassa fever in Germany: molecular characterization of a new Lassa virus strain. Emerg Infect Dis 2000 ; 6 : 466–76. [Google Scholar]
- Hortion J, Perthame E, Lafoux B, et al. Fatal Lassa fever in cynomolgus monkeys is associated with systemic viral dissemination and inflammation. PLoS Pathog 2024 ; 20 : e1012768. [Google Scholar]
- Lafoux B, Baillet N, Picard C, et al. Hemostasis defects underlying the hemorrhagic syndrome caused by mammarenaviruses in a cynomolgus macaque model. Blood 2023 ; 142 : 2092–104. [Google Scholar]
- Lafoux B, Fourcaud G, Hortion J, et al. Expansion of myeloid suppressor cells and suppression of Lassa virus-specific T cells during fatal Lassa fever. PLoS Pathog 2025 ; 21 : e1013111. [Google Scholar]
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Schéma récapitulatif des mécanismes immunitaires et pathologiques associés à l’infection fatale par le virus Lassa chez le singe cynomolgus. Un ganglion lymphatique drainant un site de l’infection est représenté en vert. Un vaisseau sanguin est représenté en rouge. PAMP : pathogen-associated molecular pattern. Figure adaptée de [7]. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




