| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
|
|
|---|---|---|
| Page(s) | 859 - 862 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2025218 | |
| Published online | 12 décembre 2025 | |
Un mode d’infection intercellulaire des macrophages par le VIH-1 qui résiste aux défenses immunitaires innées et aux traitements antirétroviraux
A cell-to-cell process of macrophage infection by HIV-1 is resistant to innate immune factors and antiretroviral drugs
1
Institut Cochin, Inserm U1016, CNRS UMR8104, Université Paris Cité, Paris, France
2
Institut RESTORE, Université de Toulouse, CNRS U5070, Établissement français du sang, École nationale vétérinaire de Toulouse, Inserm U1301, Toulouse, France
3
Service de biologie cellulaire, CHU Purpan, Toulouse, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Le paradoxe de l’infection des macrophages par le VIH-1
Les macrophages jouent un rôle central dans la physiopathologie de l’infection par le virus de l’immunodéficience humaine (VIH-1). Ils contribuent à la transmission du virus, à sa dissémination dans l’organisme, et à l’établissement de réservoirs viraux tissulaires persistants, y compris chez les personnes vivant avec le VIH-1 sous traitement antirétroviral [1]. La longévité et la distribution des macrophages infectés par le VIH-1 dans l’organisme sont propices à l’installation d’une infection chronique. Pourtant, les macrophages sont particulièrement résistants in vitro à l’infection par des virus libres. Cette faible permissivité peut s’expliquer par l’expression, souvent induite par les interférons, de plusieurs facteurs cellulaires de restriction de l’immunité innée, tels que SAMHD1 (SAM domain and HD domain-containing protein), les protéines de la famille APOBEC3 (apolipoprotein B mRNA editing enzyme, catalytic polypeptide) et SERINC (serine incorporator), ou BST-2 (bone marrow stromal cell antigen-2), qui bloquent différentes étapes du cycle de réplication virale [2]. Bien que ces facteurs de restriction soient généralement contrecarrés par les protéines auxiliaires du VIH-1, à savoir Nef (negative regulatory factor), Vif (viral infectivity factor), Vpr (viral protein R), et Vpu (viral protein U), la présence de ces protéines virales ne permet pas une infection très efficace des macrophages par des particules virales libres.
La faible infection des macrophages in vitro contraste avec la présence, chez les personnes vivant avec le VIH-1, de cellules myéloïdes infectées dans de nombreux tissus, souvent sous la forme de cellules géantes multinucléées [1]. Ce paradoxe apparent suggère l’existence d’un mode alternatif de transmission du virus permettant de contourner les restrictions cellulaires.
La fusion cellulaire entre lymphocytes T infectés et macrophages : un mode de transmission rapide et efficace du VIH-1 aux macrophages
Nous avons mis en évidence un mécanisme particulièrement efficace d’infection des macrophages reposant sur un processus de fusion cellulaire avec des lymphocytes T CD4+ infectés [3-7]. Dans un modèle d’infection in vitro, la coculture de macrophages avec des lymphocytes infectés induit un contact étroit entre les deux types de cellules, qui est rapidement suivi par la fusion de leurs membranes plasmiques. Cette fusion cellulaire entraîne la formation de cellules hybrides capables à leur tour de fusionner avec des macrophages non infectés environnants (Figure 1). Il en résulte la formation de cellules géantes multinucléées infectées contenant des noyaux issus des lymphocytes T et des macrophages, et productrices de grandes quantités de particules virales.
 |
Figure 1. Modèle de formation de cellules géantes multinucléées par fusion entre lymphocytes T infectés et macrophages. Un lymphocyte T infecté établit un contact avec un macrophage par la glycoprotéine d’enveloppe virale avant de fusionner (1ère fusion). Cette fusion conduit à la formation d’une cellule hybride capable ensuite de fusionner avec d’autres macrophages non infectés (2e fusion), donnant naissance à des cellules géantes multinucléées capables de produire des virus infectieux sur de longues périodes. In vivo, ce mécanisme pourrait contribuer à la dissémination virale et à l’établissement de réservoirs myéloïdes tissulaires. Figure créée avec BioRender. |
L’infection des macrophages par ce mécanisme de fusion avec des lymphocytes T infectés est plus rapide et plus efficace que leur infection par des virus libres, et elle ne nécessite pas la présence des protéines virales auxiliaires : en effet, leur absence n’empêche ni la formation des cellules géantes, ni la production de virus par ces cellules [3-7]. Des facteurs de restriction cellulaires tels que SERINC5, SAMHD1 et APOBEC3G, qui limitent l’infection par le VIH-1 libre, sont inefficaces lorsque le virus est transmis par fusion cellulaire, indépendamment de l’expression des protéines virales auxiliaires [4, 7]. L’activation des macrophages par des interférons de type I, qui induisent l’expression de nombreux gènes antiviraux, n’inhibe pas leur infection productive par fusion cellulaire (contrairement à une infection par des virus libres). Enfin, plusieurs molécules antirétrovirales ciblant les étapes précoces du cycle de réplication virale (synthèse de l’ADN viral par rétrotranscription, transport nucléaire et intégration de l’ADN proviral dans le génome de la cellule hôte) ne permettent pas d’obtenir une inhibition complète de l’infection des macrophages par fusion avec des lymphocytes T infectés [7].
Modèle de l’infection des macrophages par fusion cellulaire
Nous avons montré que les noyaux d’origine lymphocytaire des cellules géantes multinucléées issues de la fusion entre lymphocytes T infectés et macrophages restent transcriptionnellement actifs, comme l’indiquent l’expression prolongée, dans ces noyaux, d’un gène rapporteur placé sous le contrôle d’un promoteur viral, ainsi que la persistance, dans les cellules géantes, de marqueurs spécifiques de lymphocytes T [7]. Par ailleurs, des expériences d’hybridation in situ en fluorescence (FISH) réalisées très rapidement après la fusion mettent en évidence la présence d’ADN viral non seulement dans les noyaux d’origine lymphocytaire, comme attendu, mais également dans les noyaux d’origine macrophagique : cet ADN viral, qui ne peut pas avoir été synthétisé par les macrophages aussi rapidement après la fusion, pourrait être transmis sous la forme de complexes de pré-intégration viraux présents dans le cytoplasme des lymphocytes T infectés au moment de la fusion cellulaire, puis rapidement acheminés vers le noyau d’origine macrophagique, permettant l’intégration de l’ADN viral dans le génome cellulaire (Figure 2). Ainsi, l’infection des macrophages par fusion cellulaire contournerait les étapes précoces du cycle de réplication viral, permettant une infection rapide par le maintien de l’activité transcriptionnelle du noyau d’origine lymphocytaire et le transfert direct de matériel génétique viral dans le ou les noyaux d’origine macrophagique. Ce mécanisme intercellulaire d’infection des macrophages par fusion avec des lymphocytes T infectés permet ainsi d’expliquer l’échappement à l’activité antivirale des interférons de type I et aux facteurs cellulaires de restriction, ainsi que la résistance à certaines thérapies antivirales ciblant les étapes précoces du cycle de réplication viral. Il permet une production précoce, intense, et prolongée de virus par les cellules géantes multinucléées.
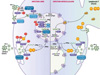 |
Figure 2. Modèle comparatif des deux modes d’infection des macrophages par le VIH-1. À gauche, l’infection par des virus libres suit les étapes classiques du cycle viral : entrée, rétrotranscription (RT) de l’ARN génomique viral (ARNg) en ADN, transport nucléaire et intégration de l’ADN viral dans le génome de la cellule cible. Ce processus est fortement limité par plusieurs facteurs de restriction cellulaires (SERINC5, APOBEC3G, SAMHD1, BST-2), contrecarrés par les protéines virales auxiliaires (en rouge), et ciblé par les traitements antirétroviraux. À droite, la fusion directe entre un lymphocyte T infecté et un macrophage entraîne le transfert massif de matériel viral et nucléaire. Par le maintien de l’activité transcriptionnelle du noyau lymphoïde, cette voie d’infection permet de contourner les restrictions cellulaires et les effets des molécules antirétrovirales. L’ADN viral peut aussi être retrouvé dans les noyaux myéloïdes, ce qui suggère l’existence d’un transfert de complexes de pré-intégration (PIC) qui vont migrer rapidement vers les noyaux myéloïdes. IFITM : interferon-induced transmembrane proteins ; ARNm : ARN messager viral ; INTI : inhibiteurs nucléosidiques de la transcriptase inverse ; INNTI : inhibiteurs non-nucléosidiques de la transcriptase inverse. Figure créée avec BioRender. |
Perspectives virologiques et thérapeutiques
Par leur longévité et leur capacité de forte production virale, les cellules géantes multinucléées pourraient donc contribuer à la dissémination tissulaire du virus et à la persistance de réservoirs viraux chez les personnes vivant avec le VIH-1, même sous traitement antirétroviral. La présence de cellules géantes dans différents tissus chez les personnes infectées par ce virus, ainsi que dans les modèles simiens d’infection par le virus de l’immunodéficience simienne (VIS), témoigne de la pertinence de ce mode d’infection des macrophages. La formation de cellules géantes par fusion entre cellules infectées et non infectées est un processus communément observé pour plusieurs virus enveloppés, dont le SARS-CoV-2, et qui explique en partie l’échappement de ces virus aux mécanismes de défense immunitaire [8]. Il importe donc de mieux caractériser ces cellules géantes multinucléées, sur le plan moléculaire et sur le plan fonctionnel, pour déterminer leur rôle dans la dynamique virale et leur contribution à la formation des réservoirs tissulaires du virus. À plus long terme, le ciblage des mécanismes viraux de fusion cellulaire et des propriétés spécifiques de ces cellules géantes multinucléées devrait être pris en compte pour le développement de nouvelles thérapies limitant la propagation et la persistance du VIH-1.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Woottum M, Yan S, Sayettat S, et al. Macrophages: key cellular players in HIV infection and pathogenesis. Viruses 2024 ; 16 : 288. [Google Scholar]
- Pagani I, Demela P, Ghezzi S, et al. Host restriction factors modulating HIV latency and replication in macrophages. Int J Mol Sci 2022 ; 3 : 3021. [Google Scholar]
- Bracq L, Xie M, Benichou S, et al. Mechanisms for cell-to-cell transmission of HIV-1. Front Immunol 2018 ; 9 : 260. [Google Scholar]
- Xie M, Leroy H, Mascarau R, et al. Cell-to-cell spreading of HIV-1 in myeloid target cells escapes SAMHD1 restriction. mBio 2019 ; 10 : e02457-19. [Google Scholar]
- Han M, Cantaloube-Ferrieu V, Xie M, et al. HIV-1 cell-to-cell spread overcomes the virus entry block of non-macrophage-tropic strains in macrophages. PLoS Pathog 2022 ; 18 : e1010335. [Google Scholar]
- Mascarau R, Woottum M, Fromont L, et al. Productive HIV-1 infection of tissue macrophages by fusion with infected CD4+ T cells. J Cell Biol 2023 ; 222 : e202205103. [Google Scholar]
- Woottum M, Yan S, Durringer A, et al. HIV-1 cell-to-cell infection of macrophages escapes type I interferon and host restriction factors, and is resistant to antiretroviral drugs. PLoS Pathog 2025 ; 21 : e1013130. [Google Scholar]
- Leroy H, Han M, Woottum M, et al. Virus-mediated cell-cell fusion. Int J Mol Sci 2020 ; 21 : 9644. [Google Scholar]
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Modèle de formation de cellules géantes multinucléées par fusion entre lymphocytes T infectés et macrophages. Un lymphocyte T infecté établit un contact avec un macrophage par la glycoprotéine d’enveloppe virale avant de fusionner (1ère fusion). Cette fusion conduit à la formation d’une cellule hybride capable ensuite de fusionner avec d’autres macrophages non infectés (2e fusion), donnant naissance à des cellules géantes multinucléées capables de produire des virus infectieux sur de longues périodes. In vivo, ce mécanisme pourrait contribuer à la dissémination virale et à l’établissement de réservoirs myéloïdes tissulaires. Figure créée avec BioRender. |
| Dans le texte | |
 |
Figure 2. Modèle comparatif des deux modes d’infection des macrophages par le VIH-1. À gauche, l’infection par des virus libres suit les étapes classiques du cycle viral : entrée, rétrotranscription (RT) de l’ARN génomique viral (ARNg) en ADN, transport nucléaire et intégration de l’ADN viral dans le génome de la cellule cible. Ce processus est fortement limité par plusieurs facteurs de restriction cellulaires (SERINC5, APOBEC3G, SAMHD1, BST-2), contrecarrés par les protéines virales auxiliaires (en rouge), et ciblé par les traitements antirétroviraux. À droite, la fusion directe entre un lymphocyte T infecté et un macrophage entraîne le transfert massif de matériel viral et nucléaire. Par le maintien de l’activité transcriptionnelle du noyau lymphoïde, cette voie d’infection permet de contourner les restrictions cellulaires et les effets des molécules antirétrovirales. L’ADN viral peut aussi être retrouvé dans les noyaux myéloïdes, ce qui suggère l’existence d’un transfert de complexes de pré-intégration (PIC) qui vont migrer rapidement vers les noyaux myéloïdes. IFITM : interferon-induced transmembrane proteins ; ARNm : ARN messager viral ; INTI : inhibiteurs nucléosidiques de la transcriptase inverse ; INNTI : inhibiteurs non-nucléosidiques de la transcriptase inverse. Figure créée avec BioRender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




