| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
Des nouvelles du passé
|
|
|---|---|---|
| Page(s) | 930 - 934 | |
| Section | Forum | |
| DOI | https://doi.org/10.1051/medsci/2025189 | |
| Published online | 12 décembre 2025 | |
Histoires de paléogénétique
Diffusion des populations des steppes et des langues indo-européennes : une première mondialisation ?
Dispersal of steppe populations and Indo-European languages: a first globalisation?
UMR7206 Éco-Anthropologie (EA), CNRS, Muséum national d’Histoire naturelle, Université Paris-Cité, Paris, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Vignette (© Céline Bon).
« Nez » se dit « nose » en anglais, mais aussi « nos » en russe, « nasa » en sanskrit1, « nosis » en lituanien, « nese » en norvégien ; quant à « nāf », en persan, « naris » en grec, et « nariz » en espagnol, ils signifient « narine ». Une même famille de langues est parlée à travers l’Eurasie, des côtes brumeuses de l’Irlande jusqu’au désert de Gobi, des rivages de la mer Rouge jusqu’aux fjords de Scandinavie.
Comment expliquer cette uniformité linguistique ?
Diverses hypothèses ont été proposées, dont deux impliquant des migrations de populations : en effet, certains proposent que les langues indo-européennes se soient répandues vers l’Europe, d’une part, et le sud de l’Asie, d’autre part, à la faveur de la diffusion de populations lors du Néolithique, à partir du Croissant fertile2 [1]. Mais d’autres archéologues, et en particulier Marija Gimbutas (1921-1994) dans les années 1950, suggèrent une théorie différente : en étudiant les tumulus kourganes d’Asie centrale, Marija Gimbutas avance que les langues indo-européennes se seraient diffusées par la migration d’un peuple originaire d’une région située entre la Volga et l’Oural, au nord de la mer Caspienne [2]. Ces locuteurs d’une langue protoeuropéenne auraient ensuite migré dès la fin du Néolithique vers l’Europe, mais aussi vers l’Asie centrale, puis vers l’Asie du Sud.
Cette question est l’une des premières questions à avoir intéressé les paléogénéticiens : est-il possible de mettre en évidence la diffusion d’une population, provenant des steppes du sud de la Russie, à la fin du Néolithique et aux débuts de l’âge du Bronze ?
La diffusion des populations des steppes
Dès 2015, deux publications [3,4] comparent la diversité génétique des populations européennes du Néolithique, et de l’âge du Bronze, avec celle des populations d’Asie centrale et du nord du Caucase. Dans les deux cas, un bouleversement démographique majeur apparaît à la fin du Néolithique (il y a environ 4500/5000 ans) en Europe du Nord et en Europe centrale : une nouvelle composante génétique associée aux populations des steppes, et en particulier aux populations de la culture des tombes en fosse (dite aussi Yamnaya), se développe et devient très rapidement majoritaire.
En Europe
En Europe du Nord, cette diffusion est principalement associée à l’expansion de la culture de la céramique cordée3, qui s’est étendue de la Pologne actuelle, vers l’ouest de l’Europe. Cette composante génétique atteint l’ouest de l’Europe en 2900-2700 av. J.-C. [5] (Figure 1). La diffusion de cette composante des steppes ne se fait pas de manière uniforme dans toutes les régions. Alors que, dans le reste de l’Europe, cette ancestralité venue des steppes se diffuse par le métissage avec les populations locales, la situation est différente dans les îles Britanniques. En effet, les individus du Néolithique de cette région étaient principalement apparentés aux fermiers de la péninsule ibérique. En revanche, à partir de l’âge du Bronze, conjointement à l’arrivée de la composante génétique venue des steppes et à l’expansion de la culture de la céramique cordée, la composante néolithique ibérique est remplacée par une composante néolithique d’Europe continentale. Cette observation suggère que ce ne sont pas des descendants directs des populations des steppes qui sont venus dans cette région, mais des individus déjà largement métissés avec les populations locales de l’ouest de l’Europe continentale, conduisant à un renouvellement de plus de 90 % des habitants de cette région [6].
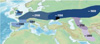 |
Figure 1 Diffusion de l’ancestralité des steppes au cours de la Protohistoire en Eurasie. Cette Figure simplifiée ne prend en compte que les génomes publiés pour l’instant. |
Si le nord de l’Europe est touché rapidement par ce phénomène, l’Europe du Sud n’est atteinte qu’au cours de l’âge du Bronze, voire au début de l’âge du Fer, et ce, malgré l’existence de cultures communes entre ces différentes régions. L’exemple le plus flagrant est celui de la culture campaniforme4. Cette culture se caractérise par l’inhumation de certaines personnes avec un attirail stéréotypé d’objets : une céramique en forme de cloche, une dague triangulaire en cuivre, un équipement d’archer, des boutons perforés en V, et un pendentif en forme de croissant de lune. Ce faciès culturel se retrouve dans tout l’ouest de l’Europe, du Portugal au nord de l’Italie, jusqu’au Danemark et dans les îles Britanniques. Pourtant, l’analyse paléogénétique des individus de la culture campaniforme [6] montre une grande hétérogénéité biologique, avec une absence totale d’ancestralité liée aux steppes dans la péninsule ibérique jusqu’en 2300 av. J.-C. [6,7]. Ce statut « campaniforme » n’était donc pas biologique, mais culturel !
Quant au pourtour de la Méditerranée, l’arrivée de la diversité génétique associée aux populations des steppes prend beaucoup plus de temps : elle est observée vers 2200 av. J.-C. en Sicile et dans le nord de l’Italie [8], et seulement à partir de l’âge du Fer en Sardaigne, aux alentours de 500 av. J.-C. [9] !
En Asie centrale et en Asie du Sud
Cette diffusion des populations des steppes s’étend également vers l’est. Les individus d’Asie centrale appartenant à différentes cultures, telles que la culture Afanasievo, Andronovo ou Sintashta, sont génétiquement très proches des Yamnaya, ce qui suggère une migration rapide de ces groupes d’éleveurs, peut-être en plusieurs phases de diffusion [3,4,10,11]. C’est seulement dans un second temps, à partir de l’âge du Bronze moyen (1600 -1400 av. J.-C.) que le métissage avec les populations locales se produit.
Vers 2000 avant notre ère, les contacts entre les populations des steppes et celles de la civilisation de l’Oxus, située dans le sud de l’Asie centrale, sont de plus en plus nombreux. Ces contacts sont associés à un flux de gènes issus des populations lointaines descendantes des Yamnaya [10]. Ce phénomène culminera à l’âge du Fer, période pendant laquelle 50 % du génome des quelques individus séquencés dérive de celui des populations des steppes [11]. Les lointains descendants de cette population forment aujourd’hui les populations d’Asie centrale de langue indo-iranienne, une langue indo-européenne, comme les Tadjiks ou les Yagnobs [12].
L’ancestralité venue des steppes s’étendra même encore plus au sud, jusqu’au sous-continent indien, où elle arrive entre 1900 et 1500 avant notre ère. Le métissage avec les populations locales donnera naissance aux populations actuelles et est encore visible, en particulier dans certaines castes, comme celle des brahmanes [10].
À la recherche de la population des steppes
Peut-on identifier précisément l’origine de ces populations des steppes ? Les premières analyses suggéraient que des individus de la culture Yamnaya étaient les plus représentatifs de cette diversité génétique. Ils portent dans leur génome des composantes associées à la fois aux chasseurs-cueilleurs du Caucase et aux chasseurs-cueilleurs de l’est de l’Europe. Cependant, ce modèle s’est avéré trop simpliste pour décrire cette diversité génétique : en effet, pour modéliser les premiers individus de la culture de la céramique cordée de Bohème, il a été nécessaire d’ajouter une composante génétique associée aux chasseurs-cueilleurs de l’Ukraine ou aux agriculteurs néolithiques provenant de Lettonie [13].
Récemment, des chercheurs ont publié une vaste étude sur la région située à l’ouest de la Russie et sud-est de l’Ukraine à la fin du Néolithique [14,15]. La diversité génétique des différentes populations qui peuplaient cette région se situe entre trois pôles : le premier représenté par les chasseurs-cueilleurs du Caucase, le deuxième par les chasseurs-cueilleurs de Sibérie, et le troisième par les chasseurs-cueilleurs ukrainiens (Figure 2), la diversité génétique des chasseurs-cueilleurs de l’est de l’Europe se situant entre ces deux derniers pôles. Les individus échantillonnés tirent leur diversité génétique de chacun de ces différents pôles, formant des clines5 qui suivent les vallées des principaux fleuves : le cline de la Haute Volga entre les chasseurs-cueilleurs de l’Ukraine et ceux d’Europe de l’est ; le cline de la Volga entre ceux d’Europe de l’Est, de la Basse Volga et du nord du Caucase, appelés le « groupe BP » ; et le cline du Dniepr qui relie la vallée de ce fleuve aux chasseurs-cueilleurs ukrainiens.
 |
Figure 2 Représentation schématique de la diversité génétique dans l’ouest de l’Asie à la fin de la préhistoire. A. Schéma de l’analyse en composantes principales (adaptée de [15]). Chaque groupe d’individus est représenté par un disque coloré. Plus les individus sont éloignés génétiquement, plus ils seront éloignés sur la Figure selon l’axe PC1 puis l’axe PC2. Les individus intermédiaires se situent dans les clines encadrés par les traits pointillés. B. La provenance de chaque groupe d’individus est représentée sur la carte avec le même code couleur. La taille des cercles indique le nombre d’individus échantillonnés dans chaque région. |
C’est dans ce cline que se situent les individus de la culture Yamnaya, à proximité du « groupe BP ». Le groupe le plus ancien montrant cette diversité génétique spécifique appartient à la culture de Serednii Sith, une culture très proche de celle des Yamnaya, qu’elle précède seulement de quelques siècles. Il apparaît donc que c’est dans cette région, au nord de la mer d’Azov, vers 4 000 avant notre ère, que le métissage ayant donné naissance à ces populations des steppes se soit produit. Et très rapidement, des individus appartenant à ce groupe génétique se sont répandus dans une région étendue sur des milliers de kilomètres.
En atteignant le nord de l’Ukraine et le sud de la Pologne actuelle, ils se métissent avec les agriculteurs locaux de la culture des amphores globulaires [13], et leurs descendants, appartenant à la culture de la céramique cordée, migreront jusqu’à l’ouest de l’Europe.
Un phénomène social complexe
La diffusion de la composante génétique des steppes montre un biais marqué selon le sexe des individus. Au niveau du génome mitochondrial, l’impact de cette diffusion est très limité ; en revanche, les haplogroupes6 Y R1a/b, associés aux populations des steppes, deviennent rapidement majoritaires, jusqu’à représenter près de 55 % des haplogroupes Y des Européens actuels. En comparant la composante génétique des steppes sur le chromosome X (transmis 2 fois sur 3 par une femme), et les autosomes (transmis 1 fois sur 2 par une femme), il a été suggéré que le métissage avec les populations des steppes impliquait 14 fois plus d’hommes que de femmes [16]. Le même phénomène apparaît dans le sud de l’Asie : les populations d’Inde ont aussi hérité la part de leur génome provenant des populations des steppes, principalement par les mâles. [10]. Faut-il pour autant imaginer un déferlement belliqueux de groupes des steppes, tuant les hommes et s’accouplant avec les femmes locales ? Pas forcément. En effet, la modélisation d’un changement de structure de parenté, impliquant patrilinéarité7, et la transmission du succès reproductif, permet d’obtenir des résultats tout aussi biaisés en fonction du sexe [17]. Effectivement, l’étude d’individus de l’âge du Bronze provenant de la vallée de Lech, dans le sud de l’Allemagne, accrédite cette hypothèse, car seuls les hommes adultes sont inhumés avec leurs parents biologiques. De plus, les hommes adultes qui ne possèdent pas l’haplogroupe Y R1b, et ne descendent donc pas des populations des steppes par la lignée paternelle, ne sont pas inhumés avec des apparentés et possèdent moins de biens funéraires, en particulier d’armes [18]. L’étude d’individus de la culture de la céramique cordée de Bohème montre que l’augmentation de la fréquence de l’haplogroupe R1a ne peut être expliquée que par un taux de survie ou de reproduction moyen supérieur de 15 %, par génération des mâles porteurs de cet haplogroupe, comparé aux autres mâles [13]. L’arrivée des descendants des Yamnaya a, non seulement, été accompagnée d’un probable changement de langue, mais aussi d’une restructuration profonde des sociétés.
Diffusion des populations des steppes et phénotype
Quel a été l’impact de ces populations des steppes sur le phénotype des populations eurasiatiques ?
L’un des phénotypes les plus étudiés en paléogénétique est l’expression de la lactase après l’âge du sevrage. Ce phénotype, causé par une ou plusieurs mutations dans la région régulatrice du gène de la lactase, se retrouve dans plusieurs régions du monde, et en particulier dans le nord-ouest de l’Europe et dans le sud de l’Asie, là où la composante génétique associée aux steppes est forte [19]. L’hypothèse selon laquelle cette mutation serait apparue chez les Yamnaya ou leurs ancêtres, des éleveurs, et se serait ensuite transmise à leurs descendants est donc séduisante. De plus, les plus anciennes traces du génotype associé n’apparaissent en Europe qu’après l’arrivée des populations des steppes mais n’ont pas pour autant été identifiées dans ces populations avant l’âge du Bronze [20]! Néanmoins, un analyse de sélection prenant en compte l’ancestralité des régions du génome étudiées pour chaque individu montre que la sélection a principalement porté sur les fragments hérités des chasseurscueilleurs de l’est de l’Europe et du Caucase, les ancêtres putatifs des Yamnaya [21]. Même si des données complémentaires seront nécessaires, il semble donc bien que la capacité de boire du lait à l’âge adulte en Eurasie soit un lointain héritage des populations des steppes !
Certains de ces phénotypes sont en revanche plus délétères. La sclérose en plaques est une maladie neurodégénérative qui touche 2,5 millions de personnes dans le monde et dont la prévalence la plus élevée est observée en Europe du Nord. 233 variants génétiques sont associés à des facteurs de risque de développer cette maladie, dont 32 sont situés dans la région HLA. Parmi ces derniers, 30 proviennent des populations des steppes, où ils auraient été soumis à une sélection récente [22]. Certains de ces variants étant connus pour être protecteurs vis-à-vis de certaines maladies infectieuses (comme la tuberculose, par exemple), il est probable qu’ils aient été sélectionnés dans un contexte environnemental différent.
La fin du Néolithique et l’âge du Bronze ont donc été des périodes de profond bouleversement en Eurasie. La diffusion des populations des steppes a induit un changement profond dans les pratiques sociales. Outre une nouvelle diversité génétique traduisant une adaptation à de nouveaux modes de vie, ces populations ont diffusé avec elles de nouvelles pratiques culturelles, et une nouvelle langue, dont les descendantes sont parlées aujourd’hui dans une vaste partie de l’Eurasie. Une première mondialisation, en quelque sorte, dont les conséquences se font encore sentir 5 000 ans plus tard dans les populations modernes.
Liens d’intérêt
L’auteure déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Renfrew C. Archaeology and Language The Puzzle of Indo-European Origins. Jonathan C. London, 1987 : 386 p. [Google Scholar]
- Gimbutas M. The Prehistory of Eastern Europe. Part I: Mesolithic, Neolithic and Copper Age Cultures in Russia and the Baltic Area. Peabody Mu. Hencken H, Eds Cambridge, Massachusetts, 1956 : p. [Google Scholar]
- Allentoft ME, Sikora M, Sjögren KG, et al. Population genomics of Bronze Age Eurasia. Nature 2015 ; 522 : 167–72. [CrossRef] [PubMed] [Google Scholar]
- Haak W, Lazaridis I, Patterson N, et al. Massive migration from the steppe was a source for Indo-European languages in Europe. Nature 2015 ; 522 : 207–11. [CrossRef] [Google Scholar]
- Furtwängler A, Rohrlach AB, Lamnidis TC, et al. Ancient genomes reveal social and genetic structure of Late Neolithic Switzerland. Nat Commun 2020 ; 11 : 1–11. [CrossRef] [PubMed] [Google Scholar]
- Olalde I, Brace S, Allentoft ME, et al. The Beaker phenomenon and the genomic transformation of northwest Europe. Nature 2018 ; 555 : 190–96. [Google Scholar]
- Olalde I, Mallick S, Patterson N, et al. The genomic history of the Iberian Peninsula over the past 8000 years. Science 2019 ; 363 : 1230–4. [Google Scholar]
- Saupe T, Montinaro F, Scaggion C, et al. Ancient genomes reveal structural shifts after the arrival of Steppe-related ancestry in the Italian Peninsula. Curr Biol 2021 ; 31 : 2576–91.e12. [Google Scholar]
- Fernandes DM, Mittnik A, Olalde I, et al. The spread of steppe and Iranian-related ancestry in the islands of the western Mediterranean. Nat Ecol Evol 2020 ; 4 : 334–345. [Google Scholar]
- Narasimhan VM, Patterson N, Moorjani P, et al. The formation of human populations in South and Central Asia. Science 2019 ; 365 : eaat7487. [Google Scholar]
- Barros Damgaard P de, Martiniano R, Kamm J, et al. The first horse herders and the impact of early Bronze Age steppe expansions into Asia. Science 2018 ; 360 : eaar7711. [Google Scholar]
- Guarino-Vignon P, Marchi N, Bendezu-Sarmiento J, et al. Genetic continuity of Indo-Iranian speakers since the Iron Age in southern Central Asia. Sci Rep 2022 ; 12 : 1–13. [CrossRef] [PubMed] [Google Scholar]
- Papac L, Ernée M, Dobeš M, et al. Dynamic changes in genomic and social structures in third millennium BCE central Europe. Sci Adv 2021 ; 7 : eabi6941. [Google Scholar]
- Nikitin AG, Lazaridis I, Patterson N, et al. A genomic history of the North Pontic Region from the Neolithic to the Bronze Age. Nature 2025 ; 639 : 124–31. [Google Scholar]
- Lazaridis I, Patterson N, Anthony D, et al. The genetic origin of the Indo-Europeans. Nature 2025 ; 639 : 132–42. [Google Scholar]
- Goldberg A, Günther T, Rosenberg NA, et al. Ancient X chromosomes reveal contrasting sex bias in Neolithic and Bronze Age Eurasian migrations. Proc Natl Acad Sci USA 2017 ; 114 : 2657–62. [Google Scholar]
- Guyon L, Guez J, Toupance B, et al. Patrilineal segmentary systems provide a peaceful explanation for the post-Neolithic Y-chromosome bottleneck. Nat Commun 2024 ; 15 : 1–16. [Google Scholar]
- Knipper C, Mittnik A, Massy K, et al. Female exogamy and gene pool diversification at the transition from the Final Neolithic to the Early Bronze Age in central Europe. Proc Natl Acad Sci USA 2017 ; 114 : 10083–8. [Google Scholar]
- Ségurel L, Bon C. On the Evolution of Lactase Persistence in Humans. Annu Rev Genomics Hum Genet 2017 ; 18 : 297–319. [Google Scholar]
- Segurel L, Guarino-Vignon P, Marchi N, et al. Why and when was lactase persistence selected for? Insights from central Asian herders and ancient DNA. PLoS Biol 2020 ; 18 : 1–11. [Google Scholar]
- Irving-Pease EK, Refoyo-Martínez A, Barrie W, et al. The selection landscape and genetic legacy of ancient Eurasians. Nature 2024 ; 625 : 312–20. [Google Scholar]
- Barrie W, Yang Y, Irving-Pease EK, et al. Elevated genetic risk for multiple sclerosis emerged in steppe pastoralist populations. Nature 2024 ; 625 : 321–8. [Google Scholar]
Une langue parlée en Inde
Région du Proche-Orient, qui s’étend de la mer Morte au golfe Persique en passant par le sud de la Turquie, le nord de l’Iraq et l’Iran occidental. Les pays qu’elle regroupe, riches en plaines et en vallées bien arrosées, ont vu naître l’agriculture au néolithique.
Il s‘agit d’une culture du Néolithique final qui s’est développée en Europe du Nord d’environ 3000 à 2200 av. J.-C. Elle doit son nom à ses poteries caractéristiques, décorées par impression de cordelettes sur l’argile crue.
Culture qui se développa en Europe ainsi qu’en Afrique du Nord approximativement au cours du IIIe millénaire avant notre ère. Elle doit son nom aux gobelets céramiques en forme typique de cloche retrouvés dans les sépultures.
Variation spatiale graduelle entre deux groupes d’individus au sein d’une espèce, sous-espèce ou population.
Un haplogroupe est un grand groupe d’haplotypes, qui sont des séries d’allèles situés à des sites spécifiques dans un chromosome et qui sont définis par des mutations par polymorphisme nucléotidique singulier.
Mode de filiation pour lequel seule compte la parenté paternelle.
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Diffusion de l’ancestralité des steppes au cours de la Protohistoire en Eurasie. Cette Figure simplifiée ne prend en compte que les génomes publiés pour l’instant. |
| Dans le texte | |
 |
Figure 2 Représentation schématique de la diversité génétique dans l’ouest de l’Asie à la fin de la préhistoire. A. Schéma de l’analyse en composantes principales (adaptée de [15]). Chaque groupe d’individus est représenté par un disque coloré. Plus les individus sont éloignés génétiquement, plus ils seront éloignés sur la Figure selon l’axe PC1 puis l’axe PC2. Les individus intermédiaires se situent dans les clines encadrés par les traits pointillés. B. La provenance de chaque groupe d’individus est représentée sur la carte avec le même code couleur. La taille des cercles indique le nombre d’individus échantillonnés dans chaque région. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




